Определение болезни. Причины заболевания
Пограничные опухоли яичников (ПОЯ; Borderline ovarian tumors) — это эпителиальные опухоли, клетки которых активно размножаются, но при этом не проникают вглубь окружающих тканей, т. е. являются неинвазивными. Такие новообразования остаются ограниченными оболочкой, что отличает их от настоящего рака яичников.
Пограничная опухоль яичника
По своему биологическому поведению пограничные опухоли значительно менее опасны, чем инвазивный рак яичников: они отличаются медленным ростом и крайне редко дают отдалённые метастазы, а правильное хирургическое лечение зачастую сопровождается благоприятным прогнозом [1][2][3][4][5].
ПОЯ составляют примерно 15–20 % от всех эпителиальных новообразований яичников. В отличие от инвазивного рака, их обычно диагностируют у женщин репродуктивного возраста и в период пременопаузы, т. е. в более молодом возрасте [3]. У многих пациенток пограничную опухоль обнаруживают случайно, например во время планового ультразвукового исследования (УЗИ) органов малого таза или при операции, выполненной по другому поводу [1].
Среди ПОЯ преобладают два основных типа: серозные и муцинозные варианты. Значительно реже встречаются эндометриоидные формы, опухоль Бреннера и некоторые другие редкие разновидности [4].
Причины развития пограничных опухолей яичников
Точные причины формирования ПОЯ неизвестны. Ситуация с факторами риска также остаётся неоднозначной. Например, в литературе описаны семейные случаи опухолей яичников и молочной железы, однако убедительной связи пограничных опухолей с наследственными синдромами, такими как BRCA-ассоциированный рак или синдром Линча, не установлено. Большинство исследований не находят характерных мутаций в генах BRCA1/BRCA2 и выраженного семейного накопления, типичного для рака яичников [26][25][27].
Среди репродуктивных факторов, которые могут повышать риск развития пограничных опухолей, выделяют отсутствие или поздние первые роды, а также длительный период активной овуляции (раннее начало менструаций, позднее наступление менопаузы). При этом многократные доношенные беременности и длительный приём комбинированных оральных контрацептивов, напротив, связаны со снижением риска развития ПОЯ [5]. Однако важно понимать, что все упомянутые факторы носят вероятностный характер: они не гарантируют возникновения или отсутствия опухоли, а лишь указывают на общую частоту таких случаев в популяции [1][4][9].
Симптомы пограничных опухолей яичников
На ранних стадиях ПОЯ обычно никак себя не проявляет. Небольшое образование часто находят случайно во время плановых обследований. Но по мере увеличения опухоли она начинает давить на окружающие ткани и органы, что сопровождается тянущими или ноющими болями в нижней части живота, вздутием, чувством тяжести и дискомфортом при физической активности. Некоторые пациентки также отмечают быстрое насыщение даже после небольшого количества пищи, а также заметное увеличение объёма живота [1][2][4][9].
Если опухоль имеет кистозное строение или состоит из нескольких крупных камер, она может механически сдавливать соседние органы. В таких случаях возникают запоры, ощущение неполного опорожнения кишечника после дефекации, учащённые позывы или, наоборот, затруднённое мочеиспускание.
Обычно ПОЯ никак не влияют на менструальный цикл, но иногда пациентки отмечают кровянистые выделения между месячными, усиление менструальной боли и нерегулярность цикла. Также возможен дискомфорт или болезненность во время полового акта.
Самое серьёзное состояние при ПОЯ — перекрут ножки опухоли, при котором развиваются симптомы «острого живота»: появляется внезапная очень сильная боль внизу живота, быстро нарастают тошнота и общая слабость, часто повышается температура тела. При таком состоянии требуется немедленное хирургическое вмешательство [1][8][9][11].
Патогенез пограничных опухолей яичников
В норме поверхностный эпителий яичника и внутренний эпителий кистозных образований постоянно подвергаются небольшим повреждениям и последующему восстановлению. Особенно активно эти процессы протекают во время овуляции, когда яйцеклетка выходит из фолликула, оставляя небольшой дефект на поверхности яичника, который в скором времени исчезает без внешней помощи. Однако ситуация может измениться при сочетании определённых условий, например генетической предрасположенности и длительного воздействия гормональных факторов. Тогда в некоторых участках эпителия могут возникать изменения: клетки начинают делиться быстрее обычного и приобретают признаки атипии, т. е. их структура меняется [12][13].
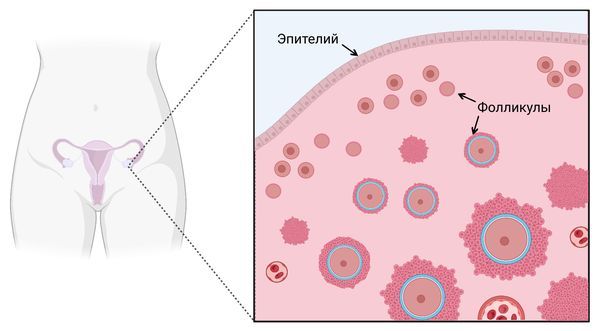
Поверхностный эпителий яичника
Для ПОЯ характерна выраженная пролиферация (активное размножение) эпителиальных клеток с формированием сосочковых выростов и сложных перегородок, при этом они не прорастают в строму (окружающую соединительную ткань) яичника, что отличает их от доброкачественных цистаденом и злокачественных опухолей. Учёные также обнаружили их различия на молекулярном уровне, ещё раз подтвердив, что пограничные опухоли и рак яичников развиваются по принципиально разным биологическим сценариям [12][13].
Считается, что значительная часть ПОЯ возникает из ранее существовавших доброкачественных кистозных образований или эндометриоидных кист путём постепенного накапливания генетических нарушений, которые в результате приводят к активному разрастанию эпителиальной ткани.
В небольшом проценте случаев, особенно при микропапиллярных опухолях с мелкими сосочковыми выростами и перитонеальных имплантах (опухолевых очагах на брюшине и сальнике, морфологически сходных с первичной опухолью яичника), возможна дальнейшая трансформация ПОЯ в инвазивный рак низкой степени злокачественности. Причём прогноз при инвазивных имплантах менее благоприятный. Именно поэтому важно провести онкологическое стадирование и полностью удалить всю видимую опухолевую ткань, чтобы исключить скрытое распространение и правильно оценить риск прогрессирования заболевания [1][4][10][12].
![Виды перитонеальных имплантов [31] Виды перитонеальных имплантов [31]](/media/bolezny/pogranichnye-opuholi-yaichnikov/vidy-peritonealnyh-implantov-31_s.jpeg?dummy=1771570217813)
Виды перитонеальных имплантов [31]
Классификация и стадии развития пограничных опухолей яичников
Основная классификация ПОЯ основана на гистологическом (тканевом) строении опухолей. К основным типам относятся серозные, муцинозные и серомуцинозные, эндометриоидные опухоли, опухоль Бреннера, а также некоторые редкие варианты [2]. Среди них чаще всего встречаются серозные и муцинозные формы.
Серозные пограничные опухоли нередко сопровождаются появлением перитонеальных имплантов и иногда имеют микропапиллярный вариант строения — с очень мелкими сосочковыми выростами. Они связаны с более высоким риском рецидива (возвращением болезни после излечения). Муцинозные пограничные опухоли, напротив, обычно выглядят как крупные многокамерные кисты [4][5][6][24].
![Микропапиллярная опухоль на МРТ [32] Микропапиллярная опухоль на МРТ [32]](/media/bolezny/pogranichnye-opuholi-yaichnikov/mikropapillyarnaya-opuhol-na-mrt-32_s.jpeg?dummy=1771570258448)
Микропапиллярная опухоль на МРТ [32]
Стадии развития пограничных опухолей яичников
Для определения стадии процесса используется международная система TNM и классификация FIGO, разработанная для эпителиальных опухолей яичников. Стадия зависит от того, ограничена ли опухоль одним или обоими яичниками, есть ли опухолевые очаги на их поверхности, распространились ли изменения на брюшину, имеется ли жидкость в брюшной полости (асцит), поражены ли отдалённые органы. Все эти критерии учитываются при выборе лечения, например, есть ли необходимость удалять яичник. Это особенно важно, когда речь идёт о сохранении репродуктивной функции у женщин молодого возраста [1][4][7].
На I стадии опухоль остаётся строго в пределах яичников. На более поздних стадиях появляются импланты на брюшине, могут поражаться близлежащие лимфоузлы или возникать отдалённые очаги. Важно, что даже при распространённом процессе прогноз при пограничных опухолях обычно значительно лучше, чем при инвазивном раке яичников той же стадии [1][2][3][4].
По классификации FIGO стадии определяются следующим образом:
- стадия I — опухоль ограничена одним (IA) или обоими (IB) яичниками или маточными трубами, также выделяют стадию IC, когда опухоль расположена на поверхности яичника, есть разрыв капсулы или обнаружены опухолевые клетки в асците/промывных водах;
- стадия II — опухоль распространяется на другие органы малого таза (матку, маточные трубы, другие тазовые структуры);
- стадия III — определяется поражение брюшины за пределами малого таза и/или близлежащих лимфоузлов;
- стадия IV — появляются отдалённые метастазы в ткани печени, лёгких и других органов, за исключением внутрибрюшных поверхностей [28].
Осложнения пограничных опухолей яичников
Основные осложнения связаны с ростом опухолей и механическим давлением на соседние органы и ткани. Самые серьёзные из них возникают внезапно и требуют немедленной медицинской помощи. К ним относятся:
- перекрут ножки опухоли — из-за нарушения кровоснабжения ткани опухоли у пациентки развивается острая и сильная боль, также может начаться некроз (отмирание) тканей;
- разрыв капсулы кистозной опухоли — в этом случае всё её содержимое изливается в брюшную полость, что вызывает резкую боль и раздражение брюшины;
- сдавление кишечника и мочевого пузыря — сопровождается запорами, болью при дефекации, чувством неполного опорожнения кишечника, частыми или затруднёнными мочеиспусканиями [8][10].
У серозных пограничных опухолей с перитонеальными имплантами сохраняется риск рецидива после лечения, а в редких случаях (особенно при микропапиллярном варианте строения и когда опухолевая ткань удалена не полностью) — дальнейшая трансформация в инвазивный рак низкой степени злокачественности.
Разрыв муцинозной опухоли может привести к развитию псевдомиксомы брюшины — состоянию, при котором в брюшной полости накапливается большое количество густой слизистой массы. Этот риск повышается, если до разрыва опухоль уже имела признаки метастатического роста. Однако это крайне редкое осложнение, которое рассматривают скорее как необычный вариант течения болезни [28].
![Виды псевдомиксомы брюшины [33] Виды псевдомиксомы брюшины [33]](/media/bolezny/pogranichnye-opuholi-yaichnikov/vidy-psevdomiksomy-bryushiny-33_s_VaOmBHq.jpeg?dummy=1771570313232)
Виды псевдомиксомы брюшины [33]
Для женщин репродуктивного возраста самым тяжёлым возможным последствием становится необходимость радикальной операции — удаления матки вместе с обоими яичниками и маточными трубами. Такое вмешательство лишает их способности забеременеть и самостоятельно родить ребёнка. Именно поэтому врачи стремятся максимально сохранить хотя бы один яичник, если это безопасно с онкологической точки зрения [1][2][4][14].
Диагностика пограничных опухолей яичников
При подозрении на опухоль яичника женщине следует как можно скорее обратиться к гинекологу.
На первом приёме врач собирает подробный анамнез (историю болезни и жизни) пациентки. Он расспрашивает её о жалобах, когда и как они появились, какой характер болей, менялся ли менструальный цикл, сколько у неё было беременностей и родов, не диагностировали ли ранее бесплодие и не проводила ли она стимуляцию овуляции. Специалист обязательно уточняет семейный анамнез: были ли у близких родственниц опухоли яичников или молочных желёз.
Затем врач проводит гинекологический осмотр, включая бимануальное (двумя руками) исследование, в ходе которого оценивает размеры, плотность и подвижность яичников и маточных труб, признаки объёмного образования и асцита. Особенно большое внимание уделяют любым опухолям яичников у женщин в пре- и менопаузе, даже если у них нет никаких симптомов, так как у них повышен риск развития рака [1][2].

Бимануальное исследование
Инструментальная диагностика
Главный и самый доступный метод первичной диагностики — трансвагинальное ультразвуковое исследование органов малого таза. При очень крупных образованиях его дополняют трансабдоминальным УЗИ (через переднюю брюшную стенку). Во время исследования врач измеряет размер опухоли, определяет, сколько в ней камер, как выглядят перегородки (их толщина, структура), есть ли внутри сосочковые выросты, плотные (солидные) участки, какова плотность (эхогенность) содержимого, насколько активно кровоснабжаются подозрительные зоны и есть ли свободная жидкость в брюшной полости. Многокамерные сложные кисты с тонкими или умеренно утолщёнными перегородками, сосочковыми разрастаниями, но без крупных плотных узлов и бурного кровотока часто наводят на мысль о пограничной опухоли. Однако уверенно отличить пограничную опухоль от ранней стадии инвазивного рака с помощью лишь одного УЗИ невозможно.

Трансвагинальное УЗИ
Для более точной оценки брюшины, сальника и лимфоузлов применяют магнитно-резонансную томографию (МРТ) органов малого таза и компьютерную томографию (КТ) брюшной полости и грудной клетки с внутривенным контрастированием. МРТ помогает лучше охарактеризовать структуру сложных кистозных образований и отличить их от эндометриоидных кист, доброкачественных муцинозных цистаденом и метастатических поражений [15][16].
Для стандартизации описания УЗ-картины и оценки риска злокачественности широко используется международная система O-RADS. С её помощью опухоли присваивают ту или иную категорию риска на основании совокупности признаков (строения кисты, наличия сосочков и плотных компонентов, характера кровотока, асцита). Это помогает врачу решить, нужно ли направлять пациентку в специализированный онкогинекологический центр для операции [28].
Дополнительно могут провести исследование по определению уровня онкомаркеров в крови. Наиболее широко используется анализ на уровень СА 125, который может умеренно повышаться при эпителиальных опухолях яичников, но при пограничных опухолях обычно не меняется или слегка увеличивается. Кроме того, СА 125 может расти и при совершенно других состояниях, например при эндометриозе, миоме матки и воспалении органов малого таза. При подозрении на муцинозный тип дополнительно смотрят СА 19-9, РЭА, СА 72-4, а также HE4 и комбинированный индекс ROMA. Однако современные данные показывают, что ни один из этих маркеров не позволяет надёжно разделить доброкачественные, пограничные и злокачественные образования. Поэтому онкомаркеры используют в основном для общей оценки риска, а не как главный критерий постановки диагноза [15][17][18].
Если есть подозрение именно на муцинозную пограничную опухоль, обязательно проводят гастроскопию и колоноскопию, чтобы исключить рак желудка, поджелудочной железы или толстой кишки с метастазами в яичники.
Однако окончательный диагноз можно поставить только после морфологического исследования удалённой опухоли. Для правильного заключения требуется большое количество срезов (особенно из сосочковых и плотных участков), правильная фиксация материала и опыт врача, который хорошо знает тонкие различия между доброкачественными цистаденомами, пограничными опухолями и инвазивным раком. В сложных случаях — при микропапиллярном росте, имплантах или сомнениях в наличии инвазии — препараты отправляют на пересмотр в референс-центры. Иногда врачи делают срочное гистологическое исследование во время операции, но при ПОЯ его точность ограничена, особенно при микропапиллярных формах и имплантах [19][20].
Дифференциальная диагностика
Прежде всего ПОЯ отличают от функциональных кист яичников (фолликулярных или кист жёлтого тела). Обычно они состоят из одной камеры и тонкой стенки, без плотных включений, и исчезают сами.
Доброкачественные серозные и муцинозные цистаденомы могут напоминать многокамерные кисты, но для них нехарактерны множественные сосочковые выросты и сложное строение. Эндометриоидные кисты (эндометриомы) чаще однокамерные или малокамерные, с густым «шоколадным» содержимым и характерной УЗ-картиной, но если внутри появляются узлы и кровоток, необходимо исключать пограничную или злокачественную опухоль [21][22].
Среди злокачественных образований ПОЯ дифференцируют с инвазивным раком яичников, особенно ранними стадиями низкозлокачественного серозного рака: у них чаще бывают крупные плотные участки, чрезмерный патологический кровоток, толстые перегородки и заметно более высокий уровень СА 125. При муцинозных опухолях важно отличить первичную пограничную опухоль от метастазов в яичники (чаще из желудка или толстой кишки). Метастазы обычно поражают оба яичника, при этом опухоли меньше по размеру, включают в себя множество мелких камер и выраженный плотный компонент. Исключить метастазы помогают признаки первичного очага в другом органе при обследовании или соответствующие данные в анамнезе. ПОЯ также дифференцируют с фибромами, текомами, гранулёзоклеточными опухолями, зрелыми тератомами, светлоклеточным и эндометриоидным раком на фоне эндометриоза [16][20][21].
Лечение пограничных опухолей яичников
Основной метод лечения — хирургический. Операция всегда сопровождается тщательным онкологическим стадированием, т. е. определением точной распространённости процесса. Объём вмешательства подбирают индивидуально, учитывая возраст женщины, её планы на беременность, размеры и расположение опухоли, её гистологический тип и наличие перитонеальных имплантов [1][3][4].
У молодых женщин с поражением только одного яичника часто выбирают органосохраняющую операцию — удаление повреждённого органа (односторонняя оварэктомия) или его частичная резекция с сохранением матки и второго яичника. Такие операции проводят только у тщательно отобранных пациенток (в первую очередь при I–II стадии) и исключительно в специализированных центрах. При более распространённом процессе возможность сохранения фертильности (способности забеременеть) обсуждают индивидуально, взвешивая риск рецидива. Чаще всего такие решения принимают в федеральных онкологических центрах.
Чтобы определить точную стадию, во время операции обязательно проводят полную ревизию брюшной полости: осматривают органы, берут смывы с поверхности брюшины и, при необходимости, выполняют биопсию подозрительных участков [1][4][7][11].
У женщин в пре- и менопаузе, а также при двустороннем поражении, микропапиллярном варианте опухоли, наличии имплантов или подозрении на инвазивный компонент чаще выполняют радикальную операцию — удаление матки вместе с обоими яичниками, маточными трубами и большим сальником [28][29].
Операцию могут выполнять лапароскопическим доступом (через небольшие проколы). В этом случае хирурги используют специальные одноразовые контейнеры — эндобэги. Опухоль помещают в эндобэг внутри брюшной полости, а затем извлекают через мини-разрез. Это существенно снижает риск разрыва кисты и разлития её содержимого в брюшину [1][2][4].
Эндобэг
В отличие от инвазивного рака яичников, при классических пограничных опухолях адъювантную (послеоперационную) химиотерапию, как правило, не назначают, особенно на ранних стадиях и при полном удалении опухоли. Многочисленные исследования и метаанализы не выявили убедительного улучшения выживаемости при её применении. Химиотерапию рассматривают только в редких спорных ситуациях после обсуждения на мультидисциплинарном консилиуме с учётом актуальных международных рекомендаций [16][29][30].
После завершения лечения всем пациенткам назначают регулярное динамическое наблюдение: периодические осмотры у онкогинеколога, УЗИ органов малого таза и/или брюшной полости, при необходимости — КТ или МРТ. Если до операции были повышены онкомаркеры (например, СА 125), их уровень также контролируют, чтобы как можно раньше выявить возможный рецидив [23].
Прогноз. Профилактика
Прогноз при ПОЯ в целом благоприятный и существенно лучше, чем при инвазивном раке яичников. Особенно высокие показатели выживаемости наблюдаются на ранних стадиях заболевания и при полном удалении всей видимой опухолевой ткани. Подавляющее большинство женщин живут долгие годы без признаков рецидива, а при органосохраняющем лечении значительная часть пациенток сохраняет возможность забеременеть и родить ребёнка естественным путём [1][2][4].
По данным исследований, 5-летняя общая выживаемость при ПОЯ достигает примерно 97 %. Даже на II–III стадиях 5-летняя выживаемость остаётся высокой — от 70 до 90 %. Однако при наличии инвазивных имплантов прогноз заметно ухудшается: 5-летняя выживаемость снижается примерно до 30 % [28][29].
Вероятность рецидива зависит от нескольких ключевых факторов: гистологического типа опухоли, наличия и характера перитонеальных имплантов, полноты выполненной операции и того, сохранялась ли часть яичниковой ткани. После органосохраняющих вмешательств рецидивы случаются чаще, чем после радикальных операций, но в большинстве случаев они ограничены областью малого таза или брюшной полости и хорошо поддаются повторному хирургическому лечению, т. е. благоприятный прогноз сохраняется.
Самый высокий риск повторного роста и перехода в инвазивный рак низкой степени злокачественности отмечается при микропапиллярных серозных вариантах и инвазивных имплантах [1][4][10][12].
Профилактика пограничных опухолей яичников
Специфических методов профилактики пограничных опухолей яичников пока не существует. Потенциально полезными могут стать меры по снижению общих факторов риска:
- поддержание нормальной массы тела;
- отказ от курения;
- своевременное лечение воспалительных заболеваний органов малого таза.
Кроме того, даже при отсутствии симптомов важно регулярно проходить осмотры у гинеколога, выполнять УЗИ органов малого таза, внимательно относиться к изменениям менструального цикла и появлению боли внизу живота. Это позволит выявить опухоль на ранней стадии, когда ещё возможно проведение органосохраняющей операции [1][2][23].
Список литературы
Ассоциация онкологов России. Пограничные опухоли яичников: клинические рекомендации. — М., 2024.
Министерства здравоохранения Республики Казахстан. Рак яичников, включая рак фаллопиевой трубы и первичную перитонеальную карциному: клинические рекомендации // Medelement. — 2022.
Давыдова И. Ю., Ашрафян Л. А., Валиев Р. К. и др. Практические рекомендации по лечению пограничных опухолей яичников // Практические рекомендации RUSSCO. — 2024. — № 3s2. — С. 124–135.
Ассоциация онкологов России. Пограничные опухоли яичников: клинические рекомендации. — М., 2020.
Оразов М. Р., Киселева М. В., Пернай В. М. Пограничные опухоли яичников у женщин репродуктивного возраста: диагностика, лечение // Клинический разбор в общей медицине. — 2024. — № 7. — С. 83–90.
Ledermann J., Matias-Guiu X., Fagotti A. et al. Ovarian Cancer Pocket Guidelines // ESGO–ESMO–ESP Consensus Recommendations. — 2025.
Sadlecki P., Dejewska K., Domieracka P. et al. Giant borderline ovarian tumours — review of the literature // Open Med (Wars). — 2025. — № 1. ссылка
Ашрафян Л. А., Новикова Е. Г., Хохлова С. В. и др. Пограничные опухоли яичников: информация для пациента. — М., 2024.
Черенков В. Г. Клиническая онкология: учебное пособие для системы последипломного образования врачей. — 3-е издание, исправленное и дополненное. — М.: Медицинская книга, 2010. — 434 с.
Della Corte L., Mercorio A., Serafino P. et al. The challenging management of borderline ovarian tumors (BOTs) in women of childbearing age // Front Surg. — 2022. — Vol. 9. ссылка
Maramai M. et al. Borderline ovarian tumours: management in the era of fertility-sparing surgery // Ecancermedicalscience. — 2020. — Vol. 14.ссылка
Baker R. E. Borderline ovarian tumours // The Obstetrician & Gynaecologist. — 2025.
Singer G., Kurman R. J., Chang H. W. et al. Molecular pathogenesis of ovarian borderline tumors // Clin Cancer Res. — 2005. — № 20. — P. 7273–7279.ссылка
Bonadio R. C., de Siqueira Santos A. G., Estevez-Diz M. D. P. Borderline ovarian tumors: a review of its biology, molecular profile and current management // Rev Bras Ginecol Obstet. — 2023.
Gotlieb W. H., Soriano D., Achiron R. et al. CA 125 measurement and ultrasonography in borderline tumors of the ovary // Am J Obstet Gynecol. — 2000. — № 3. — P. 541–546. ссылка
de Souza N. M., O’Neill R., McIndoe G. A. et al. Borderline tumors of the ovary: CT and MRI features and tumor markers in differentiation from stage I disease // AJR Am J Roentgenol. — 2005. — № 3. — P. 999–1003. ссылка
Van Gorp T., Cadron I., Despierre E. et al. HE4 and CA125 as a diagnostic test in ovarian cancer: prospective validation of the Risk of Ovarian Malignancy Algorithm // Br J Cancer. — 2011. — № 5. — P. 863–870. ссылка
Nyangoh-Timoh K., Bendifallah S., Dion L. et al. Tumeurs frontières de l’ovaire. Recommandations pour la pratique clinique du CNGOF – Pertinence des marqueurs tumoraux // Gynécologie Obstétrique Fertilité & Sénologie. — 2020. — № 3. — P. 277–286.ссылка
Gizzo S., Berretta R., Di Gangi S. et al. Borderline ovarian tumors and diagnostic dilemma of intraoperative diagnosis: Could preoperative He4 assay and ROMA score assessment increase the frozen section accuracy? A multicenter case-control study // BioMed Res Int. — 2014. — Vol. 2014. ссылка
Fischerova D., Zikan M., Dundr P., Cibula D. Diagnosis, treatment, and follow-up of borderline ovarian tumors // Oncologist. — 2012. — № 12. — P. 1515–1533.ссылка
Yoeli-Bik R., Lengyel E., Timor-Tritsch I. E. et al. The Ultrasonography Characteristics of Borderline Ovarian Tumor Subtypes // J Ultrasound Med. — 2025. — № 11. — P. 2133–2146. ссылка
Testa A. C., Timmerman D., Van Holsbeke C. et al. Ovarian cancer arising in endometrioid cysts: ultrasound findings // Ultrasound Obstet Gynecol. — 2011. — № 1. — P. 99–106. ссылка
Chen S., Huang L., Liang M. et al. Advances in understanding the molecular mechanisms of borderline ovarian tumors // Front Mol Biosci. — 2024. — Vol. 11.
Pilone V., Tramontano S., Picarelli P. et al. Giant mucinous ovarian borderline tumor. A good lesson from an asymptomatic case // Int J Surg Case Rep. — 2018. — Vol. 50. — P. 25–27.ссылка
Park J. M., Kim M. K. Hereditary risk evaluation for borderline ovarian tumors based on immunohistochemistry // J Menopausal Med. — 2014. — № 1. — P. 14–20.ссылка
Hemminki K., Granström C. Familial invasive and borderline ovarian tumors by proband status, age and histology // Int J Cancer. — 2003. — № 5. — P. 701–705.ссылка
Zheng G., Yu H., Kanerva A. et al. Borderline Ovarian Tumors Share Familial Risks with Themselves and Invasive Cancers // Cancer Epidemiol Biomarkers Prev. — 2018. — № 11. — P. 1358–1363.ссылка
Ovarian Borderline Tumors Treatment (PDQ®) // PDQ Cancer Information Summaries. — 2025. ссылка
Coumbos A., Sehouli J., Chekerov R. et al. Clinical management of borderline tumours of the ovary: results of a multicentre survey of 323 clinics in Germany // Br J Cancer. — 2009. — № 11. — P. 1731–1738. ссылка
Vasconcelos I., Olschewski J., Braicu I., Sehouli J. A meta-analysis on the impact of platinum-based adjuvant treatment on the outcome of borderline ovarian tumors with invasive implants // Oncologist. — 2015. — № 2. — P. 151–158.ссылка
Ciolina M., Baldassari P., Iannitti M., Pichi A., Iafrate F., Laghi A. Imaging of Peritoneal Carcinomatosis with MDCT: spectrum of diagnostic patterns, sites involved and proposal for a new detailed reporting scheme // European Congress of Radiology ECR 2012. — 2012.
Bhutiaa K., Mathurb M., Aggarwalc I. Micropapillary Serous Borderline Ovarian Tumor in Early Pregnancy: Is Conservative Surgery Still a Viable Option? // J Med Cases. — 2016. — № 9. — Р. 406–410.
Li X., Liu G., Wu W. Progress in Biological Research and Treatment of Pseudomyxoma Peritonei // Cancers (Basel). — 2024. — № 7. — Р. 1406.

