Определение болезни. Причины заболевания
Открытый артериальный проток (ОАП; Patent ductus arteriosus) — это врождённый порок сердца, при котором проток между дугой аорты и лёгочной артерией остаётся открытым, что приводит к «нетипичной» циркуляции крови по магистральным (наиболее крупным) сосудам [1]. Такую патологию также называют открытым Боталловым протоком. В норме он закрывается сразу после рождения.
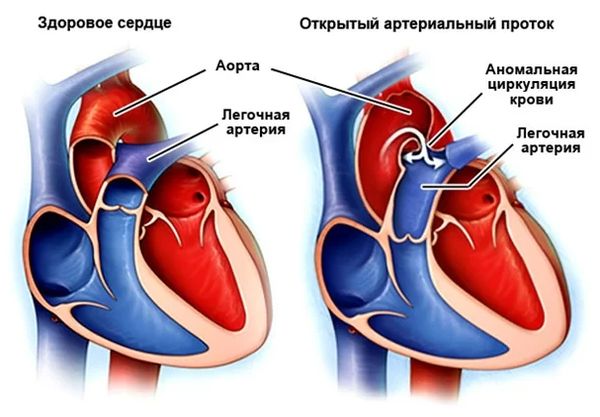
Открытый артериальный проток
В трети случаев ОАП спонтанно самостоятельно закрывается даже у детей с крайне низкой массой тела при рождении.
Распространённость открытого артериального протока
Оценить распространённость патологии сложно, так как в России нет единого учёта этой болезни [2]. Кроме того, у научного сообщество до сих пор нет определённости, с какого момента считать ОАП отклонением от нормы (в среднем, артериальный проток должен закрыться в течение 7–14 дней жизни новорождённого). Чаще всего ОАП диагностируют у недоношенных детей, гораздо реже — у младенцев, рождённых в срок.
В соответствии с этими критериями частота изолированного ОАП составляет 0,14–0,3 на 1000 живорождённых детей. На долю открытого артериального протока приходится 7 % всех врождённых пороков сердца (ВПС) и 3 % критических ВПС [3].
Согласно исследованиям, гемодинамически значимый ОАП (ГЗОАП), т. е. вызывающий серьёзные нарушения кровообращения, чаще развивается у недоношенных детей: он встречается у 10–20 % новорождённых с массой тела 1000–1500 г и у 25–70 % младенцев, которые при рождении весят менее 1000 г [4].
В некоторых случаях ОАП является частью сочетанного порока (в 5–12 % наблюдений) [8].
Причины развития открытого артериального протока
К основным причинам относят:
- генетические патологии (хромосомные аномалии) — случайные мутации;
- инфекционные заболевания беременной (например, синдром врождённой краснухи);
- аутоиммунные патологии у матери во время беременности (особенно в 1-м триместре);
- преждевременные роды и недоношенность;
- наследственность (семейный анамнез) — наличие ОАП и других ВПС у братьев, сестёр, родителей, бабушек или дедушек.
Также ОАП может быть идиопатическим (развиться без видимой причины).
Среди факторов риска также выделяют аллергию у матери, негативное воздействие радиоактивного излучения, токсических, химических, физических и других факторов на беременную, осложнённый акушерско-гинекологический анамнез (например, самопроизвольные аборты или замершие беременности).
Симптомы открытого артериального протока
Проявления ОАП зависят от величины протока, давления в лёгочном стволе, сопротивления сосудов малого и большого кругов кровообращения, а также его соотношения.
При небольшом дефекте ОАП может протекать бессимптомно, и его можно заподозрить только при обследовании (например, при помощи стетофонендоскопа определяется постоянный шум, особенно в области 2–3-го межреберья слева от грудины).
В остальных случаях могут появиться трудности с кормлением (например, младенец плохо сосёт грудь, отказывается от еды, быстро утомляется), у ребёнка также наблюдается одышка, отставание в весе и росте, он подвержен частым бронхолёгочным заболеваниям. Симптомы обычно появляются с конца первого года и длятся один-два года.
При большом диаметре ОАП патология даёт о себе знать с самого рождения или в первые недели жизни [8]. У таких детей наблюдаются признаки сердечной недостаточности в виде задержки развития, плохого аппетита, учащённого сердцебиения (тахикардии) и дыхания (тахипноэ), а также одышки при кормлении.
У недоношенных детей признаки сердечной недостаточности появляются раньше, чем у доношенных [11].
Патогенез открытого артериального протока
До рождения во время внутриутробного развития сердечно-сосудистая система плода работает без участия лёгких: они раскрываются только после рождения. Газообмен, при котором кислород насыщает кровь плода, происходит в плаценте: поток крови обходит лёгкие и поступает в левые отделы сердца из правых и обратно. В сердце плода для этого существуют два отверстия: овальное окно в межпредсердной перегородке, разделяющей правое и левое предсердие, и артериальный проток, который находится между аортой и лёгочной артерией [4].
В норме артериальный проток закрывается в течение 24–48 часов после рождения. После того как ребёнок делает первый вдох, лёгкие расправляются, и из их тканей выделяется специфическое вещество — брадикинин, вследствие чего происходит заращение артериального протока. На этот процесс также влияет воздействие кислорода. Однако проток может оставаться открытым из-за влияния других веществ, например простагландинов, поступивших из кровотока матери.
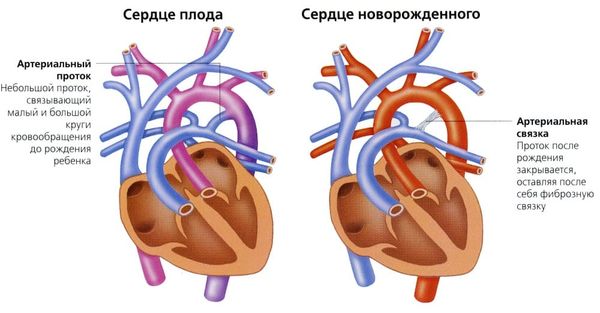
Сердце плода и новорождённого в норме
У глубоко недоношенных детей проток может не закрыться из-за значительной незрелости органов и тканей плода, зачастую протекающей на фоне внутриутробной инфекции [4].
Если у ребёнка сохраняется ОАП, артериальная кровь постоянно сбрасывается в лёгочную артерию и далее в малый круг кровообращения, после чего смешивается с венозной кровью в лёгких. Это приводит к гиперволемии (избытку крови) малого круга кровообращения и гипоксии, что в дальнейшем выражается в необратимых изменениях сосудов лёгких с последующим развитием лёгочной гипертензии. Для поддержания нормального кровообращения левым отделам сердца, особенно желудочку, приходится работать интенсивнее, что ведёт к их увеличению. При прогрессировании симптомов и увеличении нагрузки на правые отделы, связанные с повышением сопротивления сосудов малого круга, также увеличивается правый желудочек, а миокард с его стороны истончается.
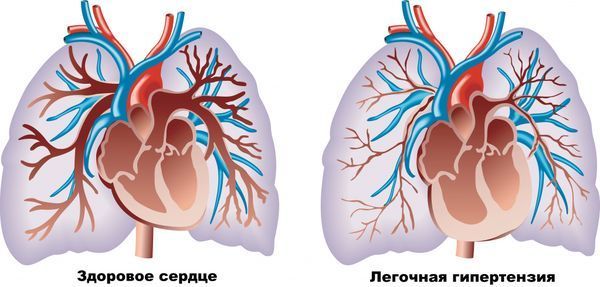
Лёгочная гипертензия
Степень нарушения кровообращения зависит от диаметра ОАП и объёма проходящей через него крови. Общепринятыми характеристиками ГЗОАП являются:
- диаметр ОАП более 1,5 мм у новорождённых с массой тела ниже 1500 г или более 1,4 мм при массе тела больше 1500 г;
- сброс крови по ОАП слева направо;
- обратный (ретроградный) кровоток в нисходящей аорте, который составляет более 50 % от обычного кровотока [5].
Классификация и стадии развития открытого артериального протока
В Международной классификации болезней 10-го пересмотра (МКБ-10) открытый артериальный проток входит в группу «Врождённые аномалии крупных артерий (Q25)» и имеет собственный шифр: Q25.0.
Он отличается:
- по форме протока — воронкообразный, цилиндрический, окончатый;
- типу клинического течения — осложнённый и неосложнённый;
- наличию сопутствующих ВПС — изолированный и сочетанный [2].
В соответствии с российскими клиническими рекомендациями, степень тяжести порока определяют на основании систолического давления в лёгочной артерии (СДЛА):
- 1 степень — СДЛА составляет не более 40 % от системного (общего) артериального давления;
- 2 степень — СДЛА находится в диапазоне 40–75 % от артериального (умеренная лёгочная гипертензия);
- 3 степень — СДЛА составляет более 75 % от артериального (выраженная лёгочная гипертензия с сохранением сброса крови слева направо);
- 4 степень — СДЛА равно артериальному или превышает его (тяжёлая степень лёгочной гипертензии с появлением сброса крови справа налево) [1][3].
Как правило, систолическое давление в лёгких значительно ниже, чем в остальном организме, т. е. в большом круге кровообращения. Поэтому чем больше оно становится, тем выше степень тяжести ОАП и ярче картина лёгочной гипертензии. При первой степени тяжести симптомов нет. СДЛА оценивают с помощью ЭхоКГ.
У ГЗОАП, т. е. при большом дефекте, выделяют 3 стадии:
- 1 стадия — первичная адаптация к ОАП (первые 2–3 года жизни ребёнка). Этот период характеризуется появлением первых симптомов и сопровождается развитием тяжёлых, иногда критических состояний. В некоторых случаях, если хирургическая помощь не была оказана своевременно, тяжёлое течение ГЗОАП заканчивается летальным исходом.
- 2 стадия — относительная компенсация ОАП (от 2–3 лет до 20 лет). В этот период у пациента практически нет никаких симптомов, так как организм приспосабливается к пороку, однако это не говорит о выздоровлении. У ребёнка медленно и длительно прогрессирует гиперволемия малого круга кровообращения. Постепенно формируется стеноз митрального клапана, который находится между левым предсердием и желудочком, растёт СДЛА и увеличивается перегрузка правого желудочка.
- 3 стадия — склеродегенеративные трансформации лёгочных сосудов. На этой стадии клинические проявления ОАП постепенно начинают уступать симптомам лёгочной гипертензии, которые затем начинают преобладать [3].
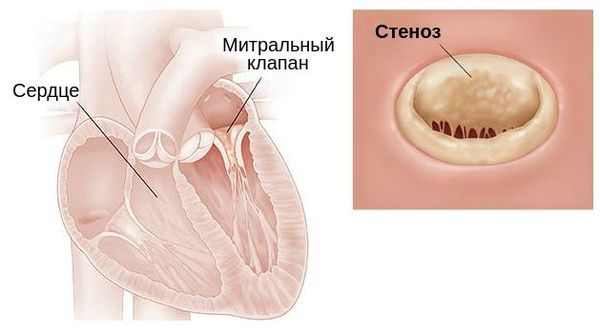
Стеноз митрального клапана
Осложнения открытого артериального протока
Значимый ОАП оказывает влияние на циркуляцию крови в лёгких и других органах, что может привести к развитию разных осложнений.
Наиболее тяжёлые жизнеугрожающие ситуации появляются у недоношенных детей с очень низкой (1000–1500 г) и экстремально низкой массой тела (до 1000 г) при рождении. Около трети младенцев с ГЗОАП, родившихся раньше срока (до 30-ти недель гестации), нуждаются в стимуляции закрытия артериального протока медикаментами или хирургически [6].
Все осложнения можно разделить на 2 обширные группы:
- осложнения, связанные с повышенным кровенаполнением лёгких;
- осложнения, связанные со снижением кровообращения в органах (почках, кишечнике, мозге) [7].
К первой группе осложнений относят:
- Лёгочное кровотечение — ребёнок становится бледным, ему тяжело дышать носом, отмечаются кровянистые выделения из носа и рта, снижается эластичность кожи и тонус мышц, появляется артериальная гипотония (но иногда она также может быть следствием снижения поступления крови по большому кругу кровообращения) [5].
- Усугубление респираторного дистресс-синдрома — обширного воспаления лёгких, которое сопровождается дыхательной недостаточностью. При ГЗОАП к лёгким поступает слишком много крови, которая должна была идти в большой круг кровообращения, что в дальнейшем приводит к интерстициальному отёку лёгких. В течение 1–3 суток после рождения этот эффект сглаживается за счёт оттока лимфы. Однако, если артериальный проток остаётся открытым более 24–72 часов, постепенно ухудшается газообмен и возникают более серьёзные нарушения в работе лёгких [7].
К осложнениям второй группы относят кровоизлияния в желудочки мозга и некротизирующий энтероколит [5]. У новорождённых с большим ОАП наблюдается выраженная турбулентность мозгового кровотока (изменения скорости, направления и плотности потока крови по мозговым сосудам) и снижение скорости кровотока в целом. Именно в результате этих отклонений происходят внутрижелудочковые кровоизлияния и гипоксические изменения в виде ишемии головного мозга [7].
Помимо расширения левых полостей сердца и формирования лёгочной гипертензии, одним из возможных коварных осложнений ОАП является боталлит [9]. Это разновидность эндартериита (воспаления внутренней стенки артерии), которая развивается в стенке протока. Боталлит может протекать вяло, создавая предпосылки для формирования эмболов. Из-за изменений в тканях риск разрыва истончённой стенки с развитием фатального кровотечения сохраняется даже после хирургического лечения.
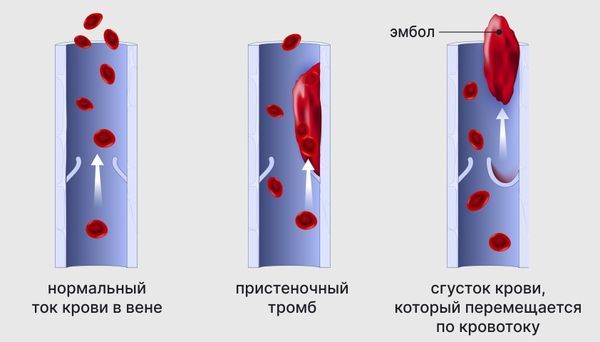
Эмбол
По срокам возникновения все осложнения ГЗОАП у новорождённых можно разделить на 2 группы:
- ранние (определяются в первые 7 суток после рождения) — усугубляется течение и степень тяжести респираторного дистресс-синдрома, развиваются внутрижелудочковые кровоизлияния, появляются признаки лёгочного кровотечения, пища плохо усваивается, что проявляется в малой прибавке в весе, снижается артериальное давление и диурез, возникают эпизоды апноэ, отмечаются неустойчивые показатели сатурации (насыщения крови кислородом), метаболические нарушения в анализах крови (смещение кислотно-щелочного баланса организма в сторону увеличения кислотности) и постоянный систолодиастолический шум в сердце;
- поздние (с 8 суток и далее) — появляются признаки недостаточности кровообращения, повышается риск формирования бронхолёгочной дисплазии, ретинопатии недоношенных и перинатального органического поражения центральной нервной системы [4].
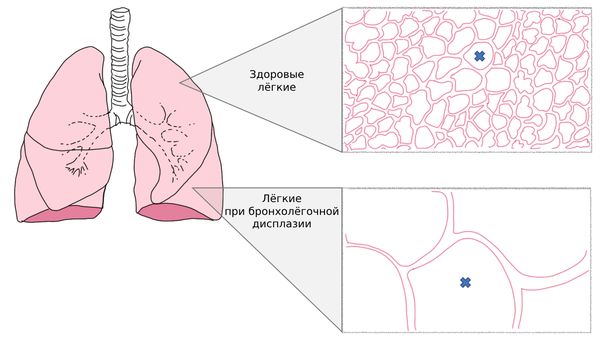
Бронхолёгочная дисплазия
К крайне редким серьёзным осложнениям относится аневризма Боталлова протока и её разрыв (встречается в 1–8 % случаев от всех ОАП). Она формируется из-за повышенного давления крови на ткани протока, что приводит к локальному истончению и ограниченному выпячиванию его стенки. При скачках артериального давления аневризма может разорваться, что вызывает жизнеугрожающее кровотечение.
Диагностика открытого артериального протока
К обязательным диагностическим мероприятиям при наличии подозрений на ОАП у ребёнка входит оценка клинической картины, сбор анамнеза (истории жизни и болезни), данные субъективного и объективного осмотра, а также инструментальные методы диагностики. Поставить диагноз можно только после ЭхоКГ, поскольку именно это исследование позволяет оценить все необходимые параметры кровотока. Остальные обследования позволяют лишь заподозрить ОАП [2][11]. Специфической лабораторной диагностики нет.
Физикальный осмотр и опрос
Во время приёма врач уточняет у родителей, есть ли у ребёнка генетические или наследственные факторы риска, болела ли чем-то мать во время беременности, отмечала аллергию, подвергалась ли токсическому или радиоактивному воздействию. Также большое значение имеет осложнённый акушерско-гинекологический анамнез (самопроизвольные, медикаментозные и осложнённые аборты, замершие беременности), возраст беременной (слишком молодой или поздний), значительная разница в возрасте родителей и близкородственные браки [8].
При физикальном исследовании обычно определяют:
- учащение частоты сердечных сокращений и пульса;
- видимую задержку в скорости роста и развития ребёнка по сравнению с детьми его возраста;
- увеличение размеров камер сердца по данным перкуссии (простукивания);
- длительный «машинный», т. е. громкий и шумный звук, при прослушивании грудной клетки (особенно во 2-м и 3-м межреберье);
- снижение нижнего артериального давления вплоть до нуля [3].
У большинства детей с признаками недоношенности и ГЗОАП наблюдается частый сильный пульс и выраженная пульсация в околосердечной области, а в области лёгочного ствола и клапана лёгочной артерии выслушиваются непрерывные шумы. Однако не во всех случаях у новорождённых есть слышимые шумы в сердце.
Инструментальная диагностика
Основным методом диагностики является ультразвуковое исследование сердца с допплерографией — ЭхоКГ [9][10]. За счёт цветного допплеровского картирования она позволяет получить необходимые данные о ГЗОАП при оценке:
- размера ОАП (принято сопоставлять с размером левой лёгочной артерии);
- величине скорости потока крови в ОАП;
- СДЛА и косвенных признаков лёгочной гипертензии;
- дилатации (увеличения) полостей левых отделов сердца;
- наличия обратного тока крови по нисходящей аорте и нормального тока в левой лёгочной артерии в диастолу (когда сердце расслаблено).
Доказано, что ЭхоКГ имеет более высокую чувствительность в диагностике по сравнению с клиническими данными (симптомы появляются в среднем на 4-е сутки от момента рождения). Для формирования наиболее полной картины и наилучшей визуализации ОАП используют 2 основных доступа: парастернальный (окологрудинный) и супрастернальный (из-под грудины).
При небольшом размере ОАП показатели ЭКГ и рентгенографии органов грудной клетки длительное время будут оставаться в норме. В случае большого шунта и ГЗОАП рентгенограмма покажет увеличение левого предсердия, желудочка и аорты в её восходящем отделе, а также усиление сосудистого рисунка лёгких. По данным ЭКГ будут определяться признаки увеличения левого желудочка.
Дифференциальная диагностика
ОАП нужно отличать от таких труднодиагностируемых патологий, как дефект аортолёгочной перегородки, общий артериальный ствол, крупные аортолёгочные коллатеральные артерии, коронаролёгочные фистулы, разрыв синуса Вальсальвы и дефект межжелудочковой перегородки с аортальной недостаточностью. Их также распознают с помощью ЭхоКГ [2].
Лечение открытого артериального протока
Лечение разделяется на консервативное и оперативное. Выбор терапии зависит от срока рождения малыша и степени тяжести ОАП. В некоторых случая ОАП закрывается самостоятельно, и лечение не требуется, в других случаях даже при бессимптомном течении и малых размерах протока (1–3 мм) необходима операция [11].
Консервативное лечение
Всем недоношенным детям с ОАП в первые дни после рождения назначают нестероидные противовоспалительные препараты (НПВП): Индометацин или Ибупрофен, которые подавляют выработку простагландинов. Приём НПВП, начатый вовремя, в большинстве случаев ведёт к уменьшению и даже самостоятельному закрытию ОАП.
Диуретики показаны в том случае, если ОАП сопровождается признаками недостаточности кровообращения. При наличии инфекционного эндокардита (воспаления во внутреннем слое сердца) во всех случаях требуется курс антибиотикотерапии в соответствующих возрастных дозировках [3][5].
Указанное лечение показано только недоношенным детям.
К медикаментозному лечению можно также отнести назначение Дигоксина [11]. Его применяют при длительном функционировании ГЗОАП и наличии хронической (застойной) сердечной недостаточности.
Хирургическое лечение
Наиболее оптимальный возраст для проведения операции — от 2 до 5 лет. Однако в случае осложнённого течения ОАП и развития декомпенсации оперативное вмешательство могут провести в любом возрасте [3]. При бессимптомном течении операцию откладывают до достижения ребёнком минимум одного года, поскольку за это время ОАП может закрыться самостоятельно [11].
Считается, что в возрасте старше 5 лет после устранения ОАП во время операции сохраняется остаточная лёгочная гипертензия из-за необратимых изменений в лёгких, поэтому хирургическое лечение лучше проводить до 5 лет.
В арсенале кардиохирургов есть несколько методик устранения ОАП: перевязка двойной лигатурой, клипирование, эндоваскулярная окклюзия и пересечение ОАП с последующим прошиванием и перевязкой обеих культей. Тактика выбора хирургического лечения зависит от вида ОАП, его размеров, СДЛА, вида сброса и тяжести осложнений.
Летальность во время и после любой из этих операций отсутствует, но иногда встречаются некоторые осложнения, связанные с повреждением гортанного или диафрагмального нервов или внутригрудного лимфатического протока в ходе операции. Такие последствия обычно обратимы [3]. К редким осложнениям, которые могут возникнуть при чрескожном закрытии ОАП, относят:
- эмболизацию сосуда (чаще всего ветви лёгочной артерии) — появляется из-за смещения импланта;
- отсутствие пульса на сосуде (преимущественно у детей младшего возраста).
Эти осложнения устраняют сразу же во время операции.
Чаще всего используют эндоваскулярную окклюзию, в ходе которой просвет протока механически закрывают специальными спиралями и окклюдерами. Технически метод практически не приводит к осложнениям. Маленькие дети проходят процедуру под наркозом, а подростки и взрослые — под местной анестезией. Доступ осуществляется с помощью пункции по бедренной артерии. Эффективность такого вмешательства составляет около 100 %, однако в единичных случаях наблюдается повторное открытие артериального протока. Хирурги устраняют рецидив таким же образом, как и в первый раз.
Ранний детский возраст (1–3 года) и выраженный дефицит массы тела ребёнка являются противопоказаниями для эндоваскулярного закрытия ОАП.
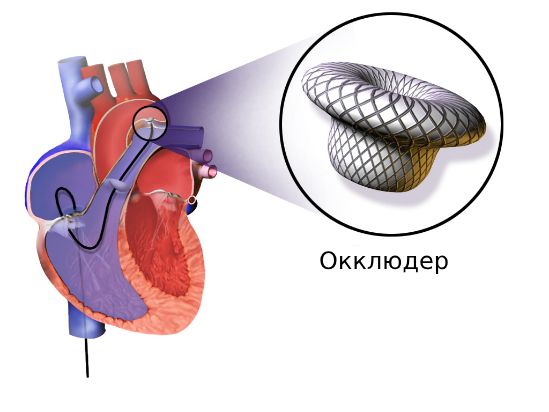
Эндоваскулярная окклюзия
Прогноз. Профилактика
Прогноз определяется степенью тяжести состояния пациента. Своевременная операция позволяет достичь полного выздоровления. Если у пациента развилась выраженная лёгочная гипертензия, конечный результат зависит от того, развились ли необратимые структурные и функциональные изменения в миокарде и в лёгочных сосудах.
При неоперированном и не закрывшемся ОАП средняя продолжительность жизни может составлять около 40 лет [3].
Если ОАП осложняется сердечной недостаточностью, бактериальным эндокардитом в виде эндартериита, в том числе боталлита, формированием и разрывом аневризмы Боталлова протока, возможен летальный исход. Его вероятность составляет: до 20 % у пациентов до 30 лет, 42 % до 45 лет и 60 % до 60 лет [3].
Профилактика ОАП
Чтобы снизить риск ОАП, необходимо придерживаться общих рекомендаций, направленных на уменьшение вероятности формирования всех врождённых пороков: обеспечить нормальные условий протекания беременности, вести здоровый образ жизни, вовремя лечить другие болезни и т. д.
Список литературы
Кужель Д. А., Матюшин Г. В., Шульман В. А., Гусева Т. А., Савченко Е. А. «Немой» открытый артериальный проток // Красноярская государственная медицинская академия. — 2008. — С. 1–5
Артюх Л. Ю., Карелина Н. Р., Оппедизано М. Д. Л., Гафиатулин М. Р. и др. Современный взгляд на классификацию и диагностику открытого артериального протока (обзор) // Российские биомедицинские исследования. — 2023. — № 2. — С. 78–91.
Ассоциация сердечно-сосудистых хирургов России. Открытый артериальный проток: клинические рекомендации. — М., 2018. — 22 с.
Гемодинамически значимый функционирующий артериальный проток (ГЗФАП) у глубоконедоношенных детей // ФГБУ НМИЦ АГП им. В. И. Кулакова Минздрава России. [Электронный ресурс]. Дата обращения: 17.07.2024.
Бокерия Е. Л., Дегтярева Е. А. Открытый артериальный проток — «Добро и зло в одном сосуде» (обзор литературы) // Вестник РУДН. — 2017. — № 2. — С. 163–170.
Спивак Е. М., Николаева Т. Н., Климачев А. М. Особенности клинических проявлений открытого артериального протока у глубоконедоношенных новорождённых детей // Российский вестник перинатологии и педиатрии. — 2016. — № 1. — С. 51–55.
Крючко Д. С., Антонов А. Г., Ленюшкина А. А., Ионов О. В., Балашова Е. Н. Современные представления об открытом артериальном протоке у новорождённых // Педиатрия. Журнал им. Г. Н. Сперанского. — 2011. — № 1. — С. 130–136.
Калашникова Е. А., Никитина Н. А. Открытый артериальный проток: особенности ранней неонатальной, постнатальной диагностики, клинической манифестации, лечение и прогноз // Здоровье ребёнка. — 2017. — № 2. — С. 171–176.
Прийма Н. Ф., Попов В. В., Иванов Д. О. Эхокардиографическое исследование в дифференциальной диагностике открытого артериального протока у детей // Педиатр. — 2016. — № 4. — С. 119–127.
Сингх Й., Фрайсс А., Эрдеве О., Атасай Б. Эхокардиографическая диагностика и гемодинамическая оценка открытого артериального протока у новорождённых с экстремально низким гестационным возрастом // Неонатология: Новости. Мнения. Обучение. — 2021. — № 1. — С. 64–75.
Beerman L. B. Patent Ductus Arteriosus (PDA) // MSD Manuals. — 2023.

