Определение болезни. Причины заболевания
Синдром Альпорта (Alport syndrome) — это наследственное заболевание, при котором нарушается развитие почечной ткани, из-за чего у пациента возникает прогрессирующая почечная недостаточность, а в моче появляется кровь и белок (протеинурия). Помимо почек, болезнь также поражает органы слуха и зрения: синдром Альпорта часто сочетается с нейросенсорной тугоухостью и глазными заболеваниями (изменением формы хрусталика, катарактой, нистагмом и т. д.).
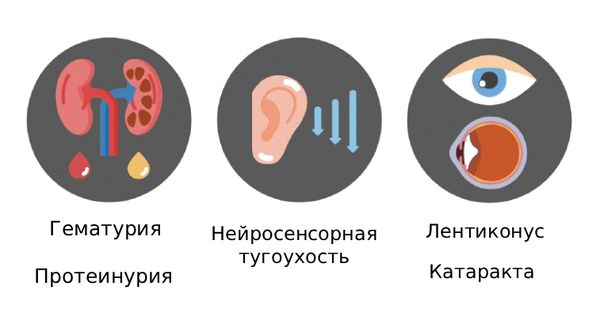
Основные проявления синдрома Альпорта
Впервые эту болезнь описал английский врач Артур Альпорт в 1927 году. Он лечил семью, в которой родственники страдали от проблем с почками и снижения слуха. При этом мужчины заболевали в более молодом возрасте по сравнению с женщинами.
Распространённость синдрома Альпорта
В США синдром Альпорта находят у 2 % детей с хронической почечной недостаточностью [3]. По другим данным, болезнь диагностируют у одного ребёнка из 5–10 тыс. населения. В России она встречается реже: на 100 тыс. детей приходится примерно 17 пациентов с таким синдромом [1].
Синдром Альпорта обычно выявляют в детском или юношеском возрасте. У мальчиков часто находят протеинурию, которая прогрессирует с возрастом, однако у девочек такой симптом встречается реже. Проявление тугоухости отмечается у 90 % мальчиков и у 10 % девочек с синдромом Альпорта [2]. При этом прогноз болезни зависит от вида генетической мутации, а не пола пациента.
Болезнь почек сочетается с нейросенсорной тугоухостью в 30–50 % случаев, с заболеваниями органа зрения — в 15–30 %. Чаще всего пациентов беспокоит истончение роговицы и развитие её конической деформации — кератоконуса [1].
Причины синдрома Альпорта
Синдром Альпорта возникает в результате генетических мутаций, которые влияют на синтез коллагена 4-го типа. Именно он является основным структурным компонентом базальной мембраны хрусталика, роговицы глаза, внутреннего уха и почечных клубочков.
Мутация может произойти в гене COL4A5, COL4A4 или COL4A3.
Выделяют 3 типа наследования:
- Доминантный Х-сцепленный тип — в этом случае изменения появляются в гене COL4A5, который расположен на половой Х-хромосоме. Для проявления болезни достаточно получить всего одну копию дефектного гена, поэтому синдром возникает у людей обоих полов.
- Аутосомно-рецессивный тип — при такой форме мутируют гены COL4A4 и COL4A3, однако они находятся на одной из 44 неполовых хромосом. При аутосомно-рецессивном типе оба родителя здоровы, но каждый из них является носителем мутантной копии гена, которую они передают ребёнку, поэтому риск заболевания одинаков как у мальчиков, так и у девочек.
- Аутосомно-доминантный тип — мутантный ген COL4A3 или COL4A4 передаётся только от одного из родителей, однако такие случаи заболевания встречаются редко [14].
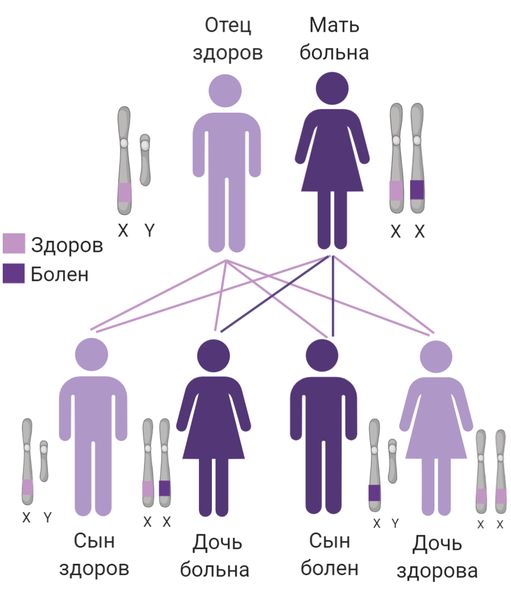
Х-сцепленный тип наследования
В большинстве случаев мутация происходит в гене COL4A5 на Х-хромосоме, поэтому мальчики болеют чаще и тяжелее девочек. Поскольку мутация доминантная, для проявления заболевания достаточно одной мутантной копии гена.
Симптомы синдрома Альпорта
Почечные симптомы:
- Микрогематурия (наличие крови в моче) — почти у всех пациентов с синдромом Альпорта она остаётся незаметной для глаз, но при лабораторных анализах в моче обнаруживают повышенный уровень эритроцитов [2]. Макрогематурия, когда моча приобретает розовый или светло-коричневый оттенок, возникает в редких случаях после перенесённой респираторной инфекции или физического перенапряжения. Такие эпизоды также могут сопровождаться болью в животе [1].
- Протеинурия (повышенный уровень белка в моче) — чаще встречается у мальчиков и прогрессирует с возрастом. При протеинурии моча становится пенистой, при этом увеличивается объём мочеиспускания.
- Артериальная гипертензия — периодическое или стойкое повышение артериального давления, которое развивается на поздних стадиях синдрома Альпорта [1]. Может сопровождаться головной болью, шумом в ушах, головокружением, тошнотой, ощущением тяжести в голове и мельканием «мушек» перед глазами.

Микро- и макрогематурия
При прогрессировании патологического процесса и необратимом снижении скорости клубочковой фильтрации развивается хроническая болезнь почек (ХБП) — основное проявление синдрома. Сначала она никак себя не проявляет, поэтому часто её обнаруживают случайно при лабораторной диагностике (у такого пациента повышается уровень креатинина и мочевины в крови). У мальчиков ХБП протекает тяжелее и может достигнуть терминальной (конечной) стадии в довольно молодом возрасте: к 40 годам её диагностируют у 90 % мужчин с синдромом Альпорта [16]. Хроническая болезнь почек обычно сопровождается отёчностью лица, рук и ног, частым ночным мочеиспусканием (никтурией), слабостью и болью в пояснице.
Внепочечные проявления:
- Нейросенсорная тугоухость — постепенное снижение слуха (вплоть до полной его потери), вызванное поражением слухового анализатора. Выявляют в 30–50 % случаев синдрома Альпорта [1].
- Патология зрения — чаще всего развивается передний лентиконус (конусовидное или шаровидное выпячивание хрусталика), кератоконус, миопия или катаракта. Они сопровождаются снижением остроты и чёткости зрения, ухудшением цветоощущения и контрастной чувствительности, искажением изображения, светобоязнью и т. д. Подобные проблемы наблюдаются у 15–30 % пациентов [1].
![Лентиконус [17] Лентиконус [17]](/media/bolezny/sindroma-alporta/lentikonus-17_s.jpeg?dummy=1763557561005)
Лентиконус [17]
Интересно, что проявление симптомов часто зависит от генотипа [11]. Например, при Х-сцепленном типе у мужчин чаще возникает гематурия и раннее развитие хронической почечной недостаточности, а у женщин болезнь может никак себя не проявлять. При аутосомно-доминантном типе у пациентов также может не быть симптомов, в то время как аутосомно-рецессивный тип приводит к тяжёлому течению болезни как у мужчин, так и у женщин [12].
Патогенез синдрома Альпорта
Гены COL4A5, COL4A4 и COL4A3 кодируют альфа-цепи коллагена 4-го типа, который является структурным компонентом базальной мембраны почечных клубочков, хрусталика глаза и внутреннего уха. В случае мутации одного из этих генов альфа-цепи формируются неправильно, что и приводит к развитию синдрома Альпорта [5].
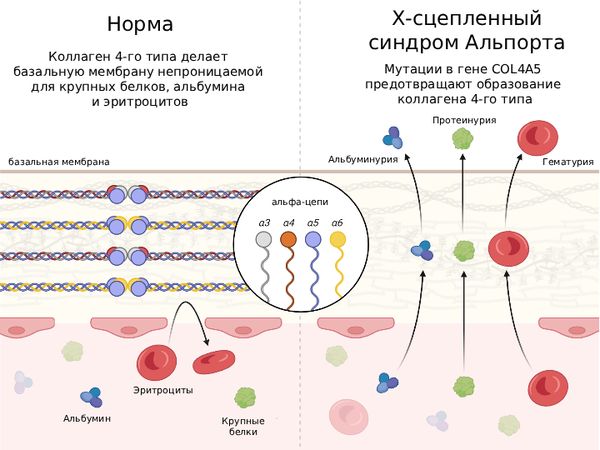
Патогенез синдрома Альпорта
В 85 % случаев у пациентов выявляют дефект в гене COL4A5 в локусе Xq22. Этот тип наследования связан с Х-хромосомой и зачастую поражает мужчин. У остальных 15 % пациентов происходят мутации в генах COL4A4 и COL4A3 в локусе 2q36 [14].
Патологический процесс начинается с истончения базальной мембраны. Чем сильнее она расщепляется и расслаивается, тем ярче становятся симптомы. На поздних стадиях болезни базальная мембрана разрушается, из-за чего почки больше не могут фильтровать кровь. Таким образом развивается хроническая болезнь почек.
Классификация и стадии развития синдрома Альпорта
Общепринятой классификации синдрома Альпорта не существует, однако в литературе есть классификация наследственного нефрита (воспаления почек), связанного с этой болезнью:
- тип 1 — доминантно наследуемый ювенильный тип нефрита (т. е. диагностируемый до 31 года) с потерей слуха;
- тип 2 — ювенильный тип нефрита с потерей слуха и доминантным, сцепленным с Х-хромосомой наследованием;
- тип 3 — «взрослый» тип нефрита с потерей слуха и доминантным, сцепленным с Х-хромосомой наследованием;
- тип 4 — «взрослый» тип нефрита с доминантным, сцепленным с Х-хромосомой наследованием без выраженных изменений слуха;
- тип 5 — аутосомно-доминантный нефрит с нарушениями слуха и тромбоцитопатией (синдром Эпштейна) [1].
Клинические стадии гломерулопатии (поражения почечных клубочков) при синдроме Альпорта:
- 0 стадия — микрогематурия, уровень креатинина и белка в моче — менее 30 мг/г;
- I стадия — альбуминурия, уровень креатинина и белка (альбумина) в моче — 30–300 мг/г;
- II стадия — протеинурия, уровень креатинина и белка (альбумина) в моче — более 300 мг/г;
- III стадия — скорость клубочковой фильтрации ниже 60 мл/мин/1,73 м²;
- IV стадия — терминальная почечная недостаточность [4].
Осложнения синдрома Альпорта
Основные осложнения:
- Преэклампсия — серьёзное осложнение, которое возникает после 20-й недели беременности и может привести к преждевременным родам. У беременных пациенток синдром Альпорта протекает быстрее, из-за чего стремительно снижается работоспособность почек. Это вызывает различные осложнения, например повышенное артериальное давление и протеинурию [6].
- Тромбоцитопения — снижение уровня тромбоцитов в крови ниже 150 тыс. Ед/мкл, вызванное генетической мутацией [7]. Тромбоцитопения сопровождается повышенной кровоточивостью при повреждении тканей и частым образованием гематом.
- Лейомиоматоз — редкое заболевание, при котором происходит разрастание гладкомышечных клеток. Мутации в генах также могут содействовать формированию доброкачественных опухолей (лейомиоматозов) [8]. При синдроме Альпорта обычно выявляют лейомиоматоз пищевода, трахеи и бронхов. Кроме того, у женщин может развиться лейомиоматоз половых органов [9].
- Интерстициальный фиброз почек — это процесс, при котором нормальная ткань почек замещается соединительной (фиброзной). Симптомы при этом состоянии очень схожи с развитием хронической болезни почек.
- Гломерулосклероз — рубцевание почечных клубочков [3]. Он развивается на поздних стадиях ХБП из-за хронического воспаления, вызванного повреждением базальной мембраны почки.
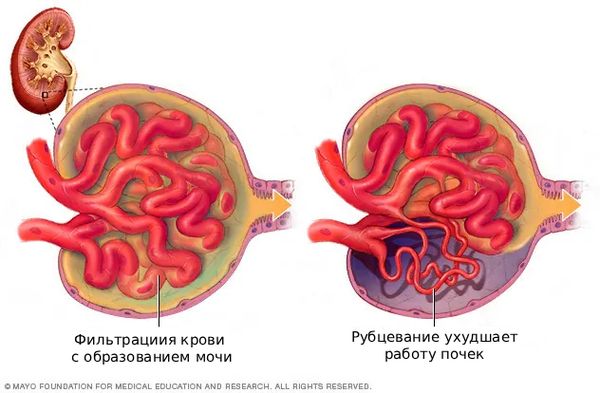
Гломерулосклероз
Диагностика синдрома Альпорта
При подозрении на синдром Альпорта необходимо обратиться к нефрологу. Чтобы поставить правильный диагноз, врач обязательно собирает анамнез (историю болезни и жизни) пациента, проводит осмотр и оценивает результаты лабораторных и инструментальных исследований.
При сборе анамнеза специалист уточняет, были ли в семье случаи врождённых патологий зрения или слуха, бессимптомной протеинурии и гематурии, которые выявляли у родственников после анализов, а также смерти от почечной недостаточности [2].
Пренатальная диагностика
Генетический скрининг на наличие синдрома Альпорта до рождения не делают из-за большой вариативности генетических мутаций, которые могут вызвать это заболевание. Однако, если у кого-то из членов семьи есть схожие симптомы или подтверждён синдром Альпорта, будущие родители проходят генетическое консультирование, чтобы оценить риск заболевания у ребёнка. Генетическое консультирование проводит врач-генетик. Сначала он также собирает анамнез, а при необходимости проводит ДНК-тестирование на мутации в генах COL4A3, COL4A4 или COL4A5 [3].
Существует несколько методов молекулярно-генетического анализа:
- секвенирование — у пациента берут кровь и выделяют из неё ДНК, чтобы определить последовательность её нуклеотидов (проводят чаще других);
- анализ делеций — помогает определить тип наследования: Х-сцепленный, аутосомно-рецессивный или аутосомно-доминантный;
- полимеразная цепная реакция (ПЦР) — используют для анализа ДНК плода, в этом случае проводят биопсию ворсин хориона [10].
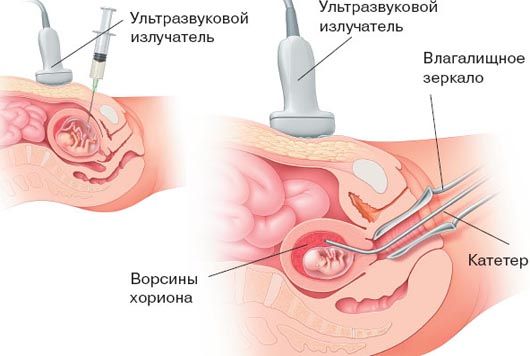
Биопсия ворсин хориона (трансабдоминальная и трансцервикальная)
Хотя молекулярно-генетическое исследование генов не обязательно для диагностики заболевания, оно помогает точно и быстро поставить диагноз.
Диагностика взрослых пациентов
Для постановки диагноза после рождения проводят биопсию — забор тканей органа посредством чрескожного доступа. Далее эти ткани передают на гистологическое исследование. На ранних стадиях заболевания оно выявит истончение базальной мембраны почек с расщеплением и расслоением, из-за чего структура мембраны будет напоминать пчелиные соты [2]. На поздних стадиях базальная мембрана начинает разрушаться.
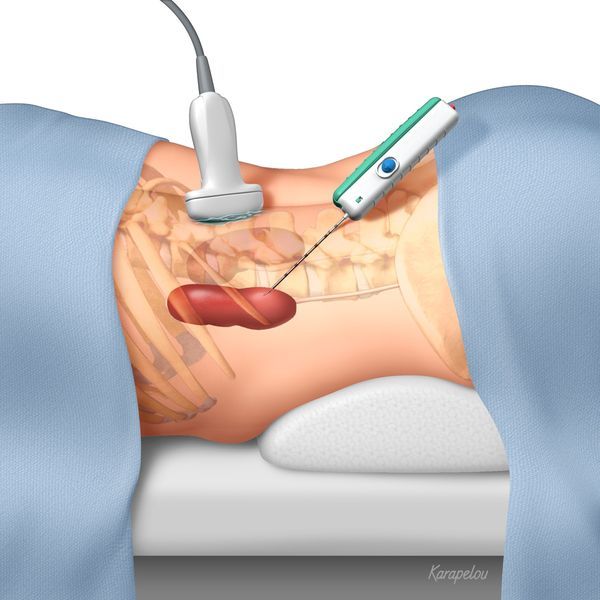
Биопсия почки
С помощью общего анализа мочи врач оценивает состояние мочевыделительной системы, а также наличие протеинурии и гематурии. Чем тяжелее протекает синдром, тем выше показатели белка и эритроцитов.
Диагностика зрения и слуха
Чтобы определить тяжесть тугоухости, проводят аудиометрию — безболезненную и безопасную процедуру, которая помогает выявить степень поражения слуха. Существует несколько видов аудиометрии:
- тональная — пациенту надевают специальные наушники, через которые подают звуки различной частоты: если человек что-то слышит, он нажимает на специальную кнопку, после чего врач отмечает на аудиограмме диапазон слышимости;
- речевая — врач произносит слова, меняя громкость и расстояние, а пациент повторяет услышанное;
- компьютерная — к голове пациента подключают электроды, которые фиксируют и передают на экран импульсы, возникшие в головном мозге в ответ на звуковые сигналы.

Тональная аудиометрия
У детей и подростков с синдромом Альпорта выявляют снижение слуха при высоких частотах, у взрослых пациентов — низко- и среднечастотную тугоухость.
Синдром Альпорта часто сопровождается передним лентиконусом, помутнением хрусталика и катарактой. Для диагностики этих состояний офтальмолог проводит:
- визометрию — пациенту по очереди закрывают глаза, после чего он называет различные символы, картинки или буквы, изображённые на таблице, которая находится на расстоянии 5 метров (чаще всего применяют таблицу Сивцева с буквами алфавита, а при осмотре детей, не умеющих читать, используют таблицу Орловой, на которой нарисованы разные картинки);
- офтальмоскопию — исследование глазного дна с помощью офтальмоскопа;
- биомикроскопию — осмотр хрусталика с помощью щелевой лампы.
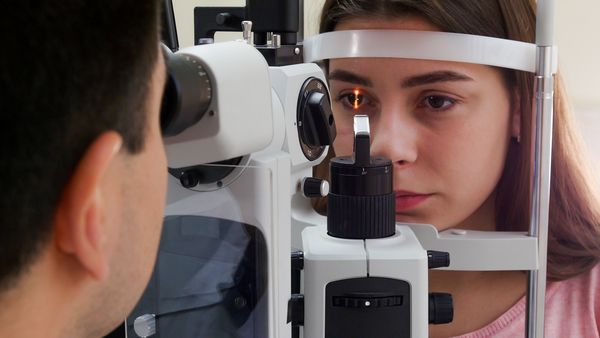
Биомикроскопия
Лечение синдрома Альпорта
Так как синдром Альпорта вызван генетическими мутациями, специфического лечения не существует, поэтому терапия направлена на устранение симптомов и осложнений, а также на сохранение функций почек. Одна из самых важных целей лечения — остановить или замедлить истончение и повреждение базальной мембраны, чтобы не допустить развития интерстициального фиброза почек.
Для этого сначала используют медикаментозную терапию:
- ингибиторы ангиотензин-превращающего фермента (иАПФ, например Рамиприл, Лизиноприл, Фозиноприл или Хинаприл);
- блокаторы рецепторов ангиотензина (БРА, к примеру Лозартан, Ирбесартан или Валсартан).
Они помогают снизить уровень белка и креатинина в моче, что позволяет замедлить прогрессирование гломерулосклероза, сосудистой и тубулоинтерстициальной патологии почек, которая сопровождается воспалением тубул и интерстиция (канальцев и окружающей их ткани).
Лечение проводят под регулярным контролем уровня калия в крови. Высокий уровень калия может вызвать нарушение сердечного ритма, судороги и аритмию, поэтому при его повышении дозировку препаратов уменьшают.
Лечение терминальной ХБП
Если у пациента развивается последняя стадия почечной недостаточности, ему назначают гемодиализ или трансплантацию почки [1].
Гемодиализ — это метод внепочечного очищения крови с помощью специального аппарата, в котором есть полупроницаемая мембрана. Продукты обмена, вода и бактерии остаются за пределами этой мембраны, а очищенная кровь возвращается через вену в организм.

Гемодиализ
В некоторых случаях проводят перитонеальный диализ — очищение крови с помощью фильтрации через брюшину. Сначала в брюшную полость вливают специальную жидкость — диализирующий раствор. В течение нескольких часов продукты обмена переходят в этот раствор через брюшину, после чего жидкость меняют на новую.
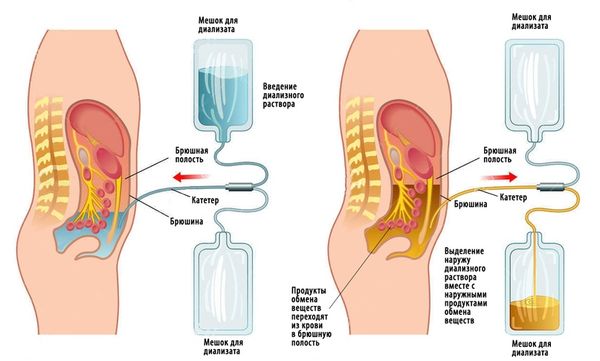
Перитонеальный диализ
Трансплантация почки — это хирургическая операция, во время которой пациенту пересаживают здоровую донорскую почку. Ранее считалось, что у человека с синдромом Альпорта повышен риск отторжения новой почки, но исследование, проведённое в 2013 году, показало, что он не выше, чем у пациентов с другими заболеваниями [13]. В России пересадка почки разрешена только от близких родственников.
Лечение внепочечных состояний
При возникновении нейросенсорной тугоухости пациенту подбирают слуховой аппарат.
Когда появляются серьёзные проблемы с хрусталиком, проводят операцию по его замене [3][15]. Другие нарушения глаз (кератоконус и миопию) лечат по стандартным офтальмологическим протоколам.
Прогноз. Профилактика
Прогноз синдрома Альпорта зависит от выраженности симптомов и типа наследования заболевания. Менее благоприятным типом наследования является аутосомно-рецессивный, более благоприятным — аутосомно-доминантный. К сожалению, ни в одном из случаев невозможно вылечить заболевание полностью.
Профилактика синдрома Альпорта
Так как заболевание носит наследственный характер, предотвратить его развитие нельзя. При установленном диагнозе у близких родственников, можно пройти генетическое тестирование, чтобы определить риск наличия синдрома у ребёнка. Обычно исследуют ДНК крови родственников на мутацию генов, что позволяет понять, являются ли они носителями данного заболевания. Особенно это важно, если женщина вынашивает плод мужского пола.
Чтобы снизить скорость прогрессирования синдрома Альпорта, важно вести здоровый образ жизни, в том числе:
- отказаться от курения;
- заниматься спортом;
- потреблять умеренное количество белка;
- ограничить потребление соли;
- поддерживать оптимальную массу тела (рекомендуется поддерживать значение ИМТ не выше 25 кг/м²) [4].

ИМТ
Список литературы
Каюков И. Г., Есаян А. М., Смирнов А. В., Сиповский В. Г., Кучер А. Г. Редкие заболевания в практике «взрослого» нефролога: наследственный нефрит (синдром Альпорта), болезнь тонкой базальной мембраны, олигомеганефрония // Нефрология. — 2008. — № 4. — С. 5–12.
Длин В. В., Игнатова М. С., Конькова Н. Е. Клинические рекомендации по диагностике и лечению синдрома Альпорта у детей // Российский вестник перинатологии и педиатрии. — 2015. — № 3. — С. 7–14.
Alport syndrome // Orphanet. — 2020.
Аксёнова М. Е. Синдром Альпорта: современные представления // Нефрология. — 2021. — № 4. — С. 451–460.
Игнатова М. С., Длин В. В. Наследственные заболевания почек, связанные с гематурией // Российский вестник перинатологии и педиатрии. — 2014. — № 5. — С. 18–25.
Mehta S., Saifan C., Abdellah M., Choueiry R. Alport's Syndrome in Pregnancy // Case Rep Med. — 2013. — Vol. 2013. — P. 374020.ссылка
Furlano M., Arlandis R., Venegas M. D. P. MYH9 Associated nephropathy // Nefrologia (Engl Ed). — 2019. — № 2. — P. 133–140. ссылка
Thanachatchairattana P., Losty P. Paediatric diffuse oesophageal leiomyomatosis with Alport syndrome // BMJ Case Rep. — 2024. — № 8. — P. e260442. ссылка
Garcia-Torres R., Cruz D., Orozco L. Alport syndrome and diffuse leiomyomatosis. Clinical aspects, pathology, molecular biology and extracellular matrix studies. A synthesis // Nephrologie. — 2000. — № 1. — P. 9–12.ссылка
Никишина Т. А. Значение молекулярно-генетических методов исследования в диагностике синдрома Альпорта // Российский вестник перинатологии и педиатрии. — 2017. — № 4. — С. 355–360.
Zhang Y., Ding J. Renal, auricular, and ocular outcomes of Alport syndrome and their current management // Pediatr Nephrol. — 2018. — № 8. — P. 1309–1316. ссылка
Kashtan C. E. Alport Syndrome: Achieving Early Diagnosis and Treatment // Am J Kidney Dis. — 2021. — № 2. — P. 272–279. ссылка
Горяйнов В. А., Каабак М. М., Бабенко Н. Н., Морозова М. М. и др. Аллотрансплантация почки от живых родственных доноров больным с синдромом Альпорта // Хирургия. Журнал им. Н. И. Пирогова. — 2016. — № 1. — С. 50–54.
Шагам Л. И., Шенцева Д. В. Молекулярно-генетические основы патогенеза синдрома Альпорта // Российский вестник перинатологии и педиатрии. — 2013. — № 6. — С. 25–28.
Savige J. Alport syndrome: its effects on the glomerular filtration barrier and implications for future treatment // J Physiol. — 2014. — № 18. — P. 4013–4023. ссылка
Watson S., Padala S. A., Hashmi M. F., Bush J. S. Alport Syndrome // StatPearls. — 2023.ссылка
Rosa J. M., Andrade Sobrinho M. V., Lipener C. Contact lens fitting in a patient with Alport syndrome and posterior polymorphous corneal dystrophy: a case report // Arq Bras Oftalmol. — 2016. — № 1. — Р. 42–43. ссылка

