Определение болезни. Причины заболевания
Синдром Мартина — Белл, или синдром ломкой Х-хромосомы (Fragile X syndrome), — это наследственное заболевание, связанное с увеличением числа тринуклеотидных повторов «цитозин-гуанин-гуанин» (CGG) в промоторной области гена FMR1, который расположен на Х-хромосоме в локусе Хq27.3. Такое заболевание сопровождается недостаточностью яичников, снижением овариального резерва и наступлением менопаузы до 40 лет у женщин, а также атаксией, которая проявляется дрожанием, шаткой походкой и иногда нарушением речи [1].

Атаксия
Распространённость этого синдрома среди мальчиков составляет 1 случай на 2500–4000 человек, среди девочек — 1 случай на 8000 человек [2]. Таким образом, у мальчиков синдром Мартина — Белл встречается в 2–3 раза чаще.
Кроме того, данная болезнь является самой частой причиной врождённой умственной отсталости после синдрома Дауна [4].
Впервые о синдроме рассказали британский невролог Дж. П. Мартин и генетик Дж. Белл в 1943 году. Совместно они опубликовали научную статью «Наследование умственных нарушений, связанных с полом», в которой описали членов одной семьи, страдающих умственной отсталостью и другими когнитивными нарушениями. Эти нарушения передавались из поколения в поколение и в основном наследовались по мужской линии: в семье было 11 мужчин с проявлениями олигофрении и 2 женщины с признаками задержки психического развития [6]. Соответственно, синдром был назван в честь этих учёных.
Исследование продолжил американский учёный и генетик Г. О. Лабс в 1969 году. Он провёл кариотипирование умственно отсталых мужчин и некоторых бессимптомных женщин из той же семьи и обнаружил перетяжку на длинном плече Х-хромосомы. Это выглядит так, будто у хромосомы «отломался» один кусочек. Поэтому этот синдром также называют синдромом ломкой Х-хромосомы [7].
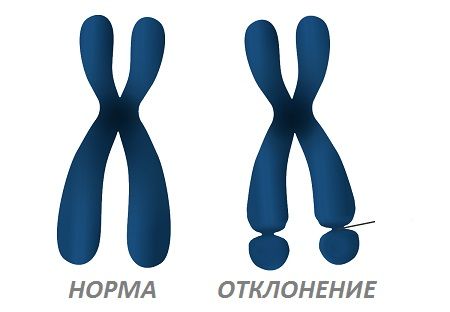
Ломкая Х-хромосома
Наконец, в 1983 году группа исследователей с помощью сканирующего электронного микроскопа выяснила, что поломка располагается именно в локусе Xq27.3 длинного плеча Х-хромосомы [8].
Причины развития синдрома Матина — Белл
Хромосомы — это нитевидные структуры, которые находятся внутри ядер клеток. Каждая клетка в норме содержит 23 пары хромосом (получается всего 46 хромосом в одной клетке), в которых хранится генетическая информация. Среди них 22 пары одинаковы у всех людей (их называют аутосомами), а 23-я пара содержит половые хромосомы, поэтому у мужчин и женщин они отличаются. Девочки рождаются с двумя Х-хромосомами, мальчики же получают по одной Х- и Y-хромосоме [3].
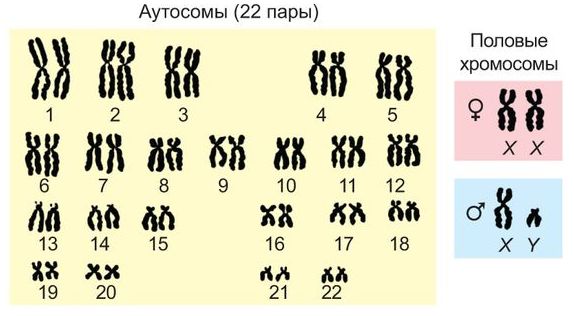
Набор хромосом
Как было указано ранее, в Х-хромосоме находится ген FMR1, который отвечает за выработку рибонуклеопротеинов (РНП). Специфическим представителем РНП-белков является белок FMRP — посредник ломкой Х-хромосомы [4].
Синдром ломкой Х-хромосомы — это доминантное заболевание, т. е. для его развития достаточно лишь одной копии мутантного гена. Так как у мальчиков есть только одна Х-хромосома, у них синдром встречается чаще и протекает тяжелее. У девочек симптомы проявляются слабее или часто отсутствуют вовсе, так как у них есть 2 Х-хромосомы, одна из которых обычно оказывается здоровой.
Как правило, женщины являются бессимптомными носителями заболевания, при этом именно носительство матери повышает вероятность рождения больного ребёнка: мужчина с мутацией гена FMR1 может передать её только своим дочерям, а женщина — детям обоих полов [18].
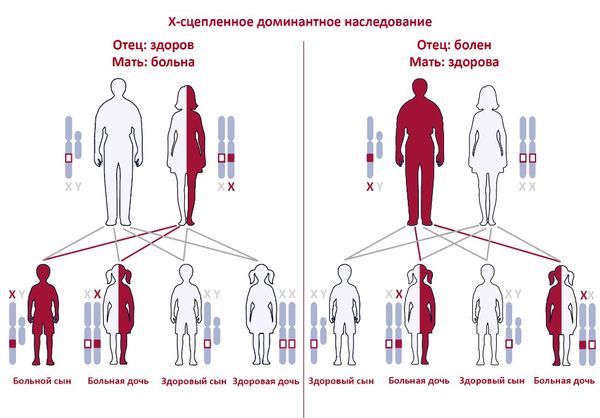
Тип наследования синдрома
Симптомы синдрома Мартина — Белл
У мальчиков с таким заболеванием наблюдаются специфические внешние черты:
- удлинённое лицо с высоким лбом и тупым кончиком носа;
- большие оттопыренные уши;
- широкие кисти и стопы;
- гиперподвижность суставов, гиперрастяжимость кожи и другие проявления дисплазии (нарушения развития) соединительной ткани;
- макроорхидизм (крупные яички) в подростковом возрасте.
![Мальчики с синдромом ломкой Х-хромосомы: от наиболее к менее выраженным внешним проявлениям болезни [20] Мальчики с синдромом ломкой Х-хромосомы: от наиболее к менее выраженным внешним проявлениям болезни [20]](/media/bolezny/sindrom-martina-bell/malchiki-s-sindromom-lomkoy-h-hromosomy-ot-naibolee-k-menee-vyrazhennym-vneshnim-proyavleniyam-bolezni-20_s_8rMBNQL.jpeg?dummy=1766578200509)
Мальчики с синдромом ломкой Х-хромосомы: от наиболее к менее выраженным внешним проявлениям болезни [20]
Среди психоневрологических проявлений выделяют:
- умственную отсталость лёгкой или умеренной степени тяжести (в крайне редких случаях она достигает тяжёлой степени тяжести);
- расстройства аутистического спектра (ребёнок бесцельно повторяет движения, слова или фразы, не смотрит в глаза, беспокоится, когда к нему прикасаются, и т. д.);
- нарушение развития речи («бормочущая», быстрая и сбивчивая речь), в том числе её понимания;
- высокий уровень тревожности;
- синдром дефицита внимания и гиперактивности (СДВГ);
- трудности в планировании, переключении внимания, решении зрительно-пространственных задач [9].
Во взрослом возрасте появляются следующие симптомы:
- снижение овариального резерва (синдром первичной яичниковой недостаточности), раннее наступление менопаузы (до 40 лет) и развитие остеопороза у женщин;
- судорожные эпилептические припадки (появляются у 14 % мужчин и примерно у 6 % женщин) [10];
- тремор рук;
- беспорядочные неловкие движения;
- нарушение равновесия при ходьбе или в положении стоя, шаткая походка.
Патогенез синдрома Мартина — Белл
Синдром ломкой Х-хромосомы развивается при недостатке специфического белка FMRP. Он вырабатывается в головном мозге, сетчатке глаза, хрящевых структурах и в печени ещё на ранних стадиях эмбриогенеза (зародышевого развития организма) и играет важную роль в нормальном созревании нервных клеток.
К 25-й неделе беременности его продукция достигает пика в холинергических нейронах базального ядра и пирамидных нейронах гиппокампа — структурах, критически важных для процессов памяти и обучения. После рождения максимальная экспрессия FMRP наблюдается в головном мозге, половых железах, глазах и селезёнке [5]. При отсутствии FMRP у ребёнка развиваются расстройства аутистического спектра, психоэмоциональные расстройства и умственная отсталость разной степени тяжести [1].

Структуры мозга
За выработку этого белка отвечает ген FMR1, в котором наблюдается повторяющаяся последовательность из трёх нуклеотидов — CGG (цитозин-гуанин-гуанин). У здоровых людей насчитывается от 6 до 54 CGG-повторов. Однако при синдроме Мартина — Белл первоначальная структура Х-хромосомы меняется из-за мутации, поэтому во время деления клетки количество этих повторов увеличивается.
Если число CGG-повторов повышается от 55 до 200, в этом случае говорят о премутации: продукция белка FMRP снижается, но не прекращается полностью, поэтому заболевание не проявляется в детстве, но может дать знать о себе во взрослом возрасте. Например, у таких людей появляется синдром тремора и атаксии. Кроме того, они являются носителями мутации, которую в дальнейшем могут передать своему ребёнку. Так как премутация нестабильна, в следующем поколении она может расширяться до полной мутации, особенно если её передала мать.
Полная мутация гена развивается, когда количество тринуклеотидных повторов превышает 200 и выработка белка FMRP практически полностью прекращается. Это приводит к ослаблению синаптических контактов между нейронами головного мозга, что и является причиной специфических нейропсихологических расстройств у детей.
Также некоторые авторы сообщают, что для этого синдрома характерен феномен антиципации — передача болезни в пределах одной родословной с утяжелением симптомов при смене поколений [2].
Классификация и стадии развития синдрома Мартина — Белл
Синдром ломкой Х-хромосомы принято классифицировать по наличию мутации в гене FMR1:
- нормальное состояние — в гене менее 54 CGG-повторов;
- премутация — от 55 до 200 повторов;
- полная мутация — более 200 повторов.
Также выделяют два варианта синдрома:
- классический (FRAXA) — CGG-повторы располагаются в локусе Хq27.3 длинного плеча Х-хромосомы в гене FMR1;
- неклассический (FRAXE) — повторы находятся в локусе Хq28 в гене FMR2 [11].
Второй вариант протекает легче: он сопровождается трудностями в обучении у детей и общей задержкой развития.
Осложнения синдрома Мартина — Белл
Из-за снижения интеллекта и развития различных психоэмоциональных расстройств ребёнку с синдромом ломкой Х-хромосомы трудно адаптироваться в обществе и найти общий язык со сверстниками, что может повлечь за собой социальную изоляцию.
Преждевременная менопауза у женщин сопровождается климактерическими симптомами и прекращением репродуктивной функции, т. е. развитием бесплодия. Кроме того, снижение уровня эстрогенов почти в 2 раза повышает риск развития рака молочной железы. Также пациенток с синдромом Мартина — Белл часто беспокоит артериальная гипертензия, ишемическая болезнь сердца, висцеральное ожирение, инсулинорезистентность, сахарный диабет и остеопороз, который проявляется хрупкостью и ломкостью суставов, что грозит переломами даже при незначительном внешнем воздействии [12].
Тремор рук, трудности в координации и судорожные эпилептические припадки со временем могут привести к тому, что пациент перестаёт справляться даже с бытовыми делами и нуждается в помощи другого человека.

Судорожные эпилептические припадки
Диагностика синдрома Мартина — Белл
При подозрении на синдром ломкой Х-хромосомы диагностику проводит сразу несколько специалистов: генетик, педиатр, невролог, психотерапевт, логопед и гинеколог. В первую очередь врачи оценивают клинические критерии (внешний вид, характерные симптомы), после чего проводят специфическое обследование.
Основным методом диагностики является ПЦР-тест — фрагментный анализ гена FMR1, который позволяет определить количество CGG-повторов. Этот анализ проводят с помощью забора венозной крови. Её можно сдать утром натощак или в течение дня, но не ранее чем через 3 часа после приёма пищи. Если диагност выявляет:
- менее 44 повторов — синдром Мартина — Белл исключают;
- 45–59 повторов — диагноз исключают, но указывают на вероятность возникновения этого синдрома через поколение и у дальних родственников;
- 60–199 повторов — возможен лёгкий фенотип синдрома, т. е. повышен риск развития первичной яичниковой недостаточности и возникновения атаксии в дальнейшем, также увеличивается риск развития синдрома у следующего поколения;
- 200 и более повторов — врач подтверждает диагноз, вероятность передачи болезни ребёнку составляет 50 % [15].
К дополнительным методам диагностики относятся:
- Электроэнцефалография (ЭЭГ) — при синдроме отмечается повышенная тета-активность (особенно 6–7 Гц) в теменно-центральных зонах коры головного мозга и дефицит альфа-ритма, что указывает на функциональную незрелость корковых нейронных сетей с нарушением баланса между возбуждением и торможением нервных клеток. Этим объясняется снижение интеллекта, повышенная тревожность и другие симптомы [13]. В некоторых случаях также регистрируют синдром «эпилептической энцефалопатии» с диффузно-продолженной пик-волновой активностью в фазе медленного сна. Такое состояние редко сопровождается судорогами, но значительно влияет на общее развитие: у ребёнка ухудшается речь, страдает память, внимание и интеллект, появляются поведенческие проблемы (гиперактивность, агрессия, аутистические черты) и моторные нарушения (атаксия, непроизвольные сокращения мышц) [14].
ЭЭГ
- Магнитно-резонансная томография (МРТ) головного мозга — выявляет уменьшение общего объёма головного мозга, мозжечка, таламуса, хвостатого ядра и гиппокампа, который отвечает за управление памятью, ориентацией в пространстве и т. д. Она также указывает на снижение плотности серого вещества головного мозга [16].
Чтобы поставить точный диагноз, врачи проводят дифференциальную диагностику. Они исключают:
- синдром Сотоса;
- синдром Прадера — Вилли;
- синдром Клайнфельтера;
- синдром Ретта;
- синдром Дауна;
- метаболический синдром;
- аутизм [19].
Лечение синдрома Мартина — Белл
Полностью вылечить синдром ломкой Х-хромосомы невозможно, но терапия помогает повысить качество жизни больного [18]. Лечение синдрома делится на патогенетическую и симптоматическую терапию. Первый подход направлен на коррекцию ключевых звеньев патогенеза (механизма развития болезни), а второй — на устранение симптомов и осложнений.
Патогенетическая терапия:
- препараты, избирательно действующие на определённые рецепторы, (2-метил-6-(фенилэтинил)пиридин) — позволяют нормализовать синаптические связи между нейронами головного мозга;
- препараты лития — предупреждают развитие маниакальных и депрессивных состояний, стабилизируют настроение;
- антихолинэстеразные препараты, агонисты ГАМК-А и ГАМК-В — снимают возбуждение, оказывают успокаивающее действие и устраняют мышечные спазмы [2].
Симптоматическое лечение:
- ноотропные препараты (Пирацетам, Церебролизин и др.) — улучшают мозговое кровообращение, стимулируют интеллектуальную деятельность, повышают память и устойчивость мозга к повреждающим факторам;
- производные гамма-аминомасляной кислоты (L-карнитин) — улучшают обмен веществ, помогают выводить токсичные вещества из организма;
- антиконвульсанты (Карбамазепин и препараты Вальпроевой кислоты) — устраняют судорожные симптомы;
- антипсихотические средства (Арипипразол и др.) — ослабляют психомоторное возбуждение, успокаивают нервную систему, улучшают когнитивные функции и повышают качество жизни;
- селективные ингибиторы обратного захвата серотонина (Флуоксетин и др.) — снижают депрессивные симптомы [2];
- заместительная гормональная терапия (ЗГТ) — назначают при синдроме преждевременной яичниковой недостаточности.
Важно помнить, что каждое лекарственное средство, указанное выше, имеет ряд побочных эффектов, поэтому единой схемы лечения нет. Правильно подобрать терапию может только врач.
Также важным компонентом лечения является поддержка семьи, специальные образовательные программы, профессиональная и сенсорная интеграция и т. д. Это обеспечивает пациенту комфортную адаптацию в обществе, а также помогает компенсировать когнитивные и поведенческие нарушения, что значительно повышает уровень его жизни.

Сенсорная интеграция
Таким образом, лечение синдрома Мартина — Белл должно быть комплексным, включая консультации психиатра, невролога, логопеда, дефектолога, нейропсихолога, физиотерапевта и др.
Прогноз. Профилактика
Прогноз при полной мутации зависит от своевременной постановки диагноза и начала лечения. Зачастую умственное и психическое развитие детей с синдромом Мартина — Белл останавливается ближе к подростковому возрасту, поэтому лечение необходимо начать как можно раньше, до наступления пубертата.
Специфической профилактики синдрома ломкой Х-хромосомы нет. Однако есть возможность остановить дальнейшую передачу болезни. Если в семье у кого-то уже есть подобный синдром, необходимо проконсультироваться с генетиком и сделать ПЦР-тест для подтверждения или опровержения мутации в гене FMR1. Если тест выявил отклонение от нормы у женщины, при планировании беременности будущим родителям рекомендуют использовать донорские яйцеклетки или эмбрионы по программе ЭКО [17].
При желании использовать собственные яйцеклетки или наличии мутации у мужчины следует провести преимплантационную генетическую диагностику, чтобы имплантировать здоровый, не затронутый мутацией эмбрион.
Список литературы
Jacquemont S., Hagerman R. J., Hagerman P. J., Leehey M. A. Fragile-X syndrome and fragile X-associated tremor/ataxia syndrome: two faces of FMR1 // Lancet Neurol. — 2007. — № 1. — Р. 45–55.ссылка
Данилина К. К., Горбачевская Н. Л. Симптоматическая и патогенетическая терапия пациентов с синдромом умственной отсталости, сцепленной с ломкой хромосомой Х (синдромом Мартина-Белл) // Журнал неврологии и психиатрии им. С. С. Корсакова. — 2014. — № 1. — С. 65–70.
Момыналиев К. Азбука генетики. Основы медицинской генетики для непрофессионалов: методическое пособие // TreeGene. [Электронный ресурс]. Дата обращения: 24.12.2025.
Verheij C., Bakker C. E., de Graaff E., Keulemans J., Willemsen R. et al. Characterization and localization of the FMR-1 gene product associated with fragile X syndrome // Nature. — 1993. — № 6431. — Р. 722–724. ссылка
Переверзева Д. С., Тюшкевич С. А., Улас Е. В., Горбачевская Н. Л. Спектр синдромальных нарушений при экспансии CGG-повторов промотера гена FMR1: патогенетические механизмы и клинические проявления // Журнал высшей нервной деятельности им. И. П. Павлова. — 2022. — № 3. — С. 293–296.
Martin J. P., Bell J. A pedigree of mental defect showing sex-linkage // J Neurol Psychiatry. — 1943. — № 3–4. — Р. 154–157. ссылка
Lubs H. A. A marker X chromosome // Am J Hum Genet. — 1969. — № 3. — Р. 231–244.ссылка
Harrison C. J., Jack E. M., Allen T. D., Harris R. The fragile X: a scanning electron microscope study // J Med Genet. — 1983. — № 4. — Р. 280–285.ссылка
Hall S. S., Burns D. D., Lightbody A. A., Reiss A. L. Longitudinal changes in intellectual development in children with Fragile X syndrome // J Abnorm Child Psychol. — 2008. — № 6. — Р. 927–939. ссылка
Berry-Kravis E., Raspa M., Loggin-Hester L., Bishop E., Holiday D., Bailey D. B. Seizures in fragile X syndrome: characteristics and comorbid diagnoses // Am J Intellect Dev Disabil. — 2010. — № 6. — Р. 461–472. ссылка
Иллариошкин С. Н. Заболевания, обусловленные экспансией тандемных микросателлитных повторов // Национальное руководство по неврологии. — 2012. — С. 511–537.
Малов А. Г. Нейропсихологические расстройства при синдроме ломкой Х-хромосомы // Научная статья. — 2019. — С. 668–676.
Горбачевская Н. Л. Современные подходы к диагностике и лечению когнитивных нарушений у детей и взрослых // Психологическая наука и образование. — 2010. — № 5. — С. 268–275.
Калашникова Т. П., Малов А. Г., Основина Т. А. Эпилептическая энцефалопатия при синдроме Мартина — Белл // Уральский медицинский журнал. — 2017. — № 9. — С. 50–53.
Кузнецова Е. Б., Стрельников В. В., Танас А. С., Немцова М. В., Залетаев Д. В. Технология комплексной ДНК-диагностики синдрома ломкой Х-хромосомы // Медицинская генетика. — 2018. — № 6. — С. 18–23.
Воинова В. Ю., Юров И. Ю., Ворсанова С. Г., Юров Ю. Б. Умственная отсталость и хромосома Х: монография. — М.: Издательский дом Академии Естествознания, 2016. — С. 48–49.
Рштуни С. Д., Зарецкая Н. В., Кузнецова М. В., Марченко Л. А. Особенности наследования тринуклеотидных CGG повторов в гене FMR1 от женщин с преждевременной недостаточностью яичников: серия случаев // Акушерство и гинекология. — 2023. — № 3.
Гамисония А. Синдром ломкой X-хромосомы // ГЕНОКАРТА. — 2019.
Hunter J. E., Berry-Kravis E., Hipp H., Todd P. K. FMR1 Disorders // GeneReviews. — 2024.ссылка
Lachiewicz A. M, Dawson D. V., Spiridigliozzi G. A. Physical characteristics of young boys with fragile X syndrome: reasons for difficulties in making a diagnosis in young males // Am J Med Genet. — 2000. — № 4. — Р. 229–236. ссылка

