Определение болезни. Причины заболевания
Синдром Гудпасчера (Goodpasture syndrome) — это редкое аутоиммунное заболевание, которое поражает почки и лёгкие, что проявляется лёгочными кровотечениями и быстро прогрессирующим гломерулонефритом.
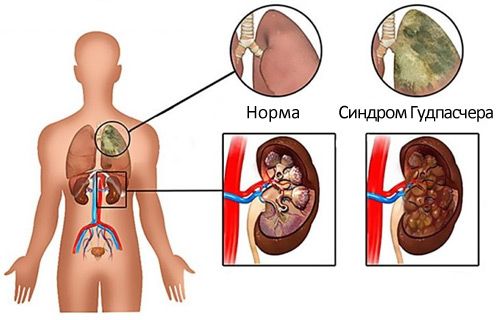
Синдром Гудпасчера
Распространённость синдрома Гудпасчера
Частота этой болезни составляет 1 случай на 1 млн населения. Чаще её находят у мужчин [6].
Обычно синдром Гудпасчера диагностируют в возрасте от 20 до 30 лет, второй пик заболеваемости приходится на возраст старше 50–60 лет [6]. При этом заболеть могут люди любого возраста, в том числе и дети. Однако точных данных о распространённости этого синдрома среди детей нет [7].
Причины развития синдрома Гудпасчера
Сейчас точно неизвестно, с чем связано формирование этого синдрома. Исследователи пока лишь предполагают, какие факторы могут влиять на его развитие. К ним относятся:
- вирусные инфекции (например, вирус гриппа, а также ВИЧ-инфекция) — при пневмоцистной пневмонии у ВИЧ-инфицированных пациентов обнаруживались антитела к базальной мембране клубочков (анти-БМК антитела), что является одним из признаков синдрома Гудпасчера [3];
- грибковая инфекция — зарегистрирован случай возникновения синдрома Гудпасчера у пациента с вторичным амилоидозом на фоне грибкового поражения кожи [5];
- лекарственные препараты — наиболее убедительной является связь между развитием синдрома и приёмом D-пенициламина, также возможно влияние других лекарственных веществ, например Азатиоприна [12];
- токсические вещества (углеводороды, кокаин);
- онкологические заболевания — предполагается, что в случае роста опухоли иммунитет может начать вырабатывать анти-БМК антитела;
- генетическая предрасположенность — учёные обнаружили, что наличие таких генов, как HLA-DR15, HLA-DR4 и HLA-DRW2, увеличивает вероятность развития синдрома Гудпасчера; также обсуждается значение мутации в гене, кодирующем альфа-3-цепь коллагена 4-го типа, который находится в базальных мембранах почек, так как именно эта цепь является мишенью анти-БМК антител [1][3][5].
Симптомы синдрома Гудпасчера
В начале заболевания симптомы могут быть неспецифичными, т. е. похожими на проявления других болезней. К ним относятся общая слабость, недомогание, повышение температуры, боль в суставах, снижение веса и повышенная потливость.
По мере прогрессирования болезни появляются признаки поражения почек или лёгких. Они могут возникнуть одновременно относительно друг друга, но у 70 % пациентов первым специфичным симптомом является кровохарканье: при откашливании человек обнаруживает в мокроте прожилки или сгустки крови [4]. Стоит отметить, что интенсивность кровохарканья не всегда связана с интенсивностью лёгочного кровотечения, т. е. при довольно массивном кровотечении в мокроте крови может быть немного.
Поражение лёгких обычно сопровождается симптомами дыхательной недостаточности. Среди них выделяют:
- диспноэ — субъективные ощущения затруднённого дыхания;
- тахи- или брадипноэ (учащение или урежение дыхательных движений) — человек делает более 25 или менее 12 вдохов и выдохов в минуту;
- синюшность кожи — чаще губ и носогубного треугольника;
- нарушения со стороны нервной системы — это могут быть как минимальные проявления вроде плохого запоминания текущих событий, так и более серьёзные нарушения в виде потери сознания и комы [13];
- одышка;
- частый сухой кашель;
- учащённое сердцебиение;
- снижение артериального давления.
В случае развития острой дыхательной недостаточности массивное кровотечение может привести к смерти.
Следом за лёгочной симптоматикой появляются признаки поражения почек: гематурия и олигурия.
Гематурия — это патологическое состояние, при котором в моче находят клетки крови (эритроциты). Гематурия может быть незначительной, так что обнаружить её можно только при лабораторном анализе мочи. Однако примерно у 30 % пациентов с синдромом Гудпасчера выявляется макрогематурия, которую видно невооружённым глазом: моча становится красной [5].
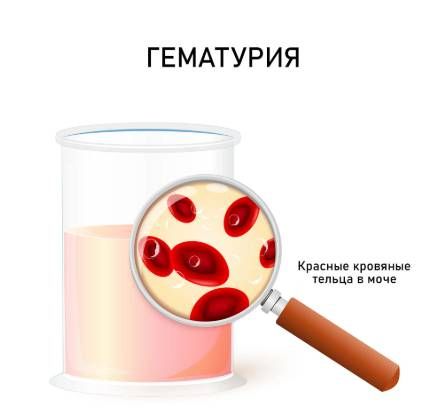
Гематурия
Олигурия — это уменьшение количества мочи. Иногда наблюдается полное её отсутствие (анурия), что говорит о быстро прогрессирующей хронической болезни почек, которая обычно развивается в течение нескольких недель. На фоне снижения объёма мочи у пациента нарастает отёчность.
Из-за кровопотери вследствие кровохарканья (или лёгочного кровотечения) и гематурии у больного развивается анемия, которая проявляется слабостью, бледностью кожи, невозможностью выполнять привычные физические нагрузки, головокружением и шумом в ушах.
К редким симптомам синдрома Гудпасчера относятся:
- двусторонний ретинит — воспаление сетчатки глаза, которое иногда сопровождается значительным снижением остроты зрения;
- увеит — воспаление радужки, цилиарного тела или хориоидеи (сосудистой оболочки глаза), при котором снижается острота зрения, возникает слезотечение, раздражение и покраснение глаз [5].
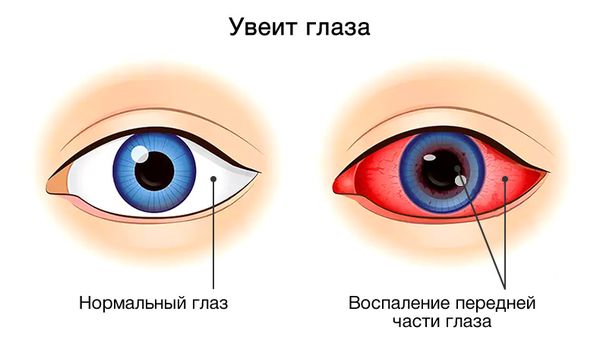
Увеит
Человек, который замечает у себя похожие симптомы, должен немедленно обратиться в больницу.
Патогенез синдрома Гудпасчера
Главную роль в развитии синдрома Гудпасчера играют цитотоксические тканевые реакции, при которых иммунная система атакует собственные ткани, в частности базальные мембраны почечных клубочков и альвеол лёгких.
Почечный клубочек — это сеть капилляров, в которых фильтруется кровь, после чего образуется первичная моча. Капилляры клубочка состоят из специальных эндотелиальных клеток и покрыты базальной мембраной — трёхслойной пластинкой, которая не содержит клеток. В основном она состоит из крупных молекул белков (гликопротеинов, протеогликанов) и коллагена 4-го типа. С внутренней стороны базальной мембраны находятся эндотелиальные клетки капилляров, а снаружи к ней прилегают эпителиальные клетки со специальными выростами — подоциты.
![Клубочковая фильтрация [15] Клубочковая фильтрация [15]](/media/bolezny/sindrom-gudpaschera/klubochkovaya-filtraciya-15_s.jpeg)
Клубочковая фильтрация [15]
В альвеолах дыхательная мембрана служит границей между капиллярами и окружающим воздухом, через которую осуществляется газообмен. Она состоит из лёгочного сурфактанта: жидкой части, эпителиального слоя и базальной мембраны.
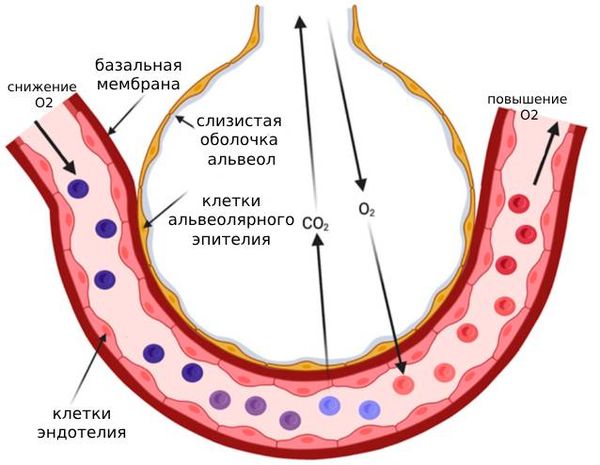
Базальная мембрана в альвеолах
Анти-БМК антитела связываются с альфа-3-цепью коллагена 4-го типа через её отдельный участок — неколлагеновый домен, образуя иммунные комплексы и активируя систему комплемента (систему защитных беков, циркулирующих в крови). Всё это приводит к тому, что в клубочках и альвеолах значительно увеличивается количество воспалительных клеток (Т-лимфоцитов и макрофагов), которые разрушают ткань, из-за чего на базальной мембране появляются множественные разрывы. Через них в очаг воспаления поступают воспалительные белки и клеточные элементы.
В капсуле почечных клубочков (капсуле Боумена) скапливается большое количество фибрина, который приводит к образованию сгустков крови, а также образуются характерные скопления клеток в виде полулуний. Капсула, заполненная полулуниями, сдавливает почечные капилляры, из-за чего количество нормально работающих клубочков уменьшается, так же как и способность почки к фильтрации мочи. В результате развивается почечная недостаточность [5].
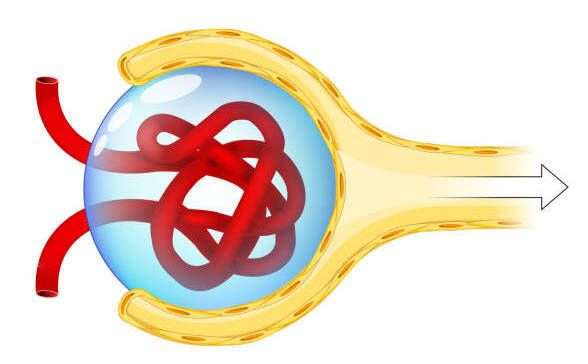
Капсула Боумена с клубочком внутри
В лёгких из-за разрушения капилляров и повреждения базальной мембраны наблюдаются альвеолярные кровотечения или кровотечения в лёгочный интерстиций (соединительную ткань внутри лёгкого).
Тканевое повреждение увеличивается из-за действия провоспалительных цитокинов (фактора некроза опухоли, интерлейкина 1, металопротеазы-9) и фактора роста. Они усиливают воспалительные реакции, тем самым стимулируя перемещение иммунных клеток к очагу воспаления, и в результате создаётся порочный круг: объём воспаления растёт и в связи с этим увеличивается объём поражённой ткани.
Классификация и стадии развития синдрома Гудпасчера
Синдром Гудпасчера относится к редким иммунокомплексным органоспецифическим системным васкулитам, при которых воспаляются и отмирают стенки мелких сосудов [8][11]. К таким болезням также относится криоглобулинемический васкулит, болезнь Шейнлен — Геноха (геморрагический васкулит) и гипокомплементемический уртикарный васкулит. Все они характеризуются образованием иммунных комплексов «антиген-антитело», которые циркулируют по крови или скапливаются в тканях поражённого органа (например, в капсуле Боумена, как в случае синдрома Гудпасчера).

Васкулит
Общепринятая классификация синдрома Гудпасчера не разработана, но в клинической практике используют классификацию, которая основана на особенностях течения болезни. Она выделяет 3 варианта течения синдрома Гудпасчера:
- Злокачественный — протекает с часто повторяющейся пневмонией, которая сопровождается кровохарканьем, лёгочным кровотечением и прогрессирующим диффузным гломерулонефритом. Заболевание быстро развивается с формированием почечной и иногда лёгочной недостаточности. У пациента рано формируется выраженная железодефицитная анемия (3–4-й степени). В редких случаях этот вариант болезни может привести к смерти в течение нескольких часов, поэтому такой вид синдрома называют молниеносным.
- Умеренный — развивается медленнее, симптомы выражены не так сильно. Признаки поражения лёгких проявляются по-разному в зависимости от периода заболевания. Например, при обострении у пациента усиливается кашель, появляются прожилки крови в мокроте, повышается температура до 38 °C и нарастает одышка. Поражение почек обнаруживают в более поздние периоды болезни, когда выявляют протеинурию (белок в моче) и изменение мочевого осадка.
- Медленно прогрессирующий — с начала и до конца такой вид синдрома сопровождается симптомами хронического гломерулонефрита и болезни почек: уменьшением количества мочи, отёками на лице, руках и ногах, изменениями в анализах мочи и т. д. При терминальной почечной недостаточности (жизнеугрожающем состоянии) может присоединиться артериальная гипертензия. Поражение лёгких в этом случае проявляется только в последнюю очередь, но необязательно в виде кровохарканья или лёгочного кровотечения [3][10].
Осложнения синдрома Гудпасчера
Осложнения синдрома Гудпасчера развиваются в органах-мишенях этого заболевания — лёгких и почках.
Лёгочное кровотечение способствует формированию фиброзирующего альвеолита и пневмонии с фиброзом. Кроме того, если кровь попадает в соединительную ткань лёгкого, вместе такие состояния приводят к развитию хронической дыхательной недостаточности [4].
Так как лёгкие больше не могут обеспечивать газообмен на должном уровне, количество кислорода в крови снижается. Наиболее чувствителен к недостатку кислорода головной мозг, поэтому в зависимости от степени дыхательной недостаточности пациент может отмечать различные симптомы от ухудшения памяти до выраженного психомоторного возбуждения, которое характеризуется суетливыми, хаотичными или повторяющимися движениями (например, покачиванием тела, потиранием рук и т. д.), сбивчивой, бессвязной речью, слуховыми или зрительными галлюцинациями. В некоторых случаях наступает гипоксемическая кома — потеря сознания на фоне недостатка кислорода.
Поражение мембран клубочков почки приводит к развитию хронической почечной недостаточности, из-за чего количество выделенной мочи снижается (вплоть до полного её отсутствия) и в организме скапливаются уремические токсины (креатинин, мочевина, аммиак, паратиреоидный гормон, калий и др.). Это приводит к выраженной интоксикации, которая сопровождается тошнотой, рвотой и мучительным кожным зудом.
Кроме того, хроническая болезнь почек может привести:
- к повышению артериального давления;
- отёкам;
- нарушению сердечной деятельности;
- гиперактивности симпатической нервной системы (проявляется широким спектром симптомов, включая тахикардию, потливость, тревожность, тремор, нарушения пищеварения и др.);
- активации ренин-ангиотензин-альдостероновой системы (сопровождается гипертонией, отёками, тахикардией, снижением почечного кровотока, признаками перегрузки сердца и т. д.).
В терминальной (заключительной) стадии пациенты с хронической почечной недостаточностью нуждаются в гемодиализе — очистки крови от вредных веществ с помощью специальной аппаратуры [1].
Диагностика синдрома Гудпасчера
При возникновении лёгочных симптомов необходимо обратиться к пульмонологу, при почечных — к нефрологу. Если у пациента есть признаки поражения обеих систем, его ведут оба специалиста.
Большое значение в диагностике имеет лёгочное кровотечение, даже если оно произошло задолго до обращения (например, год назад), так как заболевание может рецидивировать. Поэтому, если когда-то было такое кровотечение, нужно обязательно рассказать доктору.
На осмотре врач обращает внимание на бледность кожи, цианоз (посинение) губ, отёчность лица, учащённое и поверхностное дыхание. При синдроме Гудпасчера артериальное давление чаще нормальное или незначительно повышенное, пульс частый, малого наполнения, в лёгких выслушивается жёсткое дыхание, крепитация (хрустящий звук), сухие или влажные разнокалиберные хрипы [10].
Лабораторное исследование
По результатам общего анализа крови, у пациента отмечается снижение уровня гемоглобина и эритроцитов, уменьшение диаметра эритроцитов и их неправильная форма (всё это указывает на железодефицитную анемию). Также может быть повышен уровень лейкоцитов и увеличена скорость оседания эритроцитов (СОЭ).
Почечное поражение при синдроме Гудпасчера проявляется нарастающей азотемией: в крови повышается концентрация азотистых продуктов белкового обмена, главным образом креатинина и мочевины. В случаях злокачественного течения уровень азотемии может достичь терминального в течение нескольких суток (уровень креатинина превышает 700–800 мкмоль/л) [5]. Также в крови увеличивается содержание калия и мочевой кислоты.
В моче выявляют умеренное повышение белка, эритроцитов, а также возможно появление эритроцитарных цилиндров [3][5].
Инструментальная диагностика
Чаще всего пациента направляют на рентген или компьютерную томографию (КТ) лёгких, с помощью которых можно увидеть двусторонние рыхлые инфильтраты, распространяющиеся от корней лёгких к периферии. При лёгочном кровотечении могут определяться обширные зоны затемнения.
Однако наиболее достоверным методом диагностики синдрома Гудпасчера является выявление антител к базальной мембране клубочка почки. Для этого исследуют либо сыворотку крови, либо ткань почки, полученную с помощью биопсии [1].
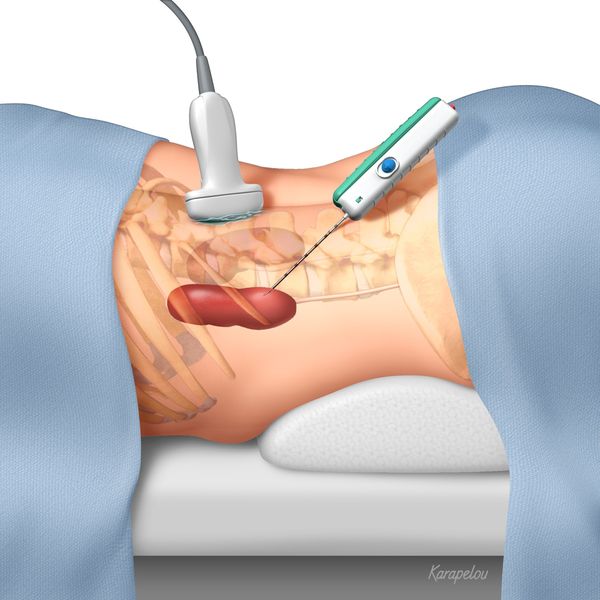
Биопсия почки
Наиболее чувствительным методом обследования сыворотки крови является радиоиммунный анализ, основанный на реакции антиген-антитело. Почечную ткань изучают с помощью различных видов микроскопии: световой, электронной и иммунофлуоресценции. Световая и электронная микроскопия показывают неспецифические признаки патологии клубочков (разрастание клеток и некроз, который впоследствии переходит в фиброз и гломерулосклероз). А при прямой иммунофлуоресценции с помощью специальных веществ, помеченных флюоресцентным красителем, можно увидеть специфичные для почечно-лёгочного синдрома линейные отложения иммуноглобулина G и комплемента (С3) на базальной мембране клубочка [6].
Дифференциальная диагностика
При кровохарканье врач обязательно исключает бронхоэктатическую болезнь, злокачественные и доброкачественные опухоли бронхов, микобактериальные инфекции (особенно туберкулёз), абсцесс лёгкого, системные васкулиты (болезнь Бехчета, гранулематоз Вегенера) и др. [9]
Если первичным является почечное поражение, синдром необходимо дифференцировать с острым гломерулонефритом, системной красной волчанкой и т. д.
Лечение синдрома Гудпасчера
Лечение синдрома Гудпасчера проводят ревматологи, пульмонологи и нефрологи совместно.
Основные цели терапии:
- быстрое удаление циркулирующих в крови антител;
- остановка дальнейшей выработки антител;
- подавление существующего тканевого воспаления;
- лечение возникших осложнений.
Для удаления циркулирующих антител используют плазмаферез — удаление части плазмы пациента, внутри которой находятся антитела, с заменой на донорскую плазму. Потерянный объём также могут восполнить с помощью внутривенного капельного введения белка или других жидкостей (например, физиологического раствора или 5%-го раствора глюкозы). Чтобы добиться выраженного снижения уровня циркулирующих антител, процедуру необходимо проводить ежедневно в течение нескольких недель.
Кроме того, плазмаферез улучшает работу почек у 80 % пациентов с уровнем креатинина ниже 600 мкмоль/л, которым не требуется диализ [6]. Разница этих методик заключается в том, что при гемодиализе после очищения крови все её компоненты (и клетки, и плазму) возвращают обратно в кровяное русло, а при плазмаферезе плазму замещают.

Гемодиализ
Чтобы остановить дальнейшую выработку антител и подавить воспаление, используют иммуносупрессивную терапию с контролем уровня анти-БМК антител. Для этого пациент должен одновременно принимать Циклофосфамид и глюкокортикостероиды. Доза препаратов и длительность их применения зависят от тяжести заболевания, выраженности воспалительного процесса и срока наступления ремиссии.
Одним из побочных эффектов Циклофосфамида может стать угнетение работы костного мозга с развитием лейкопении (недостатка уровня лейкоцитов). В этом случае препарат могут временно отменить и возобновить лечение через 3–4 недели.
В качестве альтернативы комбинированной терапии Циклофосфамидом и глюкокортикоидами также используют Ритуксимаб — иммуномодулирующее средство из группы моноклональных антител, действие которого направлено против В-лимфоцитов. В норме В-лимфоциты поддерживают адаптивный иммунитет: защищают организм от бактерий, вирусов и т. д. Но если в их работе происходит сбой, они начинают вырабатывать антитела к собственным антигенам. Применение Ритуксимаба приводит к истощению В-лимфоцитов и, соответственно, к подавлению аутоиммунного воспаления [14].
Одним из основных осложнений иммуносупрессивной терапии являются инфекции, так как при таком лечении заметно снижается иммунитет. Поэтому людям, которые проходят эту терапию, показана вакцинация против гриппа, пневмококковой инфекции, COVID-19 и др.
Кроме того, у 1 % таких пациентов может развиться пневмоцистная пневмония, которая является потенциально смертельной [6]. Чтобы не допустить формирование этого заболевания, пациенту назначают Триметоприм в сочетании с Сульфаметоксазол. При возникновении других инфекций проводят соответствующую антибактериальную терапию.
Тяжёлая дыхательная недостаточность может потребовать искусственной вентиляции лёгких.
В случае терминальной почечной недостаточности пациенту показан гемодиализ и трансплантация почки, однако пересадку проводят только после исчезновения анти-БМК антител, т. е. после иммуносупрессивной терапии. При этом синдром Гудпасчера может снова развиться в почечном трансплантате, поэтому пациент с пересаженной почкой должен регулярно проходить осмотры у нефролога и ревматолога, чтобы вовремя выявить рецидив [5][6].
Прогноз. Профилактика
Без лечения синдром Гудпасчера неуклонно прогрессирует. В этом случае прогноз для жизни неблагоприятный: больные умирают от лёгочных кровотечений, тяжёлой почечной или дыхательной недостаточности (продолжительность жизни колеблется от нескольких месяцев до 1–3 лет). При злокачественном течении пациент может умереть в течение нескольких недель. Хотя в литературе описаны случаи спонтанной ремиссии синдрома Гудпасчера, это случается крайне редко [10].
Даже при активной иммуносупрессивной терапии летальность пациентов в остром периоде болезни достигает 10–40 % [4]. Смертность больных младше 18 лет сопоставима с показателями взрослых пациентов и составляет 33,3 % [7].
Неблагоприятными прогностическими факторами являются позднее начало лечения и присоединение инфекции. Если на момент начала лечения человек уже находится на гемодиализе, как правило, восстановить работу почек не удаётся даже при адекватной иммуносупрессивной терапии [3].
После достижения ремиссии заболевание обостряется крайне редко, при этом их исходы более благоприятны, чем в дебюте. Возможно, это связано с тем, что диагноз ставят в более ранние сроки, соответственно, пациент раньше начинает иммуносупрессивную терапию.
Профилактика синдрома Гудпасчера не разработана, так как точная причина его развития неизвестна.
Чтобы снизить риск возникновения лёгочных кровотечений, необходимо отказаться от курения, так как этот симптом чаще всего появляется именно у курильщиков [10].
Список литературы
Тареева И. Е. Нефрология: руководство для врачей. — 2-е издание, переработанное и дополненное. — М.: Медицина, 2000. — 688 с.
Чучалин А. Г. Пульмонология. — М.: ГЭОТАР-Медиа, 2020. — 768 с.
Ассоциация нефрологов России. Диагностика и лечение гломерулонефрита, обусловленного антителами к базальной мембране клубочка: клинические рекомендации. — М., 2021.
Круглякова Л. В. Необычное течение синдрома Гудпасчера у пожилого пациента (случай из практики) // Бюллетень физиологии и патологии дыхания. — 2018. — № 70. — С. 93–97.
Мухин Н. А. Синдром Гудпасчера: патогенез, диагностика и лечение // Фарматека. — 2011. — № 18. — С. 8–14.
Доля Е. М., Паневская Г. Н., Сайтибрагимова Ш. Э. Лечение и диагностика синдрома Гудпасчера: обобщение российских и международных исследований // Медицина. Философия. Социология. Прикладные исследования. — 2023. — № 4. — С. 83–87.
Овсянников Д. Ю., Волков М. Ю., Гитинов Ш. А. и др. Синдром Гудпасчера в детском возрасте: обзор литературы и клиническое наблюдение // Трудный пациент. — 2015. — № 8–9. — С. 45–48.
Патрикеева Ю. М., Лушпаева Ю. А., Евенко А. Ю., Малышева Т. Ю., Биченова А. Г. Синдром Гудпасчера (клиническое наблюдение) // РМЖ. Ревматология. — 2022. — № 22. — С. 75–79.
Авдеев С. Н. Кровохарканье: современные подходы к диагностике и терапии // Атмосфера. Пульмонология и аллергология. — 2010. — № 3. — С. 20–23.
Коломиец В. И., Брежнева Е. Б., Лысогоров Б. Н., Манохина А. Ю. Синдром Гудпасчера // Крымский медицинский журнал. — 2022. — № 4. — С. 68–72.
Бекетова Т. В. Современная классификация системных васкулитов // Терапевтический архив. — 2014. — № 5. — С. 94–98.
Sharma R., Jain S., Kher V. ANCA-associated Goodpasture's syndrome in a patient with rheumatoid arthritis on penicillamine // Indian J Nephrol. — 2012. — № 1. — Р. 45–47. ссылка
Авдеев С. Н. Острая дыхательная недостаточность: основные подходы к диагностике и терапии // Атмосфера. Пульмонология и аллергология. — 2005. — № 4 — С. 25–29.
Насонов Е. Л. Перспективы применения Ритуксимаба при аутоиммунных заболеваниях человека // РМЖ. — 2007. — № 26. — С. 1958.
Tryggvason K., Wartiovaara J. How does the kidney filter plasma? // Physiology (Bethesda). — 2005. — № 2. — Р. 96–101.

