Определение болезни. Причины заболевания
Синдром Эдвардса (Edwards syndrome) — это серьёзное генетическое заболевание, возникающее из-за дополнительной хромосомы. В результате такого нарушения у человека появляются аномалии развития центральной нервной, сердечно-сосудистой, опорно-двигательной и мочеполовой систем. Кроме того, для заболевания характерны маленькие глаза и нижняя челюсть, удлинённый череп, недоразвитые ушные раковины и т. д. Также встречается другое название болезни — трисомия 18 [1].
![Ребёнок с синдромом Эдвардса [21] Ребёнок с синдромом Эдвардса [21]](/media/bolezny/sindrom-edvardsa/rebyonok-s-sindromom-edvardsa-21_s_xaiumHT.jpeg)
Ребёнок с синдромом Эдвардса [21]
Распространённость синдрома Эдвардса
Синдром Эдвардса является второй по распространённости трисомией после синдрома Дауна, при которой возникает дополнительная неполовая хромосома. Он встречается у одного из 6–8 тыс. живорождённых детей. Ещё чаще патология обнаруживается при беременностях, которые заканчиваются выкидышем, — один случай на 2600 зачатий [2][14].
Это заболевание относительно редкое и не зависит от пола, однако мальчики выживают реже. Среди живорождённых синдром Эдвардса встречается в три раза чаще у девочек [14][20].
Для этой болезни характерен высокий уровень смертности (75–95 % в первый год жизни), а также нарушения работы органов и большой риск инфекционных заболеваний у выживших [3].
Факторы риска появления синдрома Эдвардса
Точные причины хромосомного нарушения при синдроме Эдвардса пока не установлены, но известны факторы, повышающие вероятность его развития:
- Возраст матери. Риск возникновения хромосомных аномалий у ребёнка увеличивается с возрастом матери, особенно после 35 лет. Возраст отца влияет в меньшей степени [4][15][17].
- Хромосомные аномалии в семье. Синдром Эдвардса обычно не наследуется, но риск возрастает при наличии хромосомных аномалий в семье, в том числе если у женщины уже есть ребёнок с таким состоянием.
- Болезни матери. На появление хромосомных аномалий могут влиять заболевания беременной (например, сахарный диабет) и воздействие определённых лекарств (например, антибиотиков — Метронидазола, Фуразолидона и др.).
- Факторы окружающей среды. Неблагоприятная среда или воздействие токсинов во время беременности могут влиять на возникновение хромосомных аномалий у ребёнка, однако конкретные связи с синдромом Эдвардса ещё не подтверждены [18][19].
- Чувствительность деления клеток. На процесс разделения хромосом оказывает влияние множество факторов: употребление алкоголя и табакосодержащих продуктов, воздействие радиации и других мутагенов (например тяжёлых металлов, вредных летучих соединений и солей) [6].
Наличие нескольких факторов риска увеличивает вероятность рождения ребёнка с синдромом Эдвардса.
Симптомы синдрома Эдвардса
При этом заболевании наблюдаются разнообразные нарушения:
- Особенности внешнего вида: узкий и удлинённый череп, выступающий затылок, низкий лоб, маленькие глаза и рот, мелкие черты лица. Также встречаются расщелины верхнего нёба и губы, деформация ушей (низкопосажены, несимметричны), складка кожи у внутреннего уголка глаз (эпикантус), короткая шея и маленький вес при рождении.
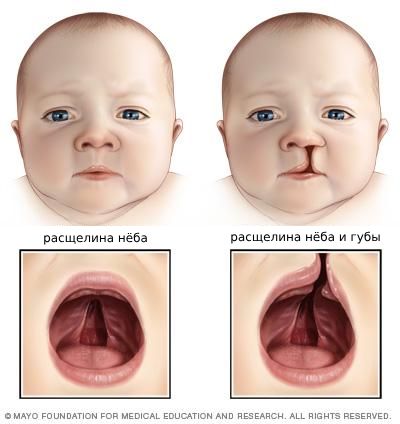
Расщелины верхнего нёба и губы
![Типы эпикантуса [22] Типы эпикантуса [22]](/media/bolezny/sindrom-edvardsa/tipy-epikantusa-22_s.jpeg)
Типы эпикантуса [22]
- Пороки центральной нервной системы: микроцефалия (уменьшенный череп и головной мозг), гидроцефалия, кисты в головном или спинном мозге, спинномозговые грыжи (менингоцеле), отсутствие, недоразвитость или маленький размер мозжечка или мозолистого тела.
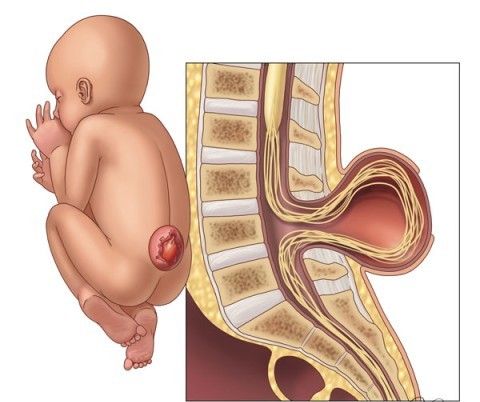
Менингоцеле (спинномозговая грыжа)
- Пороки опорно-двигательного аппарата: скрещённые пальцы на руках, дисплазия бедренных суставов, косолапость, сращённые пальцы на ногах и стопа-качалка.
- Пороки сердечно-сосудистой системы: дефекты межжелудочковой и межпредсердной перегородок сердца, коарктация аорты, аномальный дренаж вен сердца (впадение всех или отдельных лёгочных вен в правое предсердие, венечный синус или полые вены), транспозиция магистральных сосудов и открытый артериальный проток.
- Пороки пищеварительной системы: патологическое сообщение между трахеей и пищеводом (трахеопищеводный свищ), атрезия или эктопия (смещение) ануса, сужение (стеноз) привратника желудка, а также диафрагмальные, пупочные и паховые грыжи.
- Пороки половых органов: у мальчиков — гипоспадия, неопущение яичек; у девочек — двурогая матка, внутриматочная перегородка и чрезмерное увеличение клитора.
- Пороки мочевой системы: гидронефроз и подковообразная почка [10].
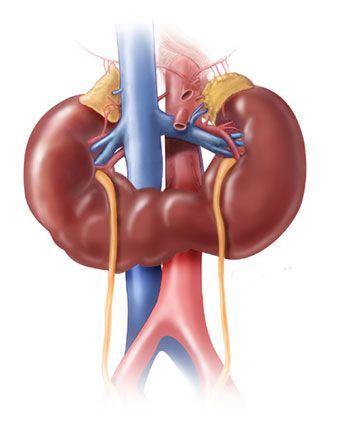
Подковообразная почка
Патогенез синдрома Эдвардса
Развитие синдрома Эдвардса связано с хромосомной аномалией. Она возникает, когда что-то идёт не так во время мейоза — деления родительских клеток, в результате которого образуются гаметы (сперматозоиды и яйцеклетки). Каждая гамета содержит 23 хромосомы, поэтому при их слиянии ребёнок получает ровно 46 хромосом.
Мейоз происходит в два этапа. На первом этапе одна клетка с полным набором хромосом делится пополам. В результате появляются две клетки, каждая из которых содержит по 23 хромосомы, состоящие из двух хроматид. В ходе второго этапа эти клетки делятся ещё раз, а вместе с ними расходятся хроматиды. Итог мейоза — формирование четырёх клеток, которые содержат так же по 23 хромосомы.
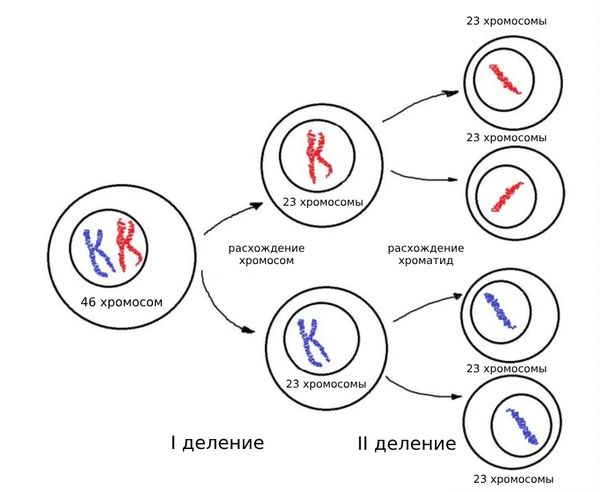
Мейоз
Ошибки деления на втором этапе мейоза обычно не приводят к значительным последствиям, так как они затрагивают хроматиды, а не целые хромосомы [8].
Основную роль в развитии синдрома Эдвардса играет первый этап мейоза, во время которого хромосомы из четырёх хроматид просто не расходятся, из-за чего в новых клетках появляется лишняя хромосома [8]. Поэтому при оплодотворении у ребёнка будет три копии вместо двух.
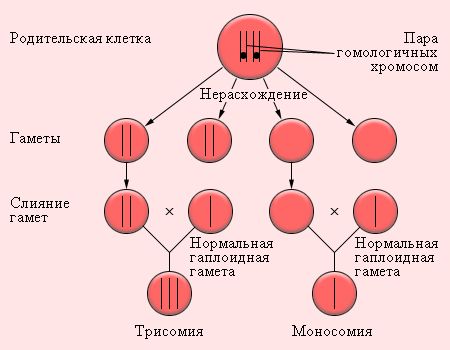
Нерасхождение хромосом
Дополнительная копия хромосомы увеличивает количество генетического материала, что мешает работе клеток и приводит к различным нарушения в развитии эмбриона. Чаще всего такие ошибки происходят именно в яйцеклетках, а не сперматозоидах.
Классификация и стадии развития синдрома Эдвардса
В Международной классификации болезней 10-го пересмотра (МКБ-10) заболевание входит в группу «Врождённые аномалии (пороки развития), деформации и хромосомные нарушения».
В зависимости от тяжести синдрома выделяют:
- Полную трисомию 18. Самая распространённая и тяжёлая форма, которая встречается в 95 % случаев и возникает, когда во всех клетках тела есть полная дополнительная копия хромосомы 18. Большинство детей с такой аномалией умирают в течение первого года жизни [16].
- Частичную трисомию 18. В этом случае дублируется только часть хромосомы 18, поэтому болезнь протекает немного легче: у ребёнка наблюдаются менее выраженные симптомы и пороки развития.
- Мозаичную трисомию 18. При таком варианте дополнительная копия хромосомы присутствует только в некоторых клетках, а в остальных наблюдается нормальное количество хромосом. Если поражена небольшая часть клеток, эта форма протекает легче остальных [7].
В зависимости от того, кто передал аномальную гамету, выделяют синдром Эдвардса, возникший из-за материнских или отцовских нерасхождений.
Осложнения синдрома Эдвардса
Самочувствие пациента зависит от тяжести пороков развития и способности организма поддерживать нормальное состояние, несмотря на эти аномалии.
Врождённые патологии почек могут привести к частым инфекциям мочевой системы, а в дальнейшем — к хронической почечной недостаточности.
Пороки головного мозга и нервной системы часто вызывают гипотонию и снижение двигательной активности, в том числе слабость или паралич рук и ног, из-за чего могут появляться пролежни и застойная пневмония.
Трудности с питанием на фоне пороков мозга или желудочно-кишечного тракта (ЖКТ) часто приводят к попаданию еды или жидкости в дыхательные пути и аспирационной пневмонии.
Из-за нарушений развития пищеварительной системы могут наблюдаться запор и кишечная непроходимость [7].
Диагностика синдрома Эдвардса
Пренатальная диагностика
Обычно первые признаки синдрома Эдвардса можно обнаружить ещё при внутриутробном развитии. Когда женщина становится на учёт по беременности, врач обязательно собирает её анамнез (историю жизни и болезни). В ходе беседы он может задать следующие вопросы:
- Сколько Вам лет?
- Были ли в семье случаи хромосомных заболеваний (например, синдром Дауна)? Есть ли у Вас дети с хромосомными аномалиями или врождёнными дефектами?
- Сколько было беременностей, родов, выкидышей или абортов?
- Есть ли у Вас вредные привычки (курение, употребление алкоголя или наркотиков)?
- Есть ли у Вас хронические заболевания и какие?
- Подвергались ли Вы воздействию вредных факторов на работе или дома?
Если пациентка входит в группу риска, ей проводят комбинированный скрининг, который включает:
- Анализ анамнестических данных. Большое значение имеет возраст матери и способ зачатия (естественное или с помощью репродуктивных технологий).
- Анализ биохимических маркеров в сыворотке крови. В первую очередь исследуют ассоциированный с беременностью протеин А (PAPP-A) и бета-субъединицу гормона хорионического гонадотропина человека (β-ХГЧ). Эти анализы проводят на 11–13-й неделе беременности. Они помогают оценить риск хромосомных аномалий, включая синдром Эдвардса, но интерпретировать результаты можно только вместе с остальными методами диагностики.
- Ультразвуковое исследование (УЗИ). Оно позволяет определить толщину воротникового пространства у плода, оценить кровоток в венозном протоке и обнаружить недостаточность трёхстворчатого клапана.
Такой подход позволяет выявить до 95 % случаев синдрома Эдвардса. Однако, если учитывать только возраст матери и толщину воротникового пространства, точность диагностики снижается до 83 % [11].
В конце второго триместра рекомендован скрининг с определением альфафетопротеина (АФП), β-ХГЧ и свободного эстриола (Е3).
В зависимости от ситуации синдром Эдвардса могут обнаружить как на 1-м, так и на 2-м триместре. После этого беременную направляют к генетику, который назначает инвазивную диагностику. Под контролем УЗИ пациентке делают пункцию (прокалывание) плаценты, чтобы взять кусочек ткани хориона (зародышевой оболочки), небольшое количество амниотической жидкости (околоплодных вод) и пуповинной крови. Полученные материалы используют для проведения кариотипирования (хромосомного анализа).

Забор околоплодных вод
Дополнительно могут назначить хромосомный микроматричный анализ (ХМА). Он способен обнаружить очень маленькие генетические изменения, которые незаметны при стандартном кариотипировании [12]. ХМА проводят, если есть клинические проявления синдрома, но нет изменений в кариотипе.
Учитывая полученные результаты, врач определяет возможный прогноз и объясняет, какой уход и лечение может потребоваться ребёнку после рождения. Решение об аборте родители принимают совместно с доктором, ведущим беременность, так как каждый случай индивидуален.
Диагностика после рождения
Послеродовую диагностику проводят, если синдром Эдвардса не выявили ранее. Такое обследование позволяет оценить тяжесть пороков развития и составить возможный план лечения и ухода за ребёнком.
Диагностика включает:
- клинический осмотр;
- генетическое тестирование;
- дополнительные исследования;
- оценку функциональных нарушений.
При осмотре ребёнка с трисомией 18 врачи обращают внимание на низкий вес и характерные физические аномалии, которые обычно заметны сразу после рождения. Для подтверждения диагноза обязательно проводят кариотипирование. С его помощью также можно определить пол ребёнка, когда он неочевиден из-за особенностей развития половой системы. Это облегчает составление плана дальнейшего лечения.
В зависимости от клинической картины к диагностике привлекают смежных специалистов, например кардиолога, уролога, ортопеда, хирурга и др. После первичного осмотра они могут направить пациента на УЗИ, магнитно-резонансную томографию (МРТ) и компьютерную томографию (КТ) для углублённого исследования. Также могут понадобиться дополнительные обследования: эхокардиография (ЭхоКГ), чтобы изучить состояние сердца, рентген костей, анализы для проверки работы почек и пищеварительной системы.
Кроме того, важно оценить неврологический статус ребёнка, в том числе проверить, есть ли у него признаки задержки в развитии и трудности с координацией (для этого наблюдают за моторными навыками, зрительным и слуховым восприятием, интеллектуальным развитием и игровой деятельностью).
Лечение синдрома Эдвардса
Лечения, которое может устранить причину болезни, не существует, поэтому врач назначает симптоматическую терапию, направленную на облегчение состояния ребёнка и устранение пороков развития [10].
Пациенту присваивают инвалидность в соответствии с диагнозом. При необходимости родители также могут оформить паллиативный статус, который обеспечивает ребёнку с неизлечимым заболеванием доступ к медицинской помощи, направленной на улучшение качества жизни, включая бесплатные лекарства и специальное оборудование.
Основные принципы лечения и ухода за пациентом:
- Оперирование имеющихся пороков сердца, кишечника, рук и ног.
- Использование специализированных сосок или кормление с помощью зонда. Эти меры предназначены для детей, у которых есть трудности с питанием из-за различных анатомических особенностей, однако они не могут полностью избавить от проблемы. Если есть возможность, необходимо провести операцию.
- Введение в рацион ребёнка высококалорийных и белковых смесей, которые ускорят набор веса. По возможности следует кормить малыша грудным молоком (при необходимости можно сцеживать), так как оно укрепляет иммунитет.
- Наблюдение у невролога для ранней терапии неврологического дефицита.
- Обучение родителей уходу за ребёнком-инвалидом и наблюдение у врачей паллиативной помощи.
- Проведение реабилитационных мероприятий, направленных на восстановление или улучшение речи, коммуникации и других когнитивных или поведенческих навыков у ребёнка.
- Вакцинирование по возрастному графику, если нет показаний для медотвода.
Важным аспектом является психологическая поддержка семей, в которых родился ребёнок с хромосомной аномалией. Такая помощь помогает родственникам принимать сложные решения, связанные с лечением, а также снижают эмоциональный стресс, вызванный поставленным диагнозом.
Прогноз. Профилактика
Из-за тяжести заболевания прогноз обычно неблагоприятный. Младенческая летальность при синдроме Эдвардса крайне высокая, особенно среди мальчиков. До года доживает около 10 % пациентов. При мозаичной форме заболевания продолжительность жизни обычно выше, но даже в этом случае у детей отмечается сильная задержка моторного и физического развития [10].
Профилактика синдрома Эдвардса
Чтобы предупредить заболевание, необходимо снизить влияние факторов риска на организм женщины, особенно в первые недели беременности. Если женщина решает рожать ребёнка после 35 лет, ей следует пройти углублённый скрининг и более тщательное наблюдение у гинеколога.
Наличие в анамнезе выкидыша на ранних сроках или рождение ребёнка с множественными пороками развития или синдромом Эдвардса является показанием для предродового консультирования при планировании новой беременности. Оно позволяет оценить риски повторных аномалий и, при возможности, рассмотреть вариант искусственного оплодотворения (ЭКО) с преимплантационной диагностикой [13].
Список литературы
Байрамова Л. В., Вердиева Г. М., Заклицкая Е. Ю., Валуев С. А. и др. Клинический случай пациента с синдромом Эдвардса // Российский педиатрический журнал. — 2019. — № 5. — С. 310.
Saldarriaga W., Rengifo-Miranda H., Ramírez-Cheyne J. Síndrome de trisomía 18. Reporte de un caso clínico [Trisomy 18 syndrome: A case report] // Rev Chil Pediatr. — 2016. — № 2. — Р. 129–136.ссылка
Kepple J. W., Fishler K. P., Peeples E. S. Surveillance guidelines for children with trisomy 18 // Am J Med Genet A. — 2021. — № 4. — Р. 1294–1303.ссылка
Краснов М. В., Кириллов А. Г., Краснов В. М., Саваскина Е. Н. и др. Наследственные болезни у детей // Практическая медицина. — 2009. — № 39. — С. 22–30.
Томарева Е. И., Меладзе Р. Д., Евдокимова Д. В. Факторы риска патологического кариотипа плода // Вестник новых медицинских технологий. — 2017. — № 2. — С. 206–211.
Юров И. Ю., Ворсанова С. Г., Зеленова М. А., Юров Ю. Б. Анеуплоидия хромосомы 21 при заболеваниях головного мозга // Фундаментальные исследования. — 2015. — № 7. — С. 61–70.
Лепесова М. М., Отегенова Д. Т., Курмантай A. M. Редкий нетипичный случай синдрома Эдвардса // Вестник АГИУВ. — 2016. — № 2. — С. 25–28.
Седова А. О., Мартемьянова А. И., Черных В. Б. Анеуплодия в сперматозоидах у фертильных мужчин и пациентов с нарушением репродукции // Андрология и генитальная хирургия. — 2021. — № 4. — С. 27–33.
Wolstenholme J., Angell R. Maternal age and trisomy — a unifying mechanism of formation // Chromosoma. — 2000. — № 7. — Р. 435–438.ссылка
Захарова Е. С., Ларикова А. Д. Синдром Эдвардса как проявление генетического заболевания в педиатрической практике (клинический случай) // Вестник новых медицинских технологий. — 2018. — № 2. — С. 17–20.
Цибизова В. И. Значимость биохимических маркеров в прогнозе перинатальных исходов при многоплодной беременности: дис. ... д-ра мед. наук: 14.01.01. — М., 2020. — 107 с.
Levy B., Wapner R. Prenatal diagnosis by chromosomal microarray analysis // Fertil Steril. — 2018. — № 2. — Р. 201–212.ссылка
Коротченко О. Е., Сыркашева А. Г., Калинина Е. А. Преимплантационный генетический скрининг у пациенток с привычным выкидышем: факторы риска анеуплоидии эмбрионов // Акушерство и гинекология: Новости. Мнения. Обучения. — 2017. — № 18. — С. 48–53.
Cereda A., Carey J. C. The trisomy 18 syndrome // Orphanet J Rare Dis. — 2012. — Vol. 7. — P. 81.ссылка
Демикова Н. С., Подольная М. А., Лапина А. С. Возраст матери как фактор риска врождённых пороков развития // Российский вестник перинатологии и педиатрии. — 2020. — № 2. — С. 34–39.
Balasundaram P., Avulakunta I. D. Edwards Syndrome // Treasure Island. — 2025.ссылка
Jónsson H., Sulem P., Kehr B., Kristmundsdottir S. et al. Parental influence on human germline de novo mutations in 1,548 trios from Iceland // Nature. — 2017. — № 7673. — Р. 519–522.ссылка
Чшиева Ф. Т. Пространственно-временной цитогенетический мониторинг подверженного техногенной нагрузке населения Северной Осетии: дис. ... д-ра мед. наук: 03.02.07. — М., 2018. — 236 с.
Kinnunen J., Nikkinen H., Keikkala E., Mustaniemi S. et al. Gestational diabetes is associated with the risk of offspring’s congenital anomalies: a register-based cohort study // BMC Pregnancy Childbirth. — 2023. — № 1. — P. 708.ссылка
Чистый А. Г. Хромосомные болезни: учебно-методическое пособие. — Минск: БГМУ, 2023. — 24 с.
Maebh // Same but Different. [Электронный ресурс]. Дата обращения: 08.07.2025.
Shin D. H., Woo K. I., Kim Y. D. Relationship between lower eyelid epiblepharon and epicanthus in Korean children // PLOS One. — 2017. — № 11. — Р. e0187690.ссылка

