Определение болезни. Причины заболевания
Гемохроматоз (Hemochromatosis) — это заболевание, при котором в организме избыточно откладывается железо. В результате нарушается работа печени, поджелудочной и щитовидной железы, сердца, половых желёз, гипофиза, повреждаются суставы и кожа.
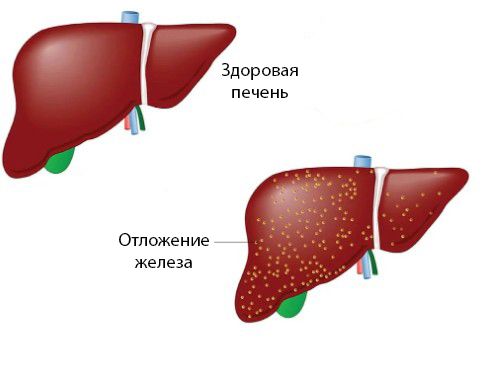
Печень в норме и при гемохроматозе
Гемохроматоз называют «бронзовым диабетом», потому что у пациентов изменяется цвет кожи и нарушается работа поджелудочной железы. Потемнение кожи связано с отложением в ней меланина и солей железа.
Выделяют наследственную и вторичную форму болезни.
Наследственный гемохроматоз — это наиболее распространённое аутосомно-рецессивное заболевание (ребёнок заболеет, если получит по одной копии дефектного гена от каждого родителя) у европеоидов, выявляемое у 1 из 300–500 человек [1]. Гемохроматоз 2, 3 и 4-го типов встречается во всём мире, а 1-й тип в основном наблюдается у людей североевропейского происхождения [2].
Статистики по наследственному гемохроматозу в Российской Федерации нет, однако известно, что приблизительно у 16 % населения есть мутации в генах обмена железа [28]. Мужчины страдают гемохроматозом примерно в 2–3 раза чаще, чем женщины [1]. Причём у женщин симптомы появляются позже — в основном это связано с менструальным циклом: каждый месяц организм теряет кровь и начинает вырабатывать новые эритроциты, что увеличивает потребность в железе [3]. Так, у мужчин заболевание обычно проявляется после 50 лет, а у женщин — после 60.
Другой вариант наследственного гемохроматоза — ювенильный, который может проявиться в возрасте от 10 до 30 лет. Эта форма перегрузки железом отличается генами, в которых возникли мутации. К ней приводят поломки в генах гемоювелина (HJV, тип 2A), гепсидина (HAMP, тип 2B), трансферринового рецептора 2 (TFR2, тип 3), ферропортина (SLC40A1 или FPN1, тип 4). Эти варианты встречаются крайне редко, в литературе описаны единичные случаи [20].
Вторичный гемохроматоз возникает из-за нарушений в работе красного костного мозга и при переливаниях крови. К такой форме заболевания может могут приводить различные анемии (в частности серповидно-клеточная, Х-сцепленная сидеробластная, талассемия), а также наследственный сфероцитоз и дефицит пируваткиназы. Но в большинстве своём вторичные перегрузки железом носят ятрогенный характер, т. е. вызваны неадекватным лечением или применением высоких доз препаратов железа. Спровоцировать накопление железа можно, употребляя без назначения врача БАДы или препараты, содержащие это вещество.
Также существуют заболевания печени, при которых может развиться вторичная перегрузка железом, например алкогольная жировая болезнь печени, метаболически ассоциированная жировая болезнь печени и хронические гепатиты [21][22][23][24].
Симптомы гемохроматоза
Клинические признаки болезни зависят от того, какая система органов наиболее поражена. Зачастую заболевание протекает бессимптомно до зрелого возраста. Часто диагноз не ставится до тех пор, пока не будут выявлены поражения нескольких систем. Симптомы зависят от поражённого органа, но почти все пациенты жалуются на сильную усталость, вялость, иногда на боли в суставах. Как правило, проявления болезни возникают в течение десяти лет до постановки диагноза.
Поздние симптомы возникают, когда железо начинает откладываться в тканях, ниже представлены некоторые из таких проявлений:
- Потемнение кожи до бронзового цвета. Наблюдается более чем у 90 % пациентов с наследственным гемохроматозом и является одним из самых ранних проявлений заболевания. Этот симптом более заметен на участках кожи, подвергающихся воздействию солнца. Потемнение кожи связано с тяжёлым течением заболевания и входит в триаду чрезмерного накопления железа в организме (более 20 г), куда также относится цирроз и сахарный диабет.
- Нарушение работы печени. Встречается у 75 % пациентов. При этом желтуха в начале заболевания обычно не возникает. Поражение печени может проявляться увеличением её размеров, болью в животе или изменениями в биохимическом анализе крови: повышением АСТ и АЛТ.
- Койлонихия — ложкообразные или вдавленные ногти, чаще на большом и указательном пальце. Наблюдается у 50 % пациентов, у 25 % — на всех ногтях.
![Койлонихия [44] Койлонихия [44]](/media/bolezny/gemohromatoz/koylonihiya-44_s.jpeg)
Койлонихия [44]
- Изменения формы и подвижности суставов. Возникает из-за отложения в них пирофосфата кальция (псевдоподагра). Может проявляться болями в суставах, припухлостью и узелками, обычно на пальцах рук. Также часто вовлекаются колени, запястья, бёдра, спина, шея и стопы.
- Эндокринная дисфункция. Заболевание может приводить к развитию сахарного диабета, снижению либидо и импотенции у мужчин, нарушениям менструального цикла у женщин, ухудшению работы щитовидной железы и надпочечников, дефектам паращитовидных желёз и остеопорозу [4]. Увеличение размеров или изменение формы молочной железы (гинекомастия), а также снижение оволосения тела могут быть вторичными признаками, т. е. следствием осложнений гемохроматоза. Частичная потеря волос на теле наблюдается у 60 % пациентов, а полная — у 12 %. Чаще всего поражается лобковая область [1].
Патогенез гемохроматоза
В норме усвоение железа жёстко регулируется организмом, поскольку он не способен выводить его избыток.
Наиболее частой причиной гемохроматоза является поломки в генах, ответственных за регуляцию обмена железа в организме. Это состояние называют первичным, или наследственным, гемохроматозом. Наследственный гемохроматоз 1-го типа возникает у людей с мутацией в гене HFE, что приводит к повышенному всасыванию железа, несмотря на нормальное потребление с пищей. Белок HFE, кодируемый этим геном, регулирует выработку гепсидина, который вырабатывается печенью и определяет, сколько железа усваивается из рациона и сколько высвобождается из мест хранения в организме [5].
Нормальная функция HFE, по-видимому, заключается в контроле поглощения железа клетками через взаимодействие с рецепторами трансферрина.
У гомозигот, т. е. для людей с двумя мутациями гена HFE, более высокие шансы развития заболевания. Помимо этого, у них повышен риск развития диабета из-за неизвестных механизмов.
Носители мутантного гена, или гетерозиготы (когда только один из пары генов содержит поломку), могут иметь отклонения в анализах по метаболизму железа, но перегрузка у них не возникает [6][7][8]. Если только у одного из родителей есть мутации в генах обмена железа, то риск, что у ребёнка разовьётся заболевание, практически нулевой [8][9].
Наиболее сильно при гемохроматозе страдает печень и поджелудочная железа. В печени происходит 90 % всех процессов обмена веществ, накопление соединений железа нарушает работу клеток и вызывает их гибель, что приводит к развитию цирроза. Поджелудочная железа из-за своей близости к печени тоже начинает накапливать ионы железа, что вызывает поражение островков Лангерганса. Островки содержат клетки, вырабатывающие инсулин и глюкагон — гормоны углеводного обмена. Когда эти клетки погибают или перестают выполнять свою функцию, развивается сахарный диабет.
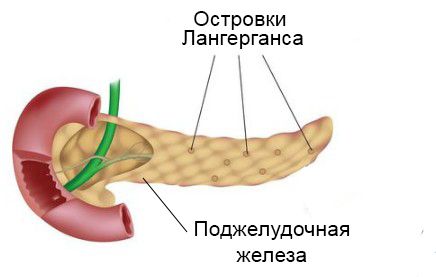
Островки Лангерганса
Остальные симптомы заболевания появляются из-за отложения в органах и тканях соединений железа, однако точные механизмы развития пока не описаны.
Причины вторичного гемохроматоза связаны с избыточным разрушением эритроцитов, в результате чего в тканях откладывается железо (эритропоэтический гемохроматоз). Часто это происходит в результате патологии эритроцитов, которая приводит к их повышенной хрупкости и, следовательно, к сокращению продолжительности жизни этих клеток. Когда клетки разрушаются, железо из них откладывается в тканях. Тот же механизм действует у пациентов, получающих многократные переливания эритроцитов. Другие, менее распространённые заболевания, такие как кутаиновая порфирия, также могут вызывать перегрузку железом. Эритропоэтический гемохроматоз зависит от распространённости основного заболевания (например, талассемии, сфероцитоза) и встречается не только у европеоидов, но и у представителей других рас.
Чрезмерное потребление железа также может вызвать гемохроматоз. Исторически это происходило из-за употребления пива, приготовленного в стальных бочках. Кроме того, передозировка железа может быть результатом употребления некоторых безрецептурных препаратов или пищевых добавок [10].
Классификация и стадии развития гемохроматоза
Заболевание, как уже было сказано выше, бывает наследственным и приобретённым.
Наследственный гемохроматоз подразделяется на 5 подтипов:
- Тип 1 — нарушения в гене белка HFE, порядка 90 % случаев от всех случаев первичного гемохроматоза [1].
- Тип 2 (ювенильный гемохроматоз). Возникает в детстве или молодом возрасте, обычно до 30 лет. Включает два генетических варианта:
- Тип 2А — мутации в гене гемоювелина (HJV), ответственном за продукцию и работу гепсидина. Встречается среди потомков жителей региона Сагеней-Лак-Сен-Жан, региона Франции [29][30]. У больных часто увеличивается сердце (кардиомиопатия), снижается толерантность к глюкозе и наблюдается недоразвитие половых желёз (гипогонадизм), а не тяжёлые заболевания печени [31][32]. Обычно болезнь диагностируется на поздних стадиях и плохо поддаётся лечению из-за обширного поражения органов и систем.
- Тип 2B — мутации в гене гепсидина (HAMP), при которых снижается его выработка, в результате становится невозможно транспортировать железо из тканей организма. Встречается среди итальянцев, греков и португальцев, а также у азиатов, среди которых распространены близкородственные браки [33][34][35].
- Тип 3 — мутации в гене трансферринового рецептора 2 (TFR2), связанные с нарушением восприятия уровня железа в крови и процессами синтеза новых клеток крови. По серьёзности симптомов эта форма находится между 1 и 2-м типом. Встречается среди итальянцев, французов, испанцев, португальцев и японцев [36].
- Тип 4 (ферропортиновая болезнь) — мутации в гене ферропортина (SLC40A1; FPN1), крайне редкая аутосомно-доминантная форма гемохроматоза (достаточно мутантного гена у одного из родителей), встречающаяся среди жителей Африки и материкового Китая [37].
Сравнительно недавно, в 2022 году, выделили новый тип наследственного гемохроматоза — PIGA. Доказано, что он является X-сцеплённым рецессивным заболеванием (т. е. повреждённый ген находится на половой Х-хромосоме и передаётся вместе с ней), поражающим преимущественно мальчиков. Особенностью этой формы является присоединение к признакам перегрузки железом тяжёлых неврологических отклонений: ранней эпилепсии, выраженной задержки развития и умственной отсталости [38].
Степень перегрузки железом определяется лабораторными и инструментальными методами, данные представлены в таблице [12].
Осложнения гемохроматоза
Без лечения гемохроматоз приводит к гибели клеток печени, в результате чего ткани этого органа замещаются на фибрин. Степень фиброза связана с прогрессированием болезни в необратимую фазу цирроза — тяжёлого состояния, при котором работа клеток печени максимально нарушается [1][11][13]. Наиболее опасно перерождение цирроза в рак, однако при гемохроматозе это случается крайне редко [1][13].
Вторым по значимости местом отложения железа в организме является сердце. Нередко у пациентов с гемохроматозом диагностируются такие осложнения, как дилятационная кардиомиопатия, хроническая сердечная недостаточность, различного рода аритмии и другие нарушения проводимости [39].
Кроме того, около половины пациентов с наследственным гемохроматозом страдают сахарным диабетом 2-го типа [40].
Также гемохромтаоз может влиять на работу половых гормонов. У женщин может нарушаться менструальный цикл, но это встречается гораздо реже, чем гипогонадизм у мужчин [41]. Так, среди пациентов с гомозиготным гемохроматозом ни у одной из женщин не было потери либидо или ранней менопаузы, в то время как у 24 % мужчин наблюдалось низкое либидо [42]. Гипогонадизм, в свою очередь, может способствовать низкой плотности костей и развитию остеопороза [19].
Диагностика гемохроматоза
Первичную диагностику гемохроматоза может проводить врач-терапевт или врач общей практики (семейный врач). При необходимости пациента направляют к гастроэнтерологу для дальнейшего обследования, наблюдения и подбора оптимального лечения. В отдельных случаях гемохроматоз может вести врач-гематолог.
Также при наличии у пациента отклонений со стороны сердечно-сосудистой, репродуктивной и эндокринной системы могут потребоваться дополнительные исследования и консультации узких специалистов: кардиолога и эндокринолога [11].
Сбор анамнеза и осмотр
Для диагностики гемохроматоза врач проведёт тщательный сбор жалоб и анамнеза (истории) заболевания. Во время консультации необходимо рассказать доктору:
- об эпизодах переливания крови;
- применении препаратов железа;
- наличии заболеваний крови, связанных с избыточным разрушением эритроцитов (талассемии, наследственного сфероцитоза, серповидно-клеточной анемии, антифосфолипидного синдрома и др.);
- наличии у кровных родственников наследственных или гематологических заболеваний [1][11].
Во время осмотра врач изучит цвет и влажность кожи, состояние ногтей и волос; проведёт осмотр органов брюшной полости: оценит состояние печени, её размеры. Дополнительно может потребоваться измерение общих показателей здоровья: температуры, пульса, артериального давления и насыщения крови кислородом.
Лабораторная диагностика
При подозрении на перегрузку железа врач назначит следующие анализы:
1. Общий клинический анализ крови: чтобы оценить состояние системы крови и исключить воспалительные заболевания.
2. Биохимический анализ крови:
- АСТ и АЛТ — по ним оценивают состояние печени и могут изменить тактику лечения;
- показатели обмена железа — уровень железа в сыворотке крови, ферритин и трансферрин (эти три показателя наиболее важны для постановки диагноза, так как от них будет зависеть назначение генетического обследования) [11].
При гемохроматозе уровень железа в сыворотке будет повышаться, а трансферрин снижаться, причём по отдельности эти показатели не позволяют поставить диагноз [11].
Наиболее чувствительными будут показатели ферритина — он повышается более 200 мкг/л у женщин и более 300 мкг/л у мужчин [1][11][13].
Вторым по значимости будет показатель степени насыщения трансферрина, который измеряется в процентах. Этот показатель рассчитывается по данным об уровне железа в сыворотке и трансферрина. При насыщении более 45 % у женщин и более 50 % у мужчин можно заподозрить перегрузку железом [1][11][13].
3. Генетическое исследование — назначается только в двух случаях:
- при выявлении у детей мутаций в генах HFE — рекомендовано пройти генетический тест родителям;
- европеоидам с высоким уровнем ферритина и коэффициента насыщения трансферрина [11].
Инструментальная диагностика
Чтобы оценить объём перегрузки железом, проводится:
- МРТ печени по специальной программе T2 и R2 (FerriScan) [25][26][27]. Это безопасный и безболезненный метод, но в России он применяется нечасто [27].
- Биопсия печени под контролем УЗИ. Это стандарт для определения степени перегрузки железом (специфической окраски на железо по Перлсу). Проводится строго по показаниям при повышении уровня ферритина более 1000 мкг/л или признаках активации ферментов печени [1][11].
Из дополнительных обследований может проводиться эластометрия печени, позволяющая определить степень фиброза и выбрать тактику лечения [11][13]. Это безопасное исследование, по степени вмешательства равноценное обычному УЗИ брюшной полости (обычное УЗИ помогает выявить увеличение печени и возможные изменения паренхимы — её ткани, но в остальном неинформативно при гемохроматозе).

Эластометрия печени
Дифференциальная диагностика
При гемохроматозе поражаются многочисленные системы органов, поэтому его нужно отличать от большого количества заболеваний, таких как:
- перегрузка железом в результате частых переливаний крови;
- гепатиты В и С;
- метаболически ассоциированная жировая болезнь печени (МАЖБП);
- чрезмерное потребление железа;
- дисметаболическая гиперферритинемия;
- наследственная ацерулоплазминемия;
- алкогольная болезнь печени;
- кутаиновая порфирия Тарда;
- гиперплазия костного мозга;
- гемолитическая анемия;
- билиарный цирроз [1].
Лечение гемохроматоза
К терапии первой линии относится флеботомия — кровопускание с утилизацией крови, которое проводится под контролем врача. В результате удаляются кровяные клетки и организм начинает вырабатывать новые эритроциты, расходуя избыточные запасы железа. Вначале кровопускание проводят раз в 1–2 недели до достижения уровня ферритина не менее 50 нг/мл. Далее требуется от 2 до 6 процедур в год [11].
Перед флеботомией оценивают уровень гемоглобина в крови, поскольку эта процедура противопоказана при показателях менее 110 г/л (при гемоглобине < 120 г/л нужно уменьшить количество кровопусканий, при < 110 г/л — прекратить на время процедуры) [11] . Ферритин и трансферрин оценивают раз в 6 месяцев — это позволяет определить, когда нужно провести кровопускание повторно.
Пациенты без осложнений и опасных инфекций, таких как гепатиты В и С, могут контролировать уровень ферритина с помощью донорства крови [11]. Если нет противопоказаний, её можно сдавать не чаще, чем 4 раза в год женщинам и 5 раз в год мужчинам.
Альтернативой флеботомии является эритроцитаферез — аналогичный процесс, при котором из кровотока удаляют исключительно красные кровяные клетки. Такая процедура менее эффективна, чем флеботомия, но легче переносится и требует меньше сеансов.
Если есть противопоказания к флеботомии или эритроцитоферезу, врач назначит вторую линию терапии — хелаторы железа.
Доступно два вида препаратов:
- Для приёма внутрь: Деферазирокс и Деферипрон. В России зарегистрирован и доступен к продаже только первый [14]. Препараты действуют в печени, связывая избыточное железо и выводя его с желчью. Побочные эффекты включают головную боль, тошноту, рвоту, диарею, запоры, нарушение работы почек (появление белка в моче, снижение фильтрационной функции почек). Препараты противопоказаны во время беременности [15][16].
- Для введения внутривенно: Дефероксамин. Этот препарат образует комплексные соединения с железом в плазме крови, которые в дальнейшем выводятся с мочой. Дефероксамин вводят длительно, в течение 8–24 часов (обычно, если человек ходит, то используются передвижные аппараты, однако чаще этот препарат применяют в отделениях реанимации при крайне тяжёлых перегрузках железа), что значительно снижает качество жизни пациентов [12]. Среди побочных эффектов выделяют головную боль, тошноту, боли в суставах и мышцах, повышение температуры тела и боли в месте инъекции. В России у препарата срок регистрации закончился в 2018 году и более он на рынок не выходил [17].
При уровне ферритина 1000–2500 мкг/л рекомендовано применять пероральные препараты с коррекцией дозы каждые 3–6 месяцев. При тяжёлой перегрузке железом начинают с внутривенного введения препаратов, а затем переходят на пероральные формы.
Питание при гемохроматозе
Рекомендуется ограничить приём препаратов железа и других железосодержащих добавок, избегать приёма витамина C (поскольку он увеличивает всасывание железа в двенадцатиперстной кишке), а также не более 2–3 раз в неделю есть красное мясо (говядину, свинину, баранину, конину, оленину, бедро курицы и индейки). Также не рекомендуется употреблять термически необработанные морепродукты, так как большинство морских обитателей накапливают различные минералы. Дополнительно рекомендуется полностью отказаться от алкоголя и алкогольсодержащих напитков.
Прогноз. Профилактика
Благодаря достижениям в диагностике и лечении этого заболевания, за последние несколько десятилетий прогноз улучшился. Ранняя диагностика и адекватное лечение могут уменьшить большинство осложнений. Но, если гемохроматоз не лечить, он может привести к необратимому повреждению печени и вызвать цирроз, гепатоцеллюлярную карциному и другие осложнения, связанные с перегрузкой тканей и органов железом [18].
Профилактика наследственного гемохроматоза невозможна из-за того, что это генетическое заболевание. Чтобы не допустить осложнений и своевременно начать лечение у пациентов с патологией, требующей частых переливаний крови, а также у людей, длительно получающих препараты железа, нужно контролировать показатели обмена железа.
Пациентам, у которых симптомы заболевания отсутствуют, но известно о генетической поломке, требуется ежегодно отслеживать уровень ферритина, степень насыщения трансферрина, АСТ и АЛТ [7][11].
Список литературы
Porter J. L., Rawla P. Hemochromatosis // StatPearls Publishing. — 2024. ссылка
Olynyk J. K., Cullen D. J., Aquilia S. et al. A population-based study of the clinical expression of the hemochromatosis gene // N Engl J Med. — 1999. — № 10. — Р. 718–724. ссылка
Moirand R., Adams P. C., Bicheler V. et al. Clinical features of genetic hemochromatosis in women compared with men // Ann Intern Med. — 1997. — № 2. — Р. 105–110. ссылка
Raju K., Venkataramappa S. M. Primary Hemochromatosis Presenting as Type 2 Diabetes Mellitus: A Case Report with Review of Literature // Int J Appl Basic Med Res. — 2018. — № 1. — Р. 57–60. ссылка
Means R. T. Jr. Hepcidin and iron regulation in health and disease // Am J Med Sci. — 2013. — № 1. — Р. 57–60. ссылка
Cheng R., Barton J. C., Morrison E. D. et al. Differences in hepatic phenotype between hemochromatosis patients with HFE C282Y homozygosity and other HFE genotypes // J Clin Gastroenterol. — 2009. — № 6. — Р. 569–573.ссылка
Bulaj Z. J., Griffen L. M., Jorde L. B. et al. Clinical and biochemical abnormalities in people heterozygous for hemochromatosis // N Engl J Med. — 1996. — № 24. — Р. 1799–1805. ссылка
Bacon B. R., Olynyk J. K., Brunt E. M. et al. HFE genotype in patients with hemochromatosis and other liver diseases // Ann Intern Med. — 1999. — № 12. — Р. 953–962.ссылка
Barton J. C., Acton R. T. Diabetes in HFE Hemochromatosis // J Diabetes Res. — 2017. ссылка
Pietrangelo A. Hereditary hemochromatosis: pathogenesis, diagnosis, and treatment // Gastroenterology. — 2010. — № 2. — P. 393–408. ссылка
European Association for the Study of the Liver. EASL Clinical Practice Guidelines on haemochromatosis // J Hepatol. — 2022. — № 2. — Р. 479–502. ссылка
Сметанина Н. С. Современные возможности хелаторной терапии // Российский журнал детской гематологии и онкологии. — 2014. — № 1. — С. 51–61.
Mehta K. J., Farnaud S. J., Sharp P. A. Iron and liver fibrosis: Mechanistic and clinical aspects // World J Gastroenterol. — 2019. — № 5. — Р. 521–538. ссылка
Министерство здравоохранения РФ. Государственный реестр лекарственных средств. Деферазирокс. [Электронный ресурс]. Дата обращения: 20.02.2024.
Deferasirox Pregnancy and Breastfeeding Warnings // Drugs.com. — 2023.
Deferiprone Pregnancy and Breastfeeding Warnings // Drugs.com. — 2023.
Министерство здравоохранения РФ. Государственный реестр лекарственных средств. Дефероксамин. [Электронный ресурс]. Дата обращения: 20.02.2024.
Rawla P., Sunkara T., Muralidharan P., Raj J. P. Update in global trends and aetiology of hepatocellular carcinoma // Contemp Oncol (Pozn). — 2018. — № 3. — Р. 141–150. ссылка
Angelopoulos N. G., Goula A. K., Papanikolaou G., Tolis G. Osteoporosis in HFE2 juvenile hemochromatosis. A case report and review of the literature // Osteoporos Int. — 2006. — № 1. — Р. 150–155.ссылка
Mantilla-Hernández J. C., Amaya-Mujica J. Juvenile hemochromatosis with multi-organ involvement diagnosed at autopsy // Rev Esp Patol. — 2019. — № 1. — Р. 45–49. ссылка
Wood M. J., Powell L. W., Dixon J. L., Ramm G. A. Clinical cofactors and hepatic fibrosis in hereditary hemochromatosis: the role of diabetes mellitus // Hepatology. — 2012. — № 3. — Р. 904–911.ссылка
Irving M. G., Halliday J. W., Powell L. W. Association between alcoholism and increased hepatic iron stores // Alcohol Clin Exp Res. — 1988. — № 1. — Р. 7–13. ссылка
Diwakaran H. H., Befeler A. S., Britton R. S. et al. Accelerated hepatic fibrosis in patients with combined hereditary hemochromatosis and chronic hepatitis C infection // J Hepatol. — 2002. — № 5. — Р. 687–691. ссылка
Thorburn D., Curry G., Spooner R. et al. The role of iron and haemochromatosis gene mutations in the progression of liver disease in chronic hepatitis C // Gut. — 2002. — № 2. — Р. 248–252.ссылка
Hernando D., Zhao R., Yuan Q. et al. Multicenter Reproducibility of Liver Iron Quantification with 1.5-T and 3.0-T MRI // Radiology. — 2023. — № 2. ссылка
Wood J. C. Estimating tissue iron burden: current status and future prospects // Br J Haematol. — 2015. — № 1. — Р. 15–28.ссылка
Назарова Э. Э., Куприянов Д. А., Новичкова Г. А., Терещенко Г. В. Неинвазивная диагностика перегрузки железом методом магнитно-резонансной томографии // Вопросы гематологии/онкологии и иммунопатологии в педиатрии. — 2020. — № 3. — С. 158–163.
Абрамов Д. Д., Кадочникова В. В., Якимова Е. Г. и др. Частота мутаций, ассоциированных с развитием наследственного гемохроматоза I типа, болезни Вильсона — Коновалова и семейной средиземноморской лихорадки, и особенности их распределения в русской популяции // Генетика. — 2021. — № 1. — С. 95–102.
Lanzara C., Roetto A., Daraio F. et al. Spectrum of hemojuvelin gene mutations in 1q-linked juvenile hemochromatosis // Blood. — 2004. — № 11. — Р. 4317–4321. ссылка
Camaschella C., Fargion S., Sampietro M. et al. Inherited HFE-unrelated hemochromatosis in Italian families // Hepatology. — 1999. — № 5. — Р. 1563–1564.ссылка
Pietrangelo A. Hereditary hemochromatosis: pathogenesis, diagnosis, and treatment // Gastroenterology. — 2010. — № 2. — Р. 393–408. ссылка
Cartella I., Tavecchia G. A., Quattrocchi G. et al. A heart of iron: juvenile haemochromatosis presents with cardiac failure // Lancet. — 2022. — № 10352. ссылка
Lok C. Y., Merryweather-Clarke A. T., Viprakasit V. et al. Iron overload in the Asian community // Blood. — 2009. — № 1. — Р. 20–25.ссылка
Roetto A., Papanikolaou G., Politou M. et al. Mutant antimicrobial peptide hepcidin is associated with severe juvenile hemochromatosis // Nat Genet. — 2003. — № 1. — Р. 21–22. ссылка
Matthes T., Aguilar-Martinez P., Pizzi-Bosman L. et al. Severe hemochromatosis in a Portuguese family associated with a new mutation in the 5'-UTR of the HAMP gene // Blood. — 2004. — № 7. — Р. 2181–2183. ссылка
Bardou-Jacquet E., Cunat S., Beaumont-Epinette M. P. et al. Variable age of onset and clinical severity in transferrin receptor 2 related haemochromatosis: novel observations // Br J Haematol. — 2013. — № 2. — Р. 278–281. ссылка
Pietrangelo A. Ferroportin disease: pathogenesis, diagnosis and treatment // Haematologica. — 2017. — № 12. — Р. 1972–1984. ссылка
Muckenthaler L., Marques O., Colucci S. et al. Constitutional PIGA mutations cause a novel subtype of hemochromatosis in patients with neurologic dysfunction // Blood. — 2022. — № 9. — Р. 1418–1422. ссылка
Crownover B. K., Covey C. J. Hereditary hemochromatosis // Am Fam Physician. — 2013. — № 3. — Р. 183–190. ссылка
Utzschneider K. M., Kowdley K. V. Hereditary hemochromatosis and diabetes mellitus: implications for clinical practice // Nat Rev Endocrinol. — 2010. — № 1. — Р. 26–33. ссылка
Vantyghem M. C., Dobbelaere D., Mention K. et al. Endocrine manifestations related to inherited metabolic diseases in adults // Orphanet J Rare Dis. — 2012. — Vol. 7. ссылка
Kelly T. M., Edwards C. Q., Meikle A. W., Kushner J. P. Hypogonadism in hemochromatosis: reversal with iron depletion // Ann Intern Med. — 1984. — № 5. — Р. 629–632. ссылка
Angelopoulos N. G., Goula A. K., Papanikolaou G., Tolis G. Osteoporosis in HFE2 juvenile hemochromatosis. A case report and review of the literature // Osteoporos Int. — 2006. — № 1. — Р. 150–155. ссылка
Yanamandra U., Mukherji R., Patyal S. et al. Ladakhi koilonychias // Case Reports. — 2014. ссылка

