Определение болезни. Причины заболевания
Болезнь Рандю — Ослера — Вебера (Rendu-Osler-Weber disease) — это наследственное заболевание, при котором возникают:
- повторяющиеся носовые кровотечения;
- множественные телеангиэктазии (расширения мелких сосудов кожи);
- артериовенозные шунты и мальформации (патологические соединения артерий и вен без капилляров) в различных внутренних органах.
![Признаки болезни Рандю — Ослера — Вебера [15] Признаки болезни Рандю — Ослера — Вебера [15]](/media/bolezny/bolezn-randyu-oslera/priznaki-bolezni-randyu-_-oslera-_-vebera-15_s.jpeg?dummy=1770811037623)
Признаки болезни Рандю — Ослера — Вебера [15]
Другие названия болезни — семейная наследственная телеангиэктазия, геморрагический семейный ангиоматоз, семейная геморрагическая телеангиэктазия или генерализованный ангиоматоз.
Впервые рецидивирующие носовые кровотечения были описаны врачом Генри Саттоном в 1864 году, а в 1865 году в журнале Lancet английский врач Бенджамин Бабингтон опубликовал статью о носовых кровотечениях, носящих наследственный характер [16].
В конце XIX – начале XX века случаи носовых кровотечений с наличием телеангиэктазий у членов одной семьи описали сразу трое учёных: французский врач Анри Рандю в 1896 году, канадский терапевт Вильям Ослер в 1901 году и британский врач Фредерик Вебер в 1907 году [16]. Они сразу сделали предположение о наследственной природе их возникновения. В последующем наследственная теория возникновения заболевания подтвердилась, и болезнь назвали в честь этих учёных.
Распространённость болезни Рандю — Ослера — Вебера
Заболевание очень редкое, его распространённость составляет, по разным данным, 1 случай на 3,5–100 тыс. населения. Наследуется оно по аутосомно-доминантному типу, т. е. если болен один из родителей, то вероятность ребёнка заболеть равна 50 % [8].

Аутосомно-доминантный тип наследования
Заболевание одинаково часто встречается среди мужчин и женщин, прогрессирует с возрастом и не зависит от расы и места проживания [6].
Причины болезни Рандю — Ослера — Вебера
Причиной патологии являются мутации в генах. Выделено более тысячи различных патологических мутаций, приводящих к развитию заболевания [9]. Из-за них нарушается структура мышечного и эластичного слоёв сосудистой стенки, в результате появляются выпячивания стенки и аневризматические расширения сосудов, а также телеангиэктазии и артериовенозные мальформации (АВМ) [6].
![Артериовенозная мальформация в головном мозге [21] Артериовенозная мальформация в головном мозге [21]](/media/bolezny/bolezn-randyu-oslera/arteriovenoznaya-malformaciya-v-golovnom-mozge-21_s.jpeg?dummy=1770959853631)
Артериовенозная мальформация в головном мозге [21]
Симптомы болезни Рандю — Ослера
Первые симптомы могут появиться уже в первый год после рождения ребёнка, но также болезнь может начать проявляться и в более позднем возрасте, например к 10 годам, а в 20–40 лет заболевание прогрессирует [11].
Рецидивирующие носовые кровотечения — наиболее частый симптом, который встречается у 90 % пациентов. Среди людей, которые обращаются к врачу по поводу носового кровотечения, от 4,8 до 14,3 %, по данным разных авторов, страдают именно болезнью Рандю — Ослера — Вебера [11].
Носовые кровотечения возникают спонтанно и носят изматывающий характер. Первоначально пациенты чаще всего не обращаются к врачу и сами останавливают кровотечения путём тампонирования носовых ходов. Со временем длительность кровотечений увеличивается и может достигать 7,5 минут и более, при этом объём кровопотери может составлять 200–300 мл [11].
Телеангиэктазии — второй наиболее распространённый симптом заболевания. Они выглядят как «паутинки» или «сосудистые звёздочки» на коже от ярко-красного до тёмно-фиолетового цвета, могут появляться в области ушных раковин, подушечек пальцев, носогубного треугольника и на других видимых участках тела и слизистых оболочках.
![Телеангиэктазии на губах и слизистой оболочке рта [14] Телеангиэктазии на губах и слизистой оболочке рта [14]](/media/bolezny/bolezn-randyu-oslera/teleangiektazii-na-gubah-i-slizistoy-obolochke-rta-14_s.jpeg?dummy=1770809593227)
Телеангиэктазии на губах и слизистой оболочке рта [14]
Размеры их варьируют от нескольких миллиметров до 3 см [11]. Некоторые представляют собой разветвлённую сосудистую сеть, которая возвышается над кожей и затрагивает большие участки кожи и слизистых оболочек, придавая им синюшно-багровый цвет. Характерной особенностью телеангиэктазий является их исчезновение при надавливании и высокая кровоточивость даже при незначительных повреждениях кожи.
Изменённые сосуды могут встречаться и во внутренних органах. В этом случае симптомов может не быть долгое время. Они будут появляться по мере взросления пациента и прогрессирования заболевания.
При наличии изменённых сосудов в головном мозге дети могут страдать от различных неврологических нарушений: головных болей, мигрени, судорог, снижения чувствительности, двигательных нарушений и головокружения.
Симптомы при АВМ в лёгких зависят от их размера: чем они больше, тем больше крови сбрасывается из артерий в вены, минуя капилляры (где кровь должна насыщаться кислородом), и тем сильнее выражена симптоматика. Чаще всего клинические признаки поражения лёгких возникают после 40 лет [9]. Из-за нехватки кислорода у пациентов появляется или начинает прогрессировать одышка, цианоз (синюшность) губ, кровохарканье.
АВМ в печени встречаются у 8–30 % пациентов, страдающих болезнью Рандю — Ослера — Вебера. Длительное время они могут протекать бессимптомно [7]. В печени встречаются мальформации различных размеров: от небольших до гигантских, приводящих к сердечной недостаточности, портальной гипертензии и заболеваниям желчевыводящих путей (холестазу, холангиту). У пациентов при этом может появляться одышка при небольшой физической нагрузке, отёки ног, боли в животе, нарушения стула, отрыжка и тошнота.
Патогенез болезни Рандю — Ослера
В норме сосудистая стенка состоит из трёх слоёв: внутреннего (интимы), среднего (медии) и наружного (адвентиции):
- внутренняя поверхность сосуда гладкая, покрыта эндотелием, благодаря ей кровь беспрепятственно движется по сосудам;
- средняя оболочка состоит из гладкомышечной и эластичной ткани, она помогает сохранять тонус сосуда и поддерживать постоянное давление крови внутри сосуда;
- наружная оболочка состоит из соединительной ткани и содержит кровеносные, лимфатические сосуды и нервы, питающие сам сосуд.
Такая многослойность помогает сосуду поддерживать эластичность и выдерживать давление крови. Мелкие сосуды могут состоять из одного эндотелиального слоя.
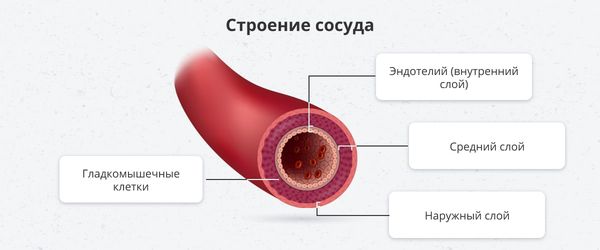
Строение сосудистой стенки
При болезни Рандю — Ослера — Вебера из-за мутаций средний слой сосудистой стенки формируется неправильно [4]. В результате стенка сосуда становится необычайно рыхлой, и даже незначительное механическое, физическое или химическое воздействие может её повредить и привести к кровотечению. Сосуды могут иметь нетипичные мешковидные расширения, артериовенозные шунты и мальформации, а также аневризмы (крупные выпячивания сосуда с тонкой стенкой).
Разрыв аневризм может приводить к массивным кровотечениям и кровопотерям, а разрыв в сосудах головного мозга (например, при повышенном артериальном давлении) грозит геморрагическим инсультом.
При артериовенозных шунтах и мальформациях кровь напрямую течёт из артерии в вену, минуя капилляры, где она должна насыщаться кислородом. Из-за этого возможны разные нарушения. Например, формирование АВМ в лёгких приводит к гипоксемии (недостатку кислорода в крови), лёгочной гипертензии (повышенному давлению в лёгочных артериях) и неврологическим нарушениям [6].
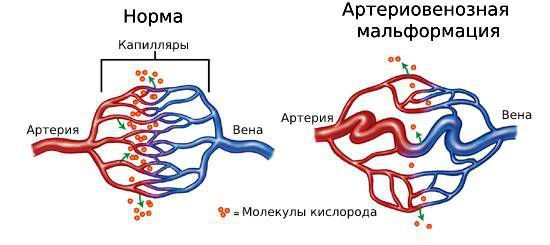
Нормальное соединение артерии и вены и АВМ
Спинальные АВМ могут приводить к парезам (слабости мышц), параличам (полной неподвижности) и нарушениям чувствительности. Такие нарушения возникают:
- из-за недостатка кислорода в тканях спинного мозга (так как кровь сбрасывается из артерий в вены и хуже насыщается кислородом);
- микрокровоизлияний из патологических сосудов;
- механического сдавления спинного мозга самими сосудистыми мальформациями.
При печёночных АВМ может развиваться сердечная недостаточность. Это связано со снижением сопротивления сосудов и падением давления, из-за чего сердце вынуждено работать активнее, чтобы всё компенсировать: поддерживать нормальное давление и кровоснабжение органов. Это приводит к гипертрофии (утолщению) левого желудочка и формированию в последующем застойных явлений в большом и малом кругах кровообращения. Также при АВМ в печени возможно развитие портальной гипертензии (повышения давления в воротной вене).
Классификация и стадии развития болезни Рандю — Ослера
Болезнь Рандю — Ослера — Вебера относится к группе наследственных заболеваний. Общепринятой классификации не существует, но Вильям Ослер в 1907 году выделил три этапа развития телеангиэктазий:
- Сначала в виде пятна (мелкие сосудистые образования).
- Затем в виде небольших «сосудистых» паучков.
- На более поздних стадиях — ярко-красные возвышающиеся узловые образования диаметром до 7 мм [13]. Вокруг них часто видна сеть расширенных капилляров, особенно в области щёк, крыльев носа, губ, век, груди, что придаёт коже багрово-синюшный оттенок.
После 25 лет могут встречаться все типы телеангиэктазий.
Осложнения болезни Рандю — Ослера
Для сосудов при наследственной телеангиэктазии характерна высокая травматичность и кровоточивость. Кровотечения носят рецидивирующий характер и могут быть в разных местах — носовые, желудочно-кишечные, маточные, лёгочные. Массивные кровопотери могут угрожать жизни.
Частые рецидивирующие кровотечения осложняются хронической железодефицитной анемии и гипоксией (недостатком кислорода в тканях организма). У пациентов появляется выраженная слабость, головокружения, бледность кожи, могут быть эпизоды потери сознания. В таких случаях может потребоваться переливание крови.
Осложнения, связанные с АВМ, будут зависеть от того, где сформировалась мальформация:
- АВМ в центральной нервной системе (ЦНС) длительное время могут протекать бессимптомно и проявиться уже в виде состоявшегося внутричерепного кровоизлияния. Оно будет сопровождаться выраженной головной болью, потерей сознания, зрительными, двигательными и чувствительными нарушениями. Это осложнение чаще всего становятся причиной смерти детей с болезнью Рандю — Ослера — Вебера и поражением центральной нервной системы [9].
- При наличии крупных АВМ в лёгких осложнением может быть гемоторакс (скопление крови в плевральной полости) и тяжёлая сердечная недостаточность, проявляющаяся резко нарастающей одышкой и снижением толерантности (переносимости) к физической нагрузке [12].

Гемоторакс
- Множественные крупные мальформации в желудочно-кишечном тракте могут осложниться тяжёлыми кровотечениями с рвотой кровью, чёрным дёгтеобразным стулом, потерей сознания и смертью. Чаще такие кровотечения появляются в более позднем возрасте — после 40 лет [6].
- Крупные мальформации в печени приводят к системному нарушению кровообращения и развитию сердечной недостаточности. В этом случае у пациента будет нарастать одышка при нагрузке, появляться отёки ног, а в более поздних стадиях одышка будет беспокоить в покое, появится жидкость в брюшной полости (асцит).
Диагностика болезни Рандю — Ослера
Диагностикой и лечением болезни Рандю — Ослера — Вебера занимается гематолог. Однако, так как при наследственной телеангиэктазии могут поражаться различные органы и системы, пациент с симптомами заболевания может оказаться на приёме практически у любого специалиста:
- чаще всего пациенты обращаются к лор-врачу или дерматологу, так как наиболее частые и ранние симптомы заболевания — носовые кровотечения и видимые телеангиэктазии;
- если заболевание начинает проявляться с желудочно-кишечного или лёгочного кровотечения, пациент окажется в хирургическом отделении стационара;
- в случае преимущественно неврологической симптоматики пациент будет консультироваться у невролога.
Так как заболевание передаётся по наследству, то все дети, у которых есть прямые кровные родственники (мама, папа, бабушка, дедушка) с этим заболеванием, обязательно проходят генетическое исследование.
Как правило, при генерализованной форме (массовом поражении органов и систем) и наличии семейного анамнеза поставить диагноз не составляет труда. Гораздо сложнее, когда поражён какой-либо один орган (желудок, матка, лёгкие или печень) и у родителей пациента не установлен диагноз болезни Рандю — Ослера — Вебера. В этом случае заболевание можно заподозрить на основании данных анамнеза, осмотра и результатов дообследования.
Сбор жалоб, анамнеза (истории жизни и болезни) и осмотр
При опросе врач уточнит, когда появились первые признаки заболевания (носовые кровотечения, кровохарканье, телеангиэктазии). Если у родителей пациента не установлен диагноз, доктор спросит есть ли подобные симптомы или подтверждённые мальформации у кровных родственников.
При осмотре обратит особое внимание на кожу и слизистые оболочки — на них будут видны сосудистые сеточки в виде «паучков», исчезающие при надавливании.
Лабораторные и инструментальные исследования
Помимо сбора анамнеза и осмотра, может потребоваться дообследование:
- общеклинические лабораторные анализы (позволяют выявить железодефицитную анемию);
- магнитно-резонансная и компьютерная томография (МРТ и КТ), в том числе с контрастированием;
- ультразвуковое исследование (УЗИ);
- различные эндоскопические методы (ФГДС, риноэндоскопия, колоноскопия, ректороманоскопия).

Фиброгастродуоденоскопия (ФГДС)
Важное значение в диагностике болезни Рандю — Ослера — Вебера принадлежит ангиографии, при которой можно выявить аневризматические расширения сосудов и АВМ [12].
Критерии диагностики
Для диагностики заболевания используют критерии, предложенные Консенсусом экспертов в 2000 году, известные как критерии Curaçao [1].
Всего их четыре:
- Спонтанные и рецидивирующие носовые кровотечения.
- Множественные телеангиэктазии с характерным расположением (губы, полость носа и рта, пальцы).
- Висцеральные поражения, т. е. поражения внутренних органов (желудочно-кишечные, лёгочные, церебральные, спинальные и/или печёночные АВМ).
- Семейный анамнез — наличие болезни у одного из родителей [10].
Диагноз считается достоверным, если присутствуют три критерия из четырёх, вероятным, если есть два критерия, и маловероятным при наличии только одного критерия.
Генетическое исследование
Если по результатам обследования возникает подозрение на болезнь Рандю — Ослера — Вебера, то врач может назначить генетическое исследование, чтобы подтвердить наличие мутаций.
Дифференциальная диагностика
Телеангиэктазии, кровотечения и другие проявления могут возникать не только при болезни Рандю — Ослера — Вебера, но и при других заболеваниях, таких как:
- болезни печени (могут сопровождаться телеангиэктазиями);
- гемофилия;
- тромбоцитопеническая пурпура;
- диффузная ангиокератома туловища Фабри.
Врач в ходе обследования будет последовательно их исключать.
Лечение болезни Рандю — Ослера
Консервативное лечение
В первую очередь всем пациентам с этим заболеванием следует соблюдать лечебно-охранительный режим и стараться избегать механических травм. В питании стоит ограничить продукты, которые могут потенциально влиять на свёртываемость крови и проницаемость сосудистой стенки, а именно:
- естественные антиагреганты (чеснок, имбирь, женьшень);
- продукты, содержащие салицилаты (кофе, пряности, шоколад, красное вино) и высокие концентрации омега-3 жирных кислот (лососёвые сорта рыбы).
Не рекомендуется принимать нестероидные противовоспалительные средства (НПВС), так как они ещё больше увеличивают риск кровотечений за счёт влияния на стенку сосудов.
Основу лечения составляет контроль над общими и местными симптомами. При носовых кровотечениях используются различные методы его остановки:
- тампонада носа гемостатической губкой;
- орошение раствором аминокапроновой кислоты;
- местное применение лубрикантов, мазей, кремов с гормональными и антифибринолитическими свойствами [2].
При значительных кровотечениях может потребоваться внутривенное введение кровоостанавливающих средств, а иногда и переливание крови.
Хирургическое лечение
В ряде случаев при выявлении жизнеугрожающих мальформаций прибегают к хирургическому лечению. Может выполняться:
- эндоваскулярное закрытие шунтов;
- удаление части органа;
- транскатетерная эмболизация (закупорка патологического сосуда изнутри через катетер);
- трансплантация органа (например, печени);
- септодермопластика слизистой оболочки на перегородке носа (замена патологически изменённой, хрупкой слизистой оболочки на более прочную ткань) [9].
Патогенетическая терапия
Медицина не стоит на месте, идёт постоянный поиск терапии, направленной на коррекцию ангиогенеза (процесса образования новых кровеносных сосудов из ранее существовавших). В лечении пытаются использовать антитела против фактора роста эндотелия сосудов (VEGF) и ингибиторы тирозинкиназы [4][9]. Эти препараты нейтрализуют биологическую активность человеческого фактора роста эндотелия сосудов и препятствуют процессу роста сети кровеносных сосудов.
Прогноз. Профилактика
Болезнь Рандю — Ослера — Вебера является наследственной, поэтому полностью вылечить её невозможно, но можно контролировать симптомы и поддерживать нормальное качество жизни.
По данным одного исследования, средняя продолжительность жизни пациентов с наследственной телеангиэктазией составила 63,2 года, тогда как средняя продолжительность жизни людей без этого заболевания составила 70 лет [5]. Однако у большинства пациентов, которые получают адекватную медицинскую помощь, средняя продолжительность жизни нормальная [3].
Прогноз зависит не только от наличия болезни, но и от того, сколько органов и систем поражено и как сильно. Длительное время пациенты могут не иметь никаких симптомов и не обращаться к врачам. Как правило, заболевание прогрессирует с возрастом [3].
Профилактика болезни Рандю — Ослера — Вебера
Так как заболевание генетическое и передаётся по наследству, предотвратить его развитие невозможно. Однако можно снизить риск его тяжёлого течения. Для этого все дети, чьи кровные родственники страдают болезнью Рандю — Ослера — Вебера, должны проходить генетическое исследование. Это позволит как можно раньше выявить болезнь и начать лечение.
При плановых стоматологических или других инвазивных вмешательствах пациентам рекомендуется антибактериальная профилактика, так как из-за особенностей кровоснабжения у них высок риск инфекционных осложнений [9].
Список литературы
Bayrak-Toydemir P., McDonald J., Markewitz B. et al. Genotype-phenotype correlation in hereditary hemorrhagic telangiectasia: mutations and manifestations // The American Journal of Medical Genetics. — 2006. — Vol. 140, № 5. — Р. 463–470.ссылка
Faughnan M. E., Mager J. J., Hetts S. W. et al. Second International Guidelines for the Diagnosis and Management of Hereditary Hemorrhagic Telangiectasia // Annals of Internal Medicine. — 2020. — Vol. 173, № 12. — Р. 989–1001. ссылка
Macri A., Wilson A. M., Shafaat O., Sharma S. Osler-Weber-Rendu Disease (Archived) // StatPearls Publishing. — 2023. ссылка
Robert F., Desroches-Castan A., Bailly S. et al. Future treatments for hereditary hemorrhagic telangiectasia // Orphanet J Rare Dis. — 2020. — Vol. 15, № 1.ссылка
Sabba C., Pasculi G., Suppressa P. et al. Life expectancy in patients with hereditary haemorrhagic telangiectasia // QJM. — 2006. — Vol. 99. — Р. 327–334.ссылка
Бойко Н. В. Современная диагностика и лечение наследственной геморрагической телеангиэктазии // Российская ринология. — 2020. — Т. 28, № 1. — С. 20–25.
Коротков С. В., Василенко М. Н., Штурич И. П. и др. Трансплантация печени при печёночной форме болезни Рандю — Ослера — Вебера / // Вестник трансплантологии и искусственных органов. — 2021. — Т. 23, № S. — С. 81.
Ильенкова Н. А., Алексеева О. В., Чикунов В. В. Семейный случай наследственной геморрагической телеангиэктазии // Прикаспийский вестник медицины и фармации. — 2023. — Т. 4, № 2. — С. 67–72.
Мизерницкий Ю. Л., Шатоха П. А., Соколова Л. В. Болезнь Рандю — Ослера — Вебера (наследственная геморрагическая телеангиэктазия) с поражением органов дыхания // Пульмонология. — 2023. — Т. 33, № 2. — С. 216–224.
Сун А. А., Усольцева А. С., Фоминский А. А. Трудности диагностики редких локальных форм наследственной геморрагической телеангиэктазии // Молодежь XXI века: шаг в будущее: материалы XXI региональной научно-практической конференции (Благовещенск, 20 мая 2020 года). В 4 т. — Том 3. — Благовещенск: Дальневосточный государственный аграрный университет, 2020. — С. 68–69.
Товмасян А. С., Мосин В. В., Носуля Е. В. и др. Наследственная геморрагическая телеангиэктазия (синдром Рандю — Ослера) // Вестник оториноларингологии. — 2022. — Т. 87, № 5. — С. 86–91.
Линник О. В., Сидорович Э. К., Лихачев С. А. и др. Клинический случай повторных инфарктов головного мозга у пациента молодого возраста с болезнью Рандю — Ослера — Вебера // Уральский медицинский журнал. — 2018. — Т. 166, № 11. — С. 46–52.
Войцеховский В. В., Гоборов Н. Д., Ткачева С. И. и др. Случай болезни Рандю — Ослера с поражением полости носа и бронхов // Бюллетень физиологии и патологии дыхания. — 2017. — № 63. — С. 91–97.
Venugopal A. Hereditary haemorrhagic telangiectasia // BMJ. — 2022. — Vol. 376.
Botella L.-M., Albiñana V., Ojeda-Fernandez L., Recio-Poveda L., Bernabéu C. Research on potential biomarkers in hereditary hemorrhagic telangiectasia // Front Genet. — 2015. — Vol. 6.ссылка
Sabba C. A rare and misdiagnosed bleeding disorder: hereditary hemorrhagic telangiectasia // J Thromb Haemost. — 2005. — Vol. 3. — Р. 2201–2210.ссылка

