Определение болезни. Причины заболевания
Синдром Золлингера — Эллисона (Zollinger — Ellison syndrome) — это заболевание, которое сопровождается множественными пептическими язвами в верхних отделах желудочно-кишечного тракта и повышенным уровнем соляной кислоты в желудке. Проявляется болью в животе, хронической диареей, изжогой и другими симптомами.
Для заболевания характерно, что при воспалении слизистой желудка и двенадцатиперстной кишки нет эффекта от приёма ингибиторов протонной помпы (ИПП), например Омепразола и Рабепразола: даже на фоне терапии сохраняется боль, изжога и периодически возникает диарея.
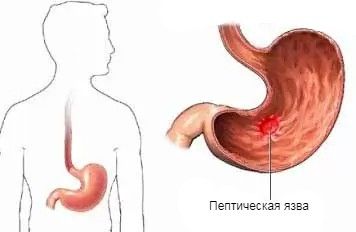
Язва в желудке при синдроме Золлингера — Эллисона
Синдром впервые описали в 1955 году американские хирурги R. Zollinger и E. Ellison из медицинского центра Университета штата Огайо [1][2][3].
Заболевание развивается на фоне появления гастриномы — функционально активного новообразования, которое вырабатывает гастрин. Этот гормон стимулирует секрецию соляной кислоты, в норме он выделяется клетками слизистой оболочки желудка и в меньшей степени клетками двенадцатиперстной кишки. Гастринома же вырабатывает избыточное количество этого гормона.
В основном опухоль образуется в пределах «треугольника гастриномы», который ограничен соединением пузырного и общего печёночного протоков, двумя отделами двенадцатиперстной кишки и соединением между шейкой и телом поджелудочной железы [1][5].
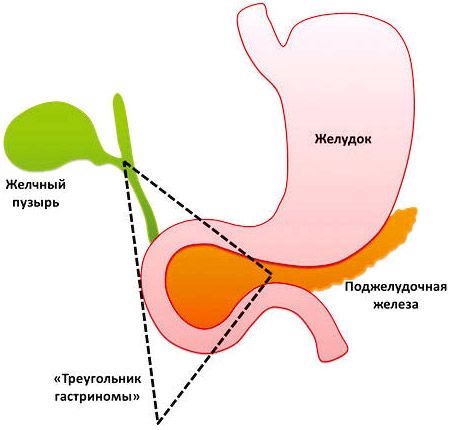
«Треугольник гастриномы»
Ранее считалось, что в 80 % случаев гастриномы локализуются в поджелудочной железе и лишь 12–20 % — в двенадцатиперстной кишке. По современным данным, 70 % гастрином расположены в двенадцатиперстной кишке, 25 % — в поджелудочной железе, 5 % — в желудке, лимфатических узлах брюшной полости и тонкой кишке, также встречаются единичные случаи в желчном пузыре, почках, печени и яичниках [4][20][22].
Синдром Золлингера — Эллисона бывает двух форм:
- Спорадичная форма (75 % пациентов). Обычно это единичный случай болезни в семье, при этом ни причина, ни механизмы заболевания не установлены [7].
- Семейная форма (30–38 % случаев [3]). У синдрома есть точное генетическое происхождение, связанное с развитием множественной эндокринной неоплазии 1-го типа, которая наследуется [1][7].
Причины синдрома Золлингера — Эллисона
Помимо генетической предрасположенности, риск развития синдрома повышается при отягощённом эндокринном анамнезе — двух и более аутоиммунных или других эндокринологических заболеваний неясной причины: аденоме гипофиза, хроническом аутоиммунном тиреоидите, Mody-диабете, синдроме поликистозных яичников и др. Также риск повышается, если такие заболевания выявлены у родственников пациента.
Распространённость
Заболевание считается орфанным (редким): его диагностируют у 0,5–1,5 человек на 1 млн. В год его выявляют у 0,2–2 пациентов на 100 тыс. населения [16]. Но в практике врачей эта патология встречается гораздо чаще [5]. Из-за того, что синдром редкий, его подозревают нечасто и обычно устанавливают другой диагноз, а в статистику входят пациенты с уже подтверждённым заболеванием. Следовательно, синдром встречается чаще, чем его верно диагностируют.
Согласно литературным данным, нет чёткой гендерной предрасположенности, так как в одних источниках указывается, что заболевание чаще встречается у мужчин [16], в других источниках — что у женщин [7]. Средний возраст постановки диагноза у пациентов со спорадическими случаями составляет 40–50 лет [16][20], при множественной эндокринной неоплазии — около 30–34 лет.
Симптомы синдрома Золлингера — Эллисона
Как для спорадических, так и для семейных форм заболевания характерны следующие общие симптомы:
- Умеренная боль в области эпигастрия (в 75 % случаев [3]). Возникает через 2–3 часа после приёма пищи или ночью («голодные» боли). Такая боль появляется из-за эрозий в желудке и двенадцатиперстной кишке, что вызвано агрессивным действием соляной кислоты на их слизистую оболочку [16]. Приступы боли могут наблюдаться от 5–7 раз в год. Они могут проходить после лечения антисекреторными препаратами (ИПП), но бывает, что не уменьшаются даже на фоне терапии. Приём этих лекарств без контроля врача может «стирать» клиническую картину: уровень гастрина в крови снижается, симптомы исчезают, из-за чего трудно поставить точный диагноз [20].

Эпигастрий
- Диарея (73 % случаев). Может возникать периодически в разное время суток из-за усиленной моторики тонкой кишки и замедленного всасывания пищи в результате попадания большого количества соляной кислоты. Стул при этом обильный, водянистый. В тяжёлых случаях снижается вес и возникают электролитные нарушения [11]. Далее диарея становится хронической (длится более 3 недель), но это встречается в 20 % случаев нейроэндокринных опухолей, обычно при метастазах в печень [25].
- Жжение в груди после приёма пищи, отрыжка воздухом или кислым содержимым, затруднение и боль при глотании. Эти симптомы связаны с повреждением стенки пищевода соляной кислотой, что приводит к эзофагиту и ГЭРБ. Симптомы часто усиливаются после переедания, употребления кислого, ночного приёма пищи, а также после отдыха лёжа (в том числе после сна) и при повышенном давлении на живот (ношении тугой одежды и корсетов, упражнениях на пресс). Тяжесть эзофагита может варьироваться от единичных эрозий до множественного поражения — 75 % пищевода [16][29].
- Наличие жира в кале (стеаторея). Кал становится блестящего цвета, без примесей, плохо смывается с унитаза. Такой симптом связан с тем, что избыточное выделение гастрина вызывает экзогенное нарушение — состояние, при котором активность ферментов, выделяемых в просвет двенадцатиперстной кишки, недостаточна для нормального переваривания пищи [3].
- Другие желудочно-кишечные симптомы. Раньше всего появляются внезапные схваткообразные боли в нижней части живота, которые сопровождаются громким урчанием и водянистой диареей со слизью, но без других дополнительных примесей [24].
- Однократная рвота кислым желудочным содержимым на фоне пика болей в животе [16].
Также на фоне заболевания может развиваться редкий синдром Вернера — Морисона, при котором стул становится водянистым, краснеет лицо, давление повышается до 140/90 мм рт. ст. Уровень калия в крови при этом опускается менее 3,5 ммоль/л, а уровень хлора — ниже 100 ммоль/л. Синдром связан с длительным обезвоживанием, которое может вызывать хроническую почечную недостаточность [12].
При семейной форме заболевания перечисленные симптомы могут сочетаться с такими состояниями, как:
- Нефролитиаз, или камни в почках (47 % случаев [6]). Может проявляться оксалатами в общем анализе мочи и камнями, которые обнаруживаются на УЗИ и КТ почек и мочевыводящих путей (чувствительность методов 45 и 90–100 % соответственно) [13]. Состояние может протекать как с симптомами, так и без них. К проявлениям нефролитиаза относятся почечные колики — сильные острые боли в области поясницы или нижней части спины, отдающие в нижнюю часть живота, паховую область и половые органы. Боль схваткообразная, наступает внезапно и может длиться до 18 часов.
- Гиперпаратиреоз (88–94 % случаев [6]). При этом состоянии повышается содержание паратгормона в крови, из-за чего ускоряются управляемые им процессы обмена кальция и фосфора. К ранним проявлениям патологии относится быстрая утомляемость при нагрузке и мышечная слабость. В крови выявляется гиперкальциемия (повышение уровня кальция в крови более 10,0 мг/дл) и гипофосфатемия (уровень фосфора менее 0,65 ммоль/л). Для поздней стадии заболевания характерны патологические переломы и образование «ложных суставов», когда в мягких тканях вокруг суставов на руках и ногах откладываются соли кальция [14].
- Доброкачественные опухоли в области гипофиза, которые могут вырабатывать гормоны (31–60 % случаев) [6]. К таким опухолям относятся:
- Соматотропная аденома (соматотропинома) — синтезирует соматотропин, или гормон роста. Для этой опухоли характерна акромегалия (увеличение отдельных частей тела: кистей, стоп, ушей, носа, губ, нижней челюсти), чрезмерная потливость и жирная кожа с акне [9].
- Пролактинсекретирующая аденома (пролактинома) — вырабатывает гормон пролактин. При пролактиномах возникает слабость, повышается утомляемость, человек набирает вес, наблюдается галакторея (выделение молока из грудных желёз, которое не связано лактацией или беременностью) и олигоменорея (менструальный цикл более 40 дней).
- Адренокортикотропинпродуцирующая аденома (кортикотропинома) — секретирует адренокортикотропный гормон (АКТГ), который стимулирует кору надпочечников. Для такой опухоли характерен плохой прогноз при синдроме Золлингера — Эллисона. В 90 % случаев диагностируется болезнь Иценко — Кушига [31], для которой характерно лунообразное лицо, появление красно-фиолетовых растяжек, увеличение живота, похудение рук и ног, раздражительность, чрезмерная потливость, повышение артериального давления более 140/90 мм рт. ст., нарушение репродуктивной функции [14].
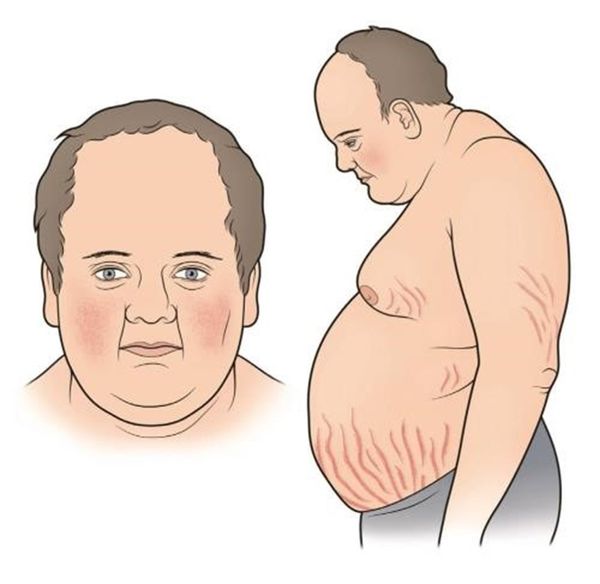
Болезнь Иценко — Кушига
- Тиреотропная аденома (тиреотропинома) — вырабатывает тиреотропный гормон (ТТГ), стимулирующий работу щитовидной железы. Проявляется симптомами гипертиреоза: похудением, раздражительностью, экзофтальмом (выпячиванием глазных яблок), аритмией (неправильным ритмом сердца), тахикардией (учащением сердечных сокращений более 90 ударов в минуту) [26].
- Карциноидная опухоль (карциноид) — это медленнорастущая гормонально активная опухоль. Она происходит из клеток, которые накапливают и секретируют пептидные гормоны и биогенные амины-вещества, образующиеся в организме из аминокислот. Эти вещества обладают высокой биологической активностью и действую как нейромедиаторы: адреналин, серотонин и норадреналин. Карциноид по клинической картине напоминает доброкачественные новообразования, но склонен к метастазированию в отдалённые органы, поэтому рассматривается как потенциально злокачественное новообразование. Чаще поражает желудок и кишечник [6].
Патогенез синдрома Золлингера — Эллисона
Для спорадической формы заболевания характерна мутация генов онкосупрессоров, или антионкогенов (INK4a, Smad4, HER2/neu), которые регулируют работу клетки во время её деления. При мутации этих генов клетки начинают делиться бесконтрольно, что и способствует росту опухоли, а именно гастриномы. Как было сказано выше, эта опухоль избыточно вырабатывает гастрин, что стимулирует чрезмерную секрецию соляной кислоты в желудке и приводит к типичным симптомам синдрома Золлингера — Эллисона.
Для семейной формы заболевания характерен аутосомно-доминантный тип наследования: болезнь проявляется, если у человека есть хотя бы один «дефектный» ген MEN1 (11q13 хромосома), доставшийся от отца или матери. Поэтому болезнь встречается в каждом поколении [1]. При этой форме опухоли появляются в нескольких органах эндокринной системы, например в гипофизе, поджелудочной железе или надпочечниках. Эти опухоли могут вырабатывать гормон, характерный именно для её типа: инсулин при инсулиноме, адренокортикотропный гормон при кортикостероме, гонадотропный гормон при гонадотропиноме [6].
Классификация и стадии развития синдрома Золлингера — Эллисона
В Международной классификации болезней (МКБ-10) синдром Золлингера — Эллисона относится к разделу К86 Другие болезни поджелудочной железы, подразделу K86.8 Другие уточнённые болезни поджелудочной железы и кодируется как K86.8.3 [17].
В новой версии Международной классификации болезней (МКБ-11) заболевание относится к разделу 5 Заболевания эндокринной системы и кодируется как 5A43.1 [18].
По происхождению:
По характеру течения:
- агрессивный характер (злокачественное течение, 25 % от всех гастрином) — характерен агрессивный рост опухоли, в течение 10 лет выживает около 30 % пациентов;
- неагрессивный характер (условно доброкачественное течение, 75 % от всех случаев) — в течение 10 лет выживает 96 % пациентов [6].
Осложнения синдрома Золлингера — Эллисона
К осложнениям заболевания относятся:
- Кровотечение в верхних отделах желудочно-кишечного тракта (24 % случаев [3]). Вызвано множественными язвенными дефектами. При кровотечении бледнеет кожа, стул становится чёрного цвета, появляется рвота кровью или содержимым цвета кофейной гущи, при этом исчезает боль в животе.
- Перфорация язвы двенадцатиперстной кишки (5 % случаев [3]). Это нарушение целостности стенки кишки, при котором желудочное содержимое проникает в брюшную полость. Проявляется невыносимой и неконтролируемой кинжальной болью в верхней части живота, дискообразным животом (напряжение мышц) и отсутствие брюшного дыхания.
- Стриктура пищевода (4–6 % случаев [3]. Это сужение его просвета, которое проявляется рвотой съеденной накануне пищей, отрыжкой тухлым, неприятным запахом изо рта и болью при глотании.
- Метастазирование опухоли (20–30 % случаев). Метастазирование гастриномы, как правило, происходит в печень, ближайшие лимфатические узлы и костную ткань [10]. Для этого осложнения нет характерной клинической картины, но обычно увеличиваются лимфоузлы, появляется слабость, снижается работоспособность, в анализах крови повышаются АСТ, АЛТ и ГГТП (синдром цитолиза — разрушения клеток печени).
- Кахексия. Это крайняя степень истощения с ИМТ менее 16–17 кг/м2. Для неё характерен метаболический синдром, при котором уменьшается объём мышечной ткани с или без потери жира и снижается уровень электролитов, необходимых витаминов и белка в организме.

Индекс массы тела
Диагностика синдрома Золлингера — Эллисона
При появлении симптомов синдрома лучше всего обратиться к гастроэнтерологу, но можно посетить и терапевта или врача общей практики. В любом случае обнаружить синдром Золлингера — Эллисона на раннем этапе довольно сложно из-за неспецифических симптомов в начале заболевания, длительного роста опухолей (10–25 лет), их малого размера, разнообразия жалоб и влияния препаратов.
Сбор анамнеза и осмотр
При сборе истории болезни врач может спросить:
- какие жалобы беспокоят и как долго;
- какие лекарства принимает пациент для облегчения симптомов и помогают ли они;
- устанавливали ли ранее какие-либо патологии желудочно-кишечного тракта (ЖКТ);
- есть ли какие-то другие сопутствующие эндокринные патологии, в том числе доброкачественные новообразования у пациента и у его родственников;
- наблюдается ли пациент у терапевта, гастроэнтеролога, эндокринолога или онколога.
В первую очередь врач обращает внимание на эффект от подобранных ранее препаратов: если они не помогают и симптомы усиливаются, то можно заподозрить орфанное заболевание.
При осмотре врач оценит вес и рост: у таких пациентов чаще всего дефицит веса. Также может наблюдаться бледность склер (но не всегда), тусклая, сероватая кожа со сниженным тургором, налёт на языке, возможен стоматит, невыраженные боли при ощупывании в эпигастральной области и вздутый живот.
Лабораторная диагностика
При подозрении на синдром Золлингера — Эллисона назначаются следующие анализы:
- Определение уровня гастрина в крови натощак. Норма гастрина составляет менее 150 пг/л. При гастриноме достигает > 1000 пг/мл. Это исследование является обязательным для первичного скрининга синдрома Золлингера — Эллисона.
- Провокационный тест с использованием синтетического секретина. Во время обследования внутривенно струйно вводится секретин (2 МЕ/кг массы тела). Уровень гастрина в сыворотке крови измеряется за 15 минут и через 1 минуту, а также через 2, 5, 10, 15, 20 и 30 минут после введения секретина. Тест будет положительным при подъёме уровня гастрина > 120 пг/мл. Это исследование обязательно для диагностики синдрома Золлингера — Эллисона.
- Определение уровня хромогранина (CgA) в крови. Маркер может применяться при опухолях со злокачественным течением для эффективности терапии [6]. Исследование назначается онкологом по показаниям и не является обязательным.
- Молекулярно-генетическое исследование на мутации в гене МЭН-1. Позволяет подобрать более эффективное лечение, но показано, только если врач подозревает множественные нейроэндокринные опухоли при семейной форме заболевания.
Инструментальная диагностика
Проводятся следующие обследования:
- Эзофагогастродуоденоскопия (ЭГДС) с биопсией желудка по стандарту OLGA и экспресс-тестом на бактерию хеликобактер пилори. Это исследование обязательно для исключения других органических патологий, например эзофагита другого происхождения (эозинофильного, паразитарного, нестероидного), аутоиммунного гастродуоденита, язвы желудка и ДПК, ассоциированных с хеликобактер пилори, стрессовых и других язв.

ЭГДС
- 24-часовая внутрижелудочная pH-метрия. Суточная рН-метрия — это измерение кислотности в пищеводе, желудке и двенадцатиперстной кишке с помощью прибора «Гастроскан-24». В желудочно-кишечный тракт через нос вводят тонкий рН-зонд со специальными датчиками, которые измеряют уровень кислотности в органах ЖКТ. Процедура может проводиться в амбулаторных условиях. Во время её проведения пациенту необходимо ввести дневник своих действий. При заболевании наблюдается снижение внутрижелудочного pH < 2. Обследование позволяет отличить синдром Золлингера — Эллисона от эзофагита при неэффективности ИПП. Также исследование может применяться для контроля назначенной терапии [3][16].
- Трансабдоминальное УЗИ. Этот метод, как и предыдущий, проводится в числе первых при подозрении на синдром Золлингера — Эллисона.
- КТ-органов брюшной и грудной полостей. Компьютерная томография — это обязательный метод, так как позволяет с высокой точностью выявить опухоль, определить её местоположение и возможное наличие метастазов [3][16].
- МРТ-головного мозга. Магнитно-резонансная томография не является обязательным методом, назначается эндокринологом при подозрении на нейроэндокринные опухоли или онкологом при подозрении на метастазы [16].
- Эндоскопическая ультрасонография (ЭУС). Это уникальный метод эндоскопической диагностики, в ходе которого выполняется ультразвуковое сканирование стенок органов ЖКТ. Проводится под общей анестезией. ЭУС в сочетании с тонкоигольной биопсией являются стандартом для диагностики гастриномы. Эти исследования назначаются онкологом для анализа тканей новообразования и подбора эффективной химиотерапии [20].
- Сцинтиграфия рецепторов к соматостатину (СРС) с использованием 111-In-пентетреотида и однофотонной эмиссионной компьютерной томографии. Сомастостин-рецепторную сцинтиграфию относят к современным радионуклидным способам обследования и лечения. Она позволяет обнаружить опухоль и оценить распространённость процесса. На снимках проявляются образования, имеющие соматостатиновые рецепторы высокой плотности. Обследование назначается пациентам с нейроэндокринными опухолями. Перед проведением исследования пациенту внутривенно вводят часть реактивного вещества, а через 4 часа проводят сканирование на аппарате. Продолжительность исследования 60–90 мин. При необходимости его проводят повторно через 48 часов после введения препарата. Этот метод признан одним из самых чувствительных, его назначает онколог, если ЭУС оказалась неэффективной [28].
- Позитронно-эмиссионная томография (ПЭТ). Это инструмент для выявления рецидивов опухолей, назначается онкологом при периодическом мониторинге во время лечения [19][28].
Лечение синдрома Золлингера — Эллисона
Сегодня единственным радикальным методом терапии является хирургическое лечение [4]. Его результаты лучше, чем у химиотерапии или медикаментозного лечения: после операции примерно у половины пациентов нет рецидивов в течение 5–10 лет [16].
Если говорить о конкретных методах, то в хирургии сейчас активно применяется эндоскопическая полностенная резекция (ЭПР) — высокотехнологичная операция, которая облегчает удаление новообразования слизистой оболочки, в том числе при его проникновении в подслизистый слой. Целостность стенки органа при этом не нарушается. Существуют два принципиальных подхода для удаления таких новообразований: с полностенной резекцией или без неё, т. е. открытый и закрытый. В первом случае происходит проникновение в брюшную полость с последующим закрытием дефекта [33].
Метод подходит как для радикального удаления ранних форм опухолей в тех случаях, когда рассечь ткани подслизистого слоя технически невозможно, так и для того, чтобы избежать более инвазивного хирургического вмешательства. После резекции опухоли в течение 2 лет после операции биохимический рецидив (т. е. появление в крови специфических маркеров) наблюдается в 65 % случаев, а морфологический рецидив (выявление опухоли) — у 40 % больных [20].
У пациентов с метастазами, а также при невозможности обнаружить опухоль применяется консервативная терапия и/или паллиативное хирургическое лечение. Терапевтические подходы должны решать две задачи: контролировать гиперсекрецию соляной кислоты и развитие гастриномы.
Также на любом этапе лечения гастроэнтеролог назначает антисекреторную терапию — приём ИПП. Они помогают подавить гиперсекрецию соляной кислоты. Препараты применяются в двойной дозировке, при полном подавлении соляной кислоты дозы уменьшают. Антисекреторная терапия при правильном подборе дозировки способна предотвратить рецидивы язв, что значительно уменьшает риск возникновения осложнений.
Также в медикаментозную терапию входят синтетические аналоги соматостатина (Октреотид). Исследования доказали, что применение аналогов соматостатина стабилизировали рост опухоли в 37–80 % случаев и уменьшали её размер в 17 % случаев [16]. При неэффективности этой терапии проводится комплексное лечение с Интерфероном-α. Эта терапия приводит к стабилизации опухоли в 20–40 % случаев, а в 12 % способствует её уменьшению [16].
Цитотоксическая химиотерапия подбирается врачом-онкологом при более злокачественных формах, тяжёлой опухолевой нагрузке или очень тяжёлых симптомах. При таком лечении выздоравливает 45–70 % пациентов [19].
Прогноз. Профилактика
При своевременной диагностике и лечении прогноз может быть благоприятным, так как можно приостановить рост опухоли. Но на прогноз сильно влияет наличие метастазов. Так, десятилетняя выживаемость у пациентов без метастазов и с метастазами только в лимфоузлы составляет 96–100 %, а с метастазами в печень, яичники, почки или костную ткань — 26–30 % [6].
Есть и другие факторы плохого прогноза: сочетание гастриномы и кортикотропиномы. В таком случае добиться ремиссии практически невозможно [27].
Профилактика этой патологии не разработана. Можно рекомендовать пройти генетическое консультирование перед планированием беременности пациентам с отягощённым семейным анамнезом (наличием нейроэндокринных опухолей у родственников: кортикотропиномы, пролактиномы, инсулиномы, тиреотропиномы и др.). Если в паре выявлена мутация гена, которая связана с такими опухолями, генетик порекомендует тщательное амбулаторное наблюдение ребёнка с рождения у эндокринолога и гастроэнтеролога.
Рекомендации для пациентов, в чьей семье встречается такая опухоль, тоже не разработаны. Можно наблюдаться у эндокринолога и гастроэнтеролога, а по показаниям обращаться к онкологу. Сам риск снизить нельзя, но чем раньше будут выявлены изменения в организме и предпосылки для развития заболевания, тем больше шансов на успех от терапии.
Список литературы
Sato Y., Hashimoto S., Mizuno K. et al. Management of gastric and duodenal neuroendocrine tumors // World J Gastroenterol. — 2016. — № 30. — Р. 6817–6828.ссылка
Jensen R. T., Norton J. A. Endocrine tumors of the pancreas and gastrointestinal tract. Gastrointestinal and Liver Disease. — 9th edition. — Philadelphia: Saunders Elsevier, 2010.
Маев И. В., Андреев Д. Н., Кучерявый Ю. А. и др. Синдром Золлингера — Эллисона: пособие для врачей. — М.: Московский государственный медико-стоматологический университет имени А. И. Евдокимова, 2016. — 48 с.
Hain E., Coriat R., Dousset B., Gaujoux S. Management of gastrinoma // Presse Med. — 2016. — № 11. — Р. 986–991.ссылка
Wang K. A., Chou Y. H., Huang S. H. et al. Primary jejunal gastrinoma: a case report and review of the literature // World J Surg Onc. — 2015. — Vol. 13. ссылка
Маев И. В., Андреев Д. Н., Кучерявый Ю. А., Баркалова Е. В. Эволюция клинических представлений о синдроме Золлингера — Эллисона // Терапевтический архив. — 2014. — № 2. — С. 82–89.
Zollinger-Ellison syndrome (ZES) // Orhanet. [Электронный ресурс]. Дата обращения: 17.12.2024.
Sansone A., Lauretta R., Vottari S. et al. Specific and Non-Specific Biomarkers in Neuroendocrine Gastroenteropancreatic Tumors // Cancers (Basel). — 2019. — № 8. ссылка
Российская ассоциация эндокринологов. Акромегалия: клиника, диагностика, дифференциальная диагностика, методы лечения: клинические рекомендации. — М., 2014. — 36 с.
Ito T., Cadiot G., Jensen R. T. Diagnosis of ZollingerEllison syndrome: increasingly difficult // World J Gastroenterol. — 2012. — № 39. — Р. 5495–5503. ссылка
Иловайская И. А. Диарея как клинический маркер нейроэндокринных опухолей // Экспериментальная и клиническая гастроэнтерология. — 2018. — № 6. — С. 143–149.
Halászlaki С., Horváth H., Kiss L. et al. Verner-Morrison syndrome: a case study // Orv Hetil. — 2010. — № 27. — Р. 1111–1114. ссылка
Российское общество урологов. Почечная колика: клинические рекомендации. — М., 2021. — 42 с.
Дзеранова Л. К., Пигарова Е. А., Селиванова Л. С. и др. АКТГ-эктопический синдром при нейроэндокринной опухоли лёгкого // Хирургия. Журнал им. Н. И. Пирогова. — 2018. — № 9. — С. 46–51.
Боряк А. Л. Особенности метаболизма костной ткани, прогнозирование переломов позвоночника и местных инфекционных осложнений в послеоперационном периоде у женщин с постменопаузальным остеопорозом: дис. … к-та мед. наук: 14.03.03. — Донецк, 2021. — 112 с.
Маев И. В., Андреев Д. Н., Кучерявый Ю. А., Дичева Д. Т. Синдром Золлингера — Эллисона: современные аспекты диагностики и лечения // РЖГГК он-лайн. — 2014. — № 4. — С. 57–69.
Всемирная организация здравоохранения. Международная статистическая классификация болезней и связанных со здоровьем проблем. 10-й пересмотр (МКБ-10). — Женева, 1992.
Всемирная организация здравоохранения. Международная статистическая классификация болезней и проблем, связанных со здоровьем. 11-й пересмотр (МКБ-11). — Женева, 2022.
Raj N., Fazio N., Strosberg J. Biology and Systemic Treatment of Advanced Gastroenteropancreatic Neuroendocrine Tumors // Am Soc Clin Oncol Educ Book. — 2018. — Vol. 38. — P. 292–299. ссылка
Оганезова И. А., Попова Е. А., Бакулин И. Г. Современные возможности диагностики и лечения гастриномы: описание клинического случая // Профилактическая медицина. — 2021. — № 7. — С. 50–55.
Poblocki J., Jasinska A., Syrenicz A. et al. The Neuroendocrine Neoplasms of the Digestive Tract: Diagnosis, Treatment and Nutrition // Nutrients. — 2020. — № 5.ссылка
Wiedmann M. W., Mössner J. Safety and efficacy of sunitinib in patients with unresectable pancreatic neuroendocrine tumors // Clin Med Insights Oncol. — 2012. — Vol. 6. — P. 381–393. ссылка
Ворожцова И. Н., Павленко О. А., Лукьянёнок П. И., Коновалова Н. А. Пролактинома: этиологические, диагностические и терапевтические аспекты // Современные проблемы науки и образования. — 2016. — № 4.
Парфенов А. И. Четыре варианта патогенеза и терапии диареи // Терапевтический архив. — 2015. — № 12. — С. 5–12.
Лазебник Л. Б., Сарсенбаева А. С., Авалуева Е. Б. и др. Клинические рекомендации «Хронические диареи у взрослых» // Экспериментальная и клиническая гастроэнтерология. — 2021. — № 4. — С. 7–67.
Астафьева Л. И., Кадашев Б. А., Шишкина Л. В. и др. Тиреотропиномы и тиреотрофная гиперплазия (описание клинических случаев и обзор литературы) // Журнал «Вопросы нейрохирургии» имени Н. Н. Бурденко. — 2016. — № 3. — С. 82–90.
Yu F., Venzon D. J., Serrano J. Prospective study of the clinical course, prognostic factors, causes of death, and survival in patients with long-standing Zollinger-Ellison syndrome // J Clin Oncol. — 1999. — № 2. — Р. 615–630.
Панкратова Е. А., Шпрах З. С. Рецепторы к соматостатину: локализация и методы визуализации (обзор литературы) // Российский биотерапевтический журнал. — 2022. — № 1. — С. 10–20.
Классификация гастроэзофагеальной рефлюксной болезни // Сеченовский университет. Хирургия пищевода и желудка. [Электронный ресурс]. Дата обращения: 18.12.2024.
Карманные рекомендации для врачей по ведению пациентов с кислотозависимыми заболеваниями / под ред. О. Н. Минушкина. — М.: Группа Ремедиум, 2020.
Кирилюк М. Л. Болезнь Иценко — Кушинга. Современные подходы к диагностике и лечению (клиническая лекция) // Эндокринология: новости, мнения, обучение. — 2014. — № 1. — С. 54–67.
Охлобыстин А. В. Диагностика и лечение синдрома Золлингера — Эллисона // РМЖ. — 1998. — № 7. — С. 6–9.
Aslanian H. R., Sethi A., Bhutani M. S. et al. ASGE guideline for endoscopic full-thickness resection and submucosal tunnel endoscopic resection // VideoGIE. — 2019. — № 8. — P. 343–350. ссылка
Shao Q. Q., Zhao B. B., Dong L. B., Cao H. T., Wang W. B. Surgical management of Zollinger-Ellison syndrome: Classical considerations and current controversies // World J Gastroenterol. — 2019. — № 32. — P. 4673–4681.ссылка

