Определение болезни. Причины заболевания
Синдром Пьера Робена (Pierre Robin syndrome) — это порок развития, который сопровождается тремя характерными симптомами: расщелиной нёба, недоразвитием (микрогнатией) нижней челюсти и западением языка (глоссоптозом), из-за чего профиль человека становится похож на птичий. Иногда такой синдром диагностируют у пациентов и без расщелины нёба.
![Младенец с синдромом Пьера Робена [17] Младенец с синдромом Пьера Робена [17]](/media/bolezny/sindrom-pera-robena/mladenec-s-sindromom-pera-robena-17_s.jpeg?dummy=1762518763438)
Младенец с синдромом Пьера Робена [17]
Это заболевание открыл врач-стоматолог Пьер Робен в 1923 году. Сейчас его диагностируют примерно у одного ребёнка из 8500–30000 новорождённых [5].
Одной из основных проблем таких пациентов является нарушение дыхания, связанное с недоразвитием нижней челюсти и аномальным положением языка, который смещён кзади, из-за чего западает в глотку и перекрывает дыхательные пути.
Причины развития синдрома Пьера Робена
Исследователи выделяют сразу несколько причин заболевания: генетическую предрасположенность и внутриутробное сдавливание нижней челюсти плода. Иногда этот синдром выступает симптомом других болезней челюстно-лицевой области (ЧЛО) и пороков развития (например, синдрома Стиклера, Ди Джорджи, Тричера Коллинза, Патау или алкогольного синдрома плода) [3][5][6].
К факторам риска также относятся:
- наследственная отягощённость — если в семье есть случаи других болезней ЧЛО, это повышает риск развития синдрома Пьера Робена у ребёнка;
- механические препятствия в полости матки — к ним могут относиться рубцовые изменения, амниотические тяжи (волокнистые структуры, соединяющие плод с плацентой), опухоли и др.;
- недостаток места при многоплодной беременности — плоды сдавливают другу друга, что может привести к деформации челюсти;
- внутриутробные инфекции — способны нарушить нормальное развитие челюстно-лицевого аппарата;
- маловодие — может негативно сказаться на росте и развитии плода [9];
- дефицит фолиевой кислоты у беременной — фолиевая кислота играет ключевую роль в процессах клеточного деления и роста, поэтому её недостаток значительно повышает риск недоразвития челюсти и, как следствие, западения языка у ребёнка;
- влияние тератогенных факторов — воздействие неблагоприятных экологических условий, радиационного облучения или химических веществ также может привести к аномалиям развития челюстно-лицевого аппарата [4];
- мутации половых клеток (сперматозоидов и яйцеклеток);
- осложнённая или поздняя беременность.
Симптомы синдрома Пьера Робена
Симптомы синдрома Пьера Робена обычно становятся заметны практически сразу после рождения. У таких детей отмечается расщелина нёба, уменьшение нижней челюсти, смещение и опущение языка книзу в сторону глотки, «птичий профиль» [10][12]. После прорезывания зубов также наблюдается смещение окклюзионной плоскости — нарушение прикуса, при котором зубы верхней и нижней челюсти смыкаются неправильно.
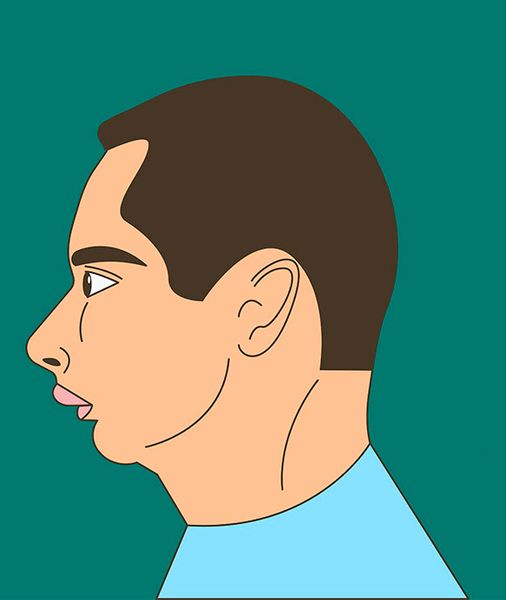
Птичий профиль
Всё это приводит к проблемам с дыханием и питанием. Например, повышается риск аспирации пищи, при которой она попадает в дыхательные пути, а не в пищевод, или асфиксии (удушья при глотании) [1]. Кроме того, у детей с синдромом Пьера Робена отмечается задержка развития и снижение темпов набора веса.
Дыхательные нарушения могут проявляться по-разному: возможны эпизоды как непродолжительного апноэ, так и длительной остановки дыхания (до 20 секунд), которая может произойти не только во сне. Тяжесть симптомов зависит от положения и смещения языка. Также у пациентов с синдромом Пьера Робена наблюдается гипоксия (недостаток кислорода) и гиперкапния (избыточное содержание углекислого газа в крови).
Из-за изменений во внутреннем ухе в 75 % заболевания наблюдается снижение слуха, в 60 % — его полная утрата [3][13]. У некоторых пациентов также возможны нарушения зрительного аппарата: врождённая катаракта и глаукома, буфтальм («бычий глаз»), мегалокорнеа (увеличение роговицы), микрофтальм (уменьшение глаза), высокая (сильная) миопия и отслойка сетчатки [14].
![Буфтальм [18] Буфтальм [18]](/media/bolezny/sindrom-pera-robena/buftalm-18_s.jpeg?dummy=1762518831775)
Буфтальм [18]
Примерно у половины детей с синдромом Пьера Робена наблюдаются проблемы с нервной системой, например гидроцефалия, эпилепсия или микроцефалия (уменьшение черепа). Однако эти проявления чаще встречаются при синдромальных формах, например в составе синдрома Стиклера или Патау. Изолированный синдром Пьера Робена редко сопровождается тяжёлыми неврологическими нарушениями.
Помимо всего прочего, возможно нарушение со стороны сердечно-сосудистой системы в виде сердечной недостаточности [3][5][7].
Патогенез синдрома Пьера Робена
Внутриутробное эмбриональное развитие ЧЛО начинается на 2–3-й неделе беременности. Между передним мозговым пузырём и сердечным выступом появляется углубление эктодермы (наружного зародышевого листка), которое называют первичной ротовой ямкой. Постепенно углубляясь, к концу третьей недели внутриутробного развития ротовая ямка достигает передней кишки, сформированной из эндодермы (внутреннего зародышевого листка), и соединяется с ней. Таким образом формируются передние отделы пищеварительного тракта.
На 2–3-й неделе внутриутробного развития по бокам головного конца эмбриона образуются жаберные, или глоточные, дуги. Первая дуга называется челюстной, или мандибулярной. Передние концы жаберной дуги раздваиваются, образуя таким образом 5 бугров, которые к концу 1-го месяца внутриутробного развития ограничивают ротовую ямку: выше всех расположен лобный, два верхнечелюстных — по бокам от него, два нижнечелюстных — снизу. В дальнейшем из верхнечелюстных отростков формируется верхняя челюсть, из нижнечелюстных — нижняя.

Жаберные дуги
На 7-й неделе лобный и два верхнечелюстных бугра сливаются, в результате чего образуется «первичное нёбо». Вторичное нёбо формируется чуть позже из пластинчатых выростов (нёбных отростков). Нёбные пластинки развиваются, срастаются друг с другом и носовой перегородкой по средней линии на 10–11-й неделе внутриутробного развития.
Врождённая расщелина нёба, характерная для синдрома Пьера Робена, возникает, если со 2-й по 11-ю неделю внутриутробного развития на плод воздействуют какие-либо вредоносные факторы [11][12]. Чем раньше произошло воздействие, тем хуже будет деформация.
Нижняя челюсть представляет собой парную кость, которая срастается примерно к концу 4-й недели внутриутробного развития. Однако рост нижней челюсти происходит на протяжении всей беременности, поэтому практически на любом этапе возможно замедление её роста [11].
В норме ребёнок рождается с младенческой нижней ретрогнатией, когда нижняя челюсть находится кзади от верхней. Это облегчает проход плода по родовым путям и позволяет выработать рефлекс сосания. Однако через некоторое время нижняя челюсть должна занять правильное положение, поэтому важно не пропустить момент, когда уже можно точно определить, что у ребёнка сформировалась именно микрогнатия.
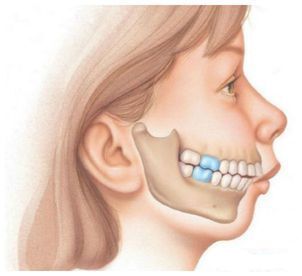
Микрогнатия нижней челюсти
Обычно изменения при синдроме Пьера Робена развиваются в определённом порядке: сначала под влиянием различных факторов нарушается развитие нижней челюсти (зачастую между 7-й и 11-й неделями внутриутробного развития), из-за чего язык располагается между нёбными пластинами и не даёт им срастись, формируя таким образом расщелину нёба [4][9].
Недостаточный рост нижней челюсти в сочетании с маленьким объёмом ротовой полости создаёт предпосылки для развития серьёзного заболевания — глоссоптоза [1]. Такое состояние характеризуется патологическим смещением языка назад, к задней стенке глотки, из-за чего ребёнку трудно вдыхать воздух. Это может привести к кислородному голоданию и другим опасным последствиям.
Классификация и стадии развития синдрома Пьера Робена
В зависимости от выраженности нарушения глотания и дыхания выделяют три степени тяжести синдрома Пьера Робена:
- Лёгкая — дыхание не нарушено, однако отмечаются небольшие трудности при кормлении младенца, которые устраняются консервативными методами в домашних условиях. У ребёнка также наблюдаются периодические эпизоды апноэ, которые проходят самостоятельно. Существенных осложнений, в том числе гипоксии и гиперкапнии, нет.
- Средняя — трудности дыхания и кормления выражены умеренно. Младенцу требуется стационарная помощь и зондовое питание. У него наблюдается более продолжительное апноэ, во время сна регистрируется умеренная гипоксия, но гиперкапнии нет. В целом такое состояние мешает ребёнку и ухудшает качество его жизни.
- Тяжёлая — новорождённому тяжело дышать (в некоторых случаях — невозможно), он не может питаться самостоятельно, поэтому ему устанавливают трахеостому и желудочный зонд. Наблюдается выраженное апноэ (от 20 секунд и более). При длительном выраженном апноэ пациенту может потребоваться сердечно-лёгочная реанимация. У такого ребёнка также наблюдается хроническая тяжёлая гипоксия, гиперкапния и сердечная недостаточность [1][5].
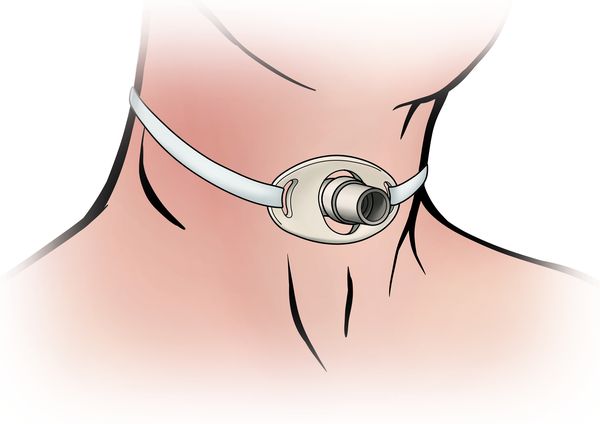
Трахеостома
Осложнения синдрома Пьера Робена
Осложнения заболевания разнообразны, но в основном они связаны с дыхательными нарушениями. Практически у всех детей с синдромом Пьера Робена наблюдаются различные речевые дефекты и нарушения произношения звуков: они поздно начинают говорить и часто неправильно произносят буквы «р», «л», «с», а также шипящие звуки.
Также у таких пациентов диагностируют неправильный прикус и рецидивирующие ушные инфекции, которые могут быть связаны с нарушениями во внутреннем ухе. На фоне приступов апноэ, продолжающейся гипоксии и гиперкапнии может развиться гипоксическая энцефалопатия, лёгочное сердце и нарушения сердечной деятельности.
Так как дети с расщелиной нёба не могут полноценно питаться, а также подвержены повышенному риску аспирации (в том числе слюны и желудочного сока), у них могут развиться расстройства пищеварения, аспирационная пневмония и гастроэзофагеальная рефлюксная болезнь (ГЭРБ). Кроме того, закупорка дыхательных путей повышает риск развития респираторного дистресс-синдрома.
Некоторые пациенты с синдромом Пьера Робена страдают от развивающейся тугоухости, ухудшения зрения и зубочелюстных нарушений окклюзии [3][8]. Кроме того, заболевание может вызвать неврологические симптомы, например умственную отсталость [15].
Диагностика синдрома Пьера Робена
В настоящее время синдром Пьера Робена диагностируют пренатально уже на первом триместре беременности. Если по каким-то причинам болезнь не выявили пренатально, сразу после родов диагноз становится очевиден.
Пациента с таким синдромом наблюдает челюстно-лицевой хирург, ортодонт, отоларинголог, невролог, логопед и генетик. При наличии других жалоб возможно обращение к смежным специалистам.
Основные методы диагностики:
- Рентген. Чтобы детально изучить анатомию ЧЛО, используют конусно-лучевую компьютерную томографию (КЛКТ) и ортопантомограмму (ОПТГ) челюстей. Проходимость дыхательных путей проверяют с помощью рентгена гортани и глотки.
- Эндоскопия гортани. В рамках этого метода исследуют гортань, носоглотку и верхние отделы трахеи. Врач оценивает степень перекрытия дыхательных путей, а также сформированность лор-органов.

Эндоскопия гортани
- Полисомнография. Этот метод позволяет определить частоту и длительность периодов остановки дыхания.
- Другие методы. Пациенту делают общий анализ крови, чтобы оценить общее состояние, проводят дыхательные пробы, пульсоксиметрию и проверяют степень насыщение крови кислородом. Также врачи оценивают профиль лица ребёнка.
Дифференциальную диагностику проводят с изолированной микрогнатией нижней челюсти и расщелиной нёба (если других признаков болезни, кроме этих симптомов, нет), синдромами Стиклера, Ди Джорджи, Тричера Коллинза, Патау, а также с алкогольным синдромом плода [1][5][8].
Лечение синдрома Пьера Робена
Стратегия лечения при синдроме Пьера Робена разнообразна и зависит от выраженности нарушений дыхания и пищеварения.
Консервативное лечение
При лёгкой степени апноэ ребёнка выкладывают на живот или на бок с приподнятой или зафиксированной головой, чтобы язык и нижняя челюсть были выдвинуты вперёд [9].
Устойчивую закупорку дыхательных путей помогает устранить назофарингеальный воздуховод — гибкая трубка, которую через нос проводят в носоглотку. Он предотвращает западение языка, обеспечивая свободный доступ воздуха в глотку. При тяжёлой степени синдрома может понадобиться подключение пациента к аппарату искусственной вентиляции лёгких.
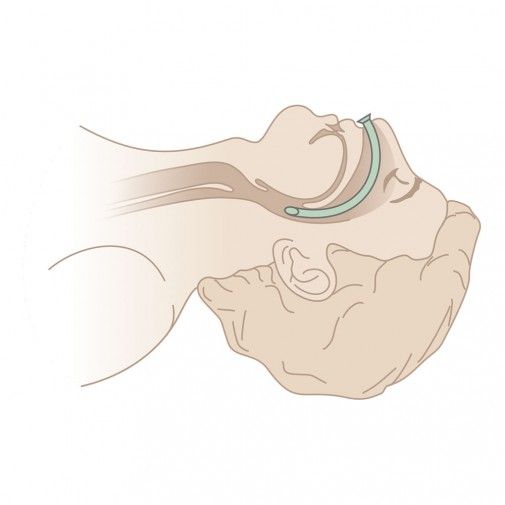
Назофарингеальный воздуховод
Если ребёнок не может питаться сам, кормление проводят через назогастральный зонд, с помощью которого гибкую трубку вставляют нос и через пищевод доставляют пищу в желудок.
Однако консервативная терапия не способна устранить все симптомы заболевания и направлена лишь на облегчение состояния пациента, поэтому даже при лёгкой степени синдрома врачи предпочитают операционный метод лечения [1][5].
Хирургическое лечение
План лечения разрабатывают в соответствии с клиническими проявлениями. Обычно последовательность операций выглядит так:
- Глоссопексия (в первые дни жизни, но не позднее 3-й недели) — проводят в том случае, если младенец не может дышать. Язык фиксируют к нижней губе или альвеолярному отростку. Через некоторое время швы рассасываются, и язык сам выдвигается вперёд.
- Компрессионно-дистракционный остеосинтез (нет ограничений по возрасту) — кости нижней челюсти распиливают и плотно прижимают друг к другу. Через 5–6 дней костные фрагменты начинают разводить со скоростью около 1 мм в сутки, благодаря чему между ними образуется костная мозоль (новая кость). Это позволяет ребёнку дышать самостоятельно уже на 6–7-й день с начала дистракции (растяжения). Однако полноценное самостоятельное питание возможно гораздо позже, уже к моменту окончания дистрации — примерно через 3 месяца. По окончании лечения аппарат удаляют [1][5].
- Велофарингопластика (в 6–8 месяцев) — мягкое нёбо соединяют с задней стенкой глотки с помощью лоскута из слизистой оболочки, подслизистой основы и мышц. Это позволяет восстановить анатомию и функциональность мягкого нёба.
- Уранопластика (в 12–18 месяцев) — устраняют расщелину твёрдого нёба, а также другие дефекты и деформации.
- Ортодонтическое лечение — включает в себя ношение брекетов, элайнеров и ретейнеров.
Если расщелины нет, 1 и 2-й этапы пропускают. В некоторых случаях расщелину закрывают с помощью ортодонтической пластинки, которая также давит на корень языка, тем самым выдвигая его вперёд [2].
Основное преимущество хирургического лечения, в частности компрессионно-дистракционного остеосинтеза, заключается в его эффективности: хороший результат отмечают в 90 % случаев, удовлетворительный — в 6,3 %, отрицательный — в 3,8 % [5].
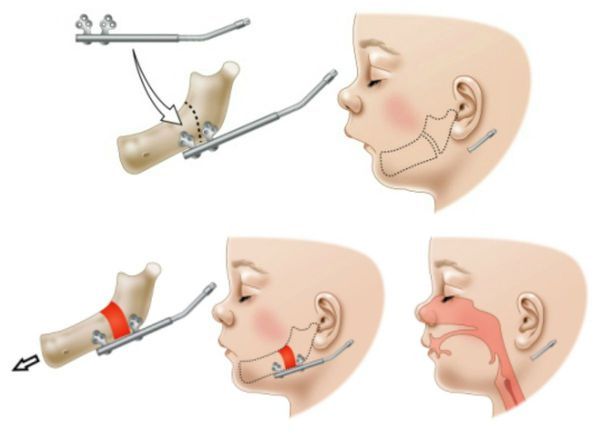
Компрессионно-дистракционный остеосинтез
Показания к применению оперативного вмешательства:
- тяжёлая и средняя степени нарушения дыхания;
- невозможность самостоятельного питания;
- лёгкая степень нарушения дыхания у новорождённых (операция предотвращает ухудшение ситуации и переход в среднюю и тяжёлые степени тяжести).
В последнее время приобретает популярность инновационный метод лечения с помощью специальной PEBP-пластинки (Pre-epiglottic baton plate) — съёмной нёбной пластинки из акриловой пластмассы с ортодонтическим пелотом (небольшим выступом) сзади нёба и двумя металлическими лигатурами (проволоками). Её изготавливает врач-ортодонт по ортодонтическим слепкам, после чего устанавливает пациенту примерно на год. Раз в сутки её нужно снимать и промывать проточной водой [2].
![PEBP-пластинка [16] PEBP-пластинка [16]](/media/bolezny/sindrom-pera-robena/pebp-plastinka-16_s.jpeg?dummy=1762519316581)
PEBP-пластинка [16]
Согласно европейским исследованиям, этот метод особенно эффективен при лёгкой и умеренной закупорке дыхательных путей [19]. Она помогает улучшить дыхание и изменить положение языка, благодаря чему нормализуется уровень кислорода в крови и частота сердечных сокращений.
Прогноз. Профилактика
Прогноз заболевания благоприятный: большинство пациентов с синдромом Пьера Робена проходят лечение, которое даёт хороший результат. Однако важно понимать, что, даже после окончания компрессионно-дистракционного остеосинтеза, ребёнку приходится ещё долго лечиться у других специалистов: ортодонта, логопеда и невролога [3].
Профилактика синдрома Пьера Робена
Чтобы снизить риск рождения ребёнка с таким диагнозом, рекомендуется проходить тщательное обследование во время беременности, исключить воздействие тератогенных факторов и восполнить все дефициты витаминов.
Если в семье у кого-то уже есть подобный синдром, необходимо проконсультироваться с генетиком. Так как в этом случае риск заболевания повышен, беременной важно вовремя делать все генетические и ультразвуковые пренатальные скрининги [3].
Чтобы не допустить развития серьёзных осложнений, важно следить за тем, чтобы у ребёнка не было аспирации, закупорки дыхательных путей, апноэ, гипоксии и гиперкапнии [5][9].
Список литературы
Комелягин Д. Ю., Дубин С. А., Владимиров Ф. И., Петухов А. В. и др. Лечение детей с синдромом Пьера Робена // Здоровье мегаполиса. — 2021. — № 3. — С. 35–53.
Горячкина Ю. А., Горячкин А. М. Лечение младенцев с синдромом Пьера Робена с применением ортодонтического аппарата PEBP (pre-epiglottic baton plate) // Стоматология. — 2020. — № 6. — С. 29–32.
Кириллова Л. Г., Ткачук Л. И., Шевченко А. А., Силаева Л. Ю. и др. Синдром Пьера Робена у детей // Международный неврологический журнал. — 2010. — № 3. — С. 106–109.
Дудник О. В., Мамедов А. А., Билле Д. С., Чертихина А. С. и др. Особенности этиологии и патогенеза расщелины губы и нёба челюстно-лицевой области // Врач. — 2021. — № 2. — С. 16–22.
Комелягин Д. Ю., Дубин С. А., Владимиров Ф. И., Петухов А. В. и др. Лечение детей с синдромом Пьера Робена: клинические рекомендации. — М.: Департамент здравоохранения города Москвы, 2020. — 28 с.
Айдан Б. Б. Синдром Пьера Робена // Российский педиатрический журнал. — 2025. — № 1S. — С. 14.
Жуковская Ю. А., Басаргина П. С., Никитчук А. Р. Клиническое наблюдение синдрома Пьера Робена // Актуальные проблемы экспериментальной и клинической медицины. — 2023. — С. 183–184.
Главацкая Е. Н., Зверко В. Л., Прибушеня О. В., Барановская Е. В. и др. Клиническое наблюдение семейного случая генетического синдрома, включающего аномалии Пьера Робена // Актуальные вопросы акушерства и гинекологии. — 2021. — С. 28–31.
Baxter D., Shanks A. L. Pierre Robin Syndrome // StatPearls. — 2023.ссылка
Varadarajan S., Balaji T. M., Raj A. T., Gupta A. A. et al. Genetic Mutations Associated with Pierre Robin Syndrome/Sequence: A Systematic Review // Molecular Syndromology. — 2021. — № 2. — P. 69–86. ссылка
Исаков Ю. Ф., Дронов А. Ф. Детская хирургия: национальное руководство. — М.: ГЭОТАР-Медиа, 2009. — 1168 с.
Тимофеев А. А. Руководство по челюстно-лицевой хирургии и хирургической стоматологии. — Киев: Червона Рута-Турс, 2002. — 1024 с.
Козлова Е. В., Козлов В. В., Пашкова И. А., Пашков А. А. Секвенция Пьера Робена — ранний диагностический признак синдрома Стиклера (клинический случай) // Российский вестник перинатологии и педиатрии. — 2014. — № 4. — С. 112–116.
Сопутствующая врождённой глаукоме патология глаз: методические рекомендации // Eyepress. [Электронный ресурс]. Дата обращения: 07.11.2025.
Гуляева Л. В., Коляда Ю. В., Кудинов В. А. Синдром Пьера Робена — междисциплинарная проблема // Детская оториноларингология. — 2019. — № 3. — С. 50–52.
Buchenau W., Wenzel S., Müller-Hagedorn S., Urschitz M. S. et al. Caring for Infants with Robin Sequence Treated with the Tübingen Palatal Plate: A Review of Personal Practice // Children. — 2023. — № 10. — Р. 1628.ссылка
Sesenna Е., Magri A. S., Magnani C., Brevi B. C. Mandibular distraction in neonates: Indications, techniques, results // Ital J Pediatr. — 2012. — Vol. 38. — Р. 7. ссылка
Feroze K. B., Blair K., Patel B. C. Buphthalmos // StatPearls. — 2025. ссылка
Poets C. F., Maas C., Buchenau W. еt al. Multicenter study on the effectiveness of the pre-epiglottic baton plate for airway obstruction and feeding problems in Robin sequence // Orphanet J Rare Dis. — 2017. — № 1. — Р. 46.ссылка

