Определение болезни. Причины заболевания
Воронкообразная деформация грудной клетки (ВДГК) (впалая грудь, воронкообразная грудь, грудь сапожника, ресtus ехсаvatum) — это тяжелый порок развития передней грудной стенки, представляющий собой различные по форме и глубине западения грудины с вовлечением грудино-реберных хрящей и ребер. Это приводит к снижению объема грудной клетки, смещению и сдавлению органов загрудинного пространства, к заметному косметическому дефекту, выраженным функциональным изменениям со стороны сердца и легких. Среди врожденных деформаций грудной клетки воронкообразная деформация составляет 91%. Мальчики болеют в 4 раза чаще девочек.
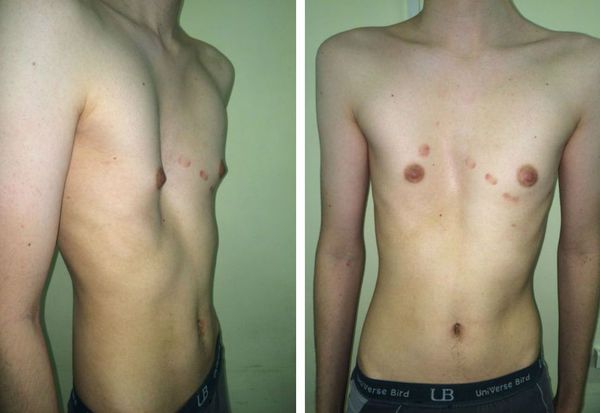
Западение грудной клетки
Данный вид деформации грудины известен человечеству издавна. Первые упоминания в литературе встречаются в 1594 году, а первое детальное описание ВДГК сделал в 1870 году H. Eggel.
Этиология воронкообразной деформации грудной клетки остается до конца не изученной. Большинство авторов в своих работах ссылаются на диспластический процесс как основную причину возникновения деформации, что подтверждает повышенная экскреция оксипролина как продукта деградации коллагена.
Дисплазия соединительной ткани — это генетически детерминированный процесс, обусловленный мутацией генoв, которые отвечают за синтез коллагеновых структур. Вследствие различных мутаций в генах происходит неправильное формирование коллагеновых цепей, что приводит к слабости при механических воздействиях на основные разновидности соединительной ткани — хрящи и кости.
Почти 65% пациентов с данной патологией имеют родственников с деформацией грудной клетки в анамнезе. Учитывая системное нарушение коллагеновых структур, у пациентов с воронкообразной деформацией грудной клетки наблюдается астеническое телосложение, удлиненные конечности, различные формы нарушения осанки, плоскостопие, арахнодактилия, гипермобильность суставов, миопия, слабо развитая мышечная система, нарушение прикуса и т. д. Нередко у пациентов с ВДГК имеется сопутствующая различная синдромальная патология, например, синдром Элерса-Данлоса, Марфана, Сиклера, Жена, нейрофиброматоз I типа.
Основная причина западения грудины — чрезмерный рост грудино-реберных хрящей, которые опережают рост ребер, тем самым вворачивая грудину внутрь грудной клетки.[1][3]
Симптомы воронкообразной грудной клетки
Больные отмечают «чувство сердцебиения» в состоянии покоя, быструю утомляемость при малых физических нагрузках, одышку, реже — дисфагические и дыхательные нарушения, связанные со степенью деформации грудино-реберного комплекса.
Дети с ВДГК часто болеют различными респираторными заболеваниями, что, во-первых, обусловлено хроническим сдавлением органов загрудинного пространства, а во-вторых, связано с этиологией заболевания. Дисплазия соединительной ткани носит полиорганный характер и влияет не только на хрящи и ребра, но и на бронхолегочную ткань в частности. Пораженная дисплазией легочная ткань и бронхиальное дерево подвержены таким заболеваниям, как бронхоэктазы, трахеобронхомаляция, бронхообструктивный синдром, аномалия развития бронхиального дерева. У пациентов этой группы часто встречаются малые аномалии развития сердца, которые проявляются в виде пролапса митрального клапана, открытым овальным окном, дополнительными хордами в камерах сердца.[5][7]
Патогенез воронкообразной грудной клетки
У 79% детей, страдающих ВДГК, деформация определяется на первом году жизни, когда заболевание проявляется «симптомом парадокса при вдохе». Отмечается западение грудины во время вдоха в проекции мечевидного отростка. Функциональные нарушения на первом году жизни обычно не проявляются, что сглаживает клиническую картину заболевания, но общепризнанно считать ВДГК врожденным пороком.
В периоде новорожденности втяжение в области грудины может быть незначительным, проявляется ригидностью грудино-реберного комплекса, втяжением при акте дыхания и визуально не привлекать к себе внимания педиатров и родителей, в возрасте 4-6 лет ригидность исчезает, и деформация постепенно начинает прогрессировать. Основным возрастом для манифестации воронкообразной деформации грудной клетки у детей является пубертатный период. Как правило, родители отмечают активный рост ребенка, одновременно сопровождающийся усилением западения грудины и грудино-реберных хрящей, ранее остававшимися без внимания.[8]
Классификация и стадии развития воронкообразной грудной клетки
Существует множество классификаций воронкообразной деформации грудной клетки. С развитием малоинвазивной хирургии эти классификации добавляются и уточняются. Наиболее анатомически емкая и полная классификация, используемая нами, классификация по Park. На основании РКТ органов грудной клетки выделяется две группы:
I с симметричной деформацией
- классическая (IА);
- симметричная деформация с широким плоским типом (IВ);
II с ассиметричной деформацией
- эксцентричная локальная (IIA1);
- ассиметричная эксцентричная с широким плоским типом (IIA2);
- ассиметричная эксцентричная с глубоким типом, или так называемый Grand Canyon (IIA3);
- ассиметричная с несбалансированным типом (IIB).
Существует достаточное количество шкал оценки степени деформации. Мы использовали общеевропейскую шкалу, принятую ассоциацией торакальных хирургов, занимающихся воронкообразной деформацией грудной клетки, для оценки степени деформации и выставлении показаний к операции — шкалу Халлера, или индекс Халлера (Haller Index (HI). Этот индекс представляет собой отношение поперечного грудного размера к передне-заднему размеру, в норме равен 2,5. В нынешнее время практически все ведущие специалисты в области воронкообразной деформации грудины считают индекс Халлера основным диагностическим показателем и критерием выбора в показаниях к операции. При превышении показателя 3,2-3,5 показано оперативное лечение.
Одним из наиболее известных и применяемых методов оценки степени деформации является предложенный в 1962 году индекс Гижицкой. Индекс представляет собой отношение наименьшего (А) стерно-вертебрального расстояния к наибольшему (В), и характеризует 3 степени деформации.[3]
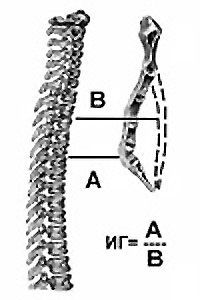
Индекс Гижицкой
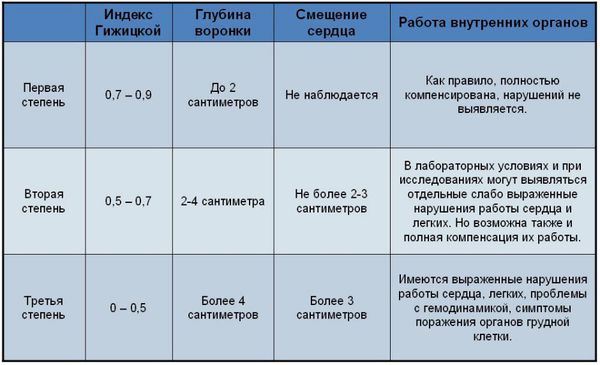
Степени деформации грудной клетки
Осложнения воронкообразной грудной клетки
Зачастую ВДГК как фенотипическое проявление дисплазии соединительной ткани влияет не только на форму и внешний вид грудины и грудинно-реберного комплекса в частности, но и вызывает изменения со стороны сердечно-легочной системы. Со стороны легких у пациентов с выраженной воронкообразной деформацией грудной клетки отмечается снижение ЖЕЛ (жизненная емкость легких) до 25%, что влияет на общее состояние ребенка, его быструю утомляемость и плохое развитие. Характерны частые обструктивные заболевания, ОРВИ, бронхиты.
У детей с воронкообразной деформацией грудной клетки в 70% случаев выявлены патологические изменения на ЭКГ. Наиболее часто встречаются нарушения в проводимой системе сердца и изменения положения электрической оси, гипертрофия миокарда как следствие компрессии, сдавления камер сердца, пролапс или недостаточность клапанов, дополнительные хорды в камерах сердца, расширение аорты и т. д.[3]
Диагностика воронкообразной грудной клетки
Для оценки степени деформации, выбора метода коррекции и объема оперативного вмешательства необходимо провести полный комплекс диагностических исследований, включающий:
- сбор жалоб;
- анамнеза;
- осмотр;
- общие клинические анализы (развёрнутый анализ крови, общий анализ мочи, исследование кала и др.);
- биохимические анализы крови (определение в крови уровня К, Na, сахара, кальция, билирубина и его фракций, АЛТ, ACT, амилазы и др.).
Помимо общих клинических и биохимических анализов, комплекс обследования включает в себя:
- проведение клинического осмотра пациента;
- эхокардиографию;
- исследования функций внешнего дыхания или бодиплетизмография;
- рентген органов грудной клетки в прямой и боковой проекции;
- компьютерная томография с 3-D реконструкцией.
Клинический осмотр
Для установления диагноза воронкообразной деформации грудной клетки достаточно внешнего осмотра. Деформация, как правило, начинается от места соединения рукоятки с телом грудины с наибольшей выраженностью на уровне соединения с мечевидным отростком и распространяется на III – VIII ребра, чаще всего включая обе реберные дуги. Ширина и глубина варьируют в разных пределах. Часто реберные дуги развернуты, и эпигастральная область выбухает.
При вовлечении в ее общую площадь и костной части ребер по сосковой или передней подмышечной линии, помимо первичной (воронкообразной) выявляется вторичная — плоская грудная клетка, в целом формируется плоско-воронкообразная грудь. На фоне воронкообразной деформации отмечаются острый эпигастральный угол и парадоксальное дыхание. Больные с ВДГК имеют заметно выраженную астеническую конституцию за счет диспропорции массы и роста, кифосколиотическую установку туловища, общую гипотонию мышц. При детальном физикальном обследовании выявляются разной степени выраженности признаки соединительно-тканой дисплазии: гипермобильность суставов, повышенная эластичность кожи, плоскостопие и др. В диагностике синдромальных форм ВДГК используется клинико-генетическое исследование.
Рентгенография
Одним из важных исследований, но менее актуальным в последнее десятилетие, в предоперационном периоде является рентгенография органов грудной клетки в прямой и боковой проекциях. В прямой проекции можно определить патологию со стороны костной системы, ребер, грудины и легочной ткани. Боковая рентгенография, до появления и широкого внедрения в практику современных компьютерных рентген-технологий, широко применялась и использовалась для определения степени деформации грудины.
Функции внешнего дыхания
С целью выявления тяжести поражения дыхательной системы всем пациентам с ВДГК необходимо проведение исследования функции внешнего дыхания. При ВДГК наиболее значимым показателем внешнего дыхания является функциональная остаточная емкость легких.
Функция внешнего дыхания оценивается с помощью спирографического метода на компьютерном спирографе с графической фиксацией и записью кривой поток-объема при выполнении маневра форсированного выдоха и регистрацией показателей. Диагностика вентиляционных нарушений основана на оценке отклонения от нормы показателей, выраженных в процентах от должной величины.
Определяются следующие функциональные параметры:
- объем жизненной емкости легких (ЖЕЛ, %);
- объем форсированной жизненной емкости легких
- (ФЖЕЛ, %);
- объем форсированного выдоха за 1 секунду (ОФВ, %);
- пиковая объемная скорость (ПОС, %);
- максимальная объемная скорость 25% от форсированной жизненной емкости (МОС25%);
- максимальная объемная скорость 50% от форсированной жизненной емкости (МОС5о%);
- максимальная объемная скорость 75% от форсированной жизненной емкости (МОС75%).
При проведении спирометрических проб у больных с I-II степенью деформации отмечаются рестриктивные изменения функции внешнего дыхания, а при III степени деформации более тяжелые изменения по реструктивно-обструктивному типу. При этих изменениях происходит снижение вентиляционно-обструктивных соотношений. Это ведет к хроническому гипоксическому состоянию тканей и гиперфункциональным изменениям в миокарде и в последующем может прогрессировать.
Кардиография
Зачастую ВДГК как фенотипическое проявление дисплазии соединительной ткани влияет не только на форму и внешний вид грудины и грудино-реберного комплекса в частности, но и вызывает изменения со стороны сердечно-сосудистой системы. ЭКГ — один из наиболее доступных и простых методов обследования сердечно-сосудистой системы. ЭХО-КГ, помимо ЭКГ, — один из наиболее важных методов обследования ССС. Исследование проводится с целью определения формы и положения сердца, изучения строения клапанной системы, межпредсердной и межжелудочковой перегородок, состояния сердечной мышцы, сдавления камер сердца, непосредственно состояния правого и левого желудочков, выявления малых аномалий сердца.
Компьютерная томография
Наиболее полным, емким, информативным, доступным методом обследования является мультиспиральная компьютерная томография с 3D реконструкцией грудной клетки. При проведении данного обследования появляется полное понимание взаимоотношения костно-хрящевого каркаса и органов средостения. Нередко выявляется сопутствующая патология как в костно-хрящевом каркасе так и с стороны легочной ткани, к примеру, «реберная вилка» или расщепление ребра, буллы верхушки легкого. Анатомическая ориентированность помогает осуществить безопасный вход в плевральную полость, не травмировав сердце и дополнительные внутриплевральные сосуды. С учетом формы и степени деформации появляется возможность моделирования положения и количества корригирующей пластины. С помощью 3D моделирования возможно оценить точку максимальной депрессии, тем самым выбрать нужное межреберье для установки корригирующей пластины с целью достижения наилучшего косметического и физиологического результата, выставить медицинские показания для коррекции грудной клетки.
Лечение воронкообразной грудной клетки
Cегодня существует более 100 разновидностей оперативного лечения воронкообразной деформации грудной клетки. Основоположниками в этой области являются Ludwig Meyer и Ferdinand Sauerbruch, которые первыми описали методики оперативного лечения воронкообразной деформации грудной клетки, сочетая наружное вытяжение, стернотомию и остеотомию деформированных ребер в 1911 и 1920 годах соответственно. Основным принципом хирургического лечения являлось удаление второй и третей пары грудинно-реберных хрящей. В методике F.Sauerbruch выполнялась резекция реберных хрящей от третьей до седьмой пары, с последующей стернотомией, мобилизацией подмечевидной связки и наложением тяги. Однако этот метод не увенчался успехом и признанием в широких хирургических кругах из-за неудовлетворительного косметического результата. Золотым стандартом в хирургическом лечении воронкообразной деформации грудной клетки с 1949 по 2000 гг. являлась техника оперативной коррекции по M. Ravitch, которая обладала лучшим косметическим результатом без использования каких-либо тяг. Техника основывалась также на резекции деформированных реберных хрящей от реберной дуги до третьих (реже — вторых) ребер включительно через большой поперечный или мерседес-образный разрез с отсепаровкой мышц, последующей поперечной стернотомией и ретростернальной поддержкой грудины металлоконструкцией. Безусловно операция являлась крайне травматичной, с обширной кровопотерей, продолжительностью от 160 до 200 минут, и обладала рядом осложнений как ранних, так и отсроченных, таких как пневмонии, развившиеся вследствие длительного ателектаза легкого, грубый послеоперационный рубец, рестрикция грудной клетки, развившаяся в связи с обширной резекцией реберных хрящей, рецидивы, повторные оперативные резекции хрящей. К ранним можно отнести послеоперационные гидротораксы, вызванные аллергической реакцией плевры на травму и инородное тело — пластину, гематораксы, пневмотраксы, подкожные эмфиземы и гематомы. Этот метод операции сопровождался нестабильностью грудной клетки и подвижностью грудины.
В конце ХХ века началась эпоха эндохирургии. В 1998 году американский хирург D. Nuss опубликовал десятилетний опыт лечения ВДГК по собственной малоинвазивной методике торакопластики, получившей название Minimally invasive repair of pectus excavatum (MIRPE), или просто Nuss procedure. Этот метод сразу вышел на первое место в торакопластике ВДГК, стал самым малоинвазивным, менее травматичным, и менее продолжительным по времени операции. Но, несмотря на то, что старая школа торакальных хирургов и ортопедов использует до сих пор методики открытых торакопластик, операция Насса считается золотым стандартом в лечении воронкообразной деформации грудной клетки у детей. Данная методика позволяет непосредственно на операционном столе добиться хорошего косметического результата, избежать травмирующей отсепаровки мышц передней грудной клетки, резекции грудино-реберных хрящей и стернотомии, что снижает риск возможных интра- и послеоперационных осложнений, а также формирования грубых и уродующих послеоперационных рубцов, встречающихся при открытых торакопластиках. Кроме того, значительно сокращается время операции и минимизируется интраоперационная кровопотеря. Удовлетворительный косметический результат достигается при помощи проведенной загрудинно-коррегирующей пластины через два минимальных разреза кожи по переднеподмышечным линиям.
На сегодняшний день основной выбор при торакопластике у пациентов с ВДГК хирурги отдают предпочтение в большинстве случаев методике Дональда Насса. Торакопластика по Нассу завоевала всеобщее признание среди ортопедов-хирургов, торакальных хирургов и особенно у детских хирургов. Преимущество методики заключается в удовлетворительном косметическом результате в сравнении с открытыми торакопластиками, относительной простоте выполнения операции, сокращении операционного времени, а соответственно и количестве наркоза, уменьшении интраоперационных осложнений, отсутствии уродующих послеоперационных рубцов. Как показали опросы пациентов, перенесших торакопластику по Нассу, после удаления пластины, они отмечали улучшение качества жизни и хороший косметический результат.[11][12]
Для выполнения этих операций необходимы пластины из титанового сплава либо из стали. Важно, чтобы пластины были прочными и идеально полированными. Пластина должна выдерживать большое давление грудины, особенно высокое у детей старшего возраста и подростков. Все края и поверхности пластин должны быть идеально гладкими и полированными, чтобы уменьшить силу трения при проведении и перевороте, тем самым предотвратить возможность повреждения органов и тканей.[13]
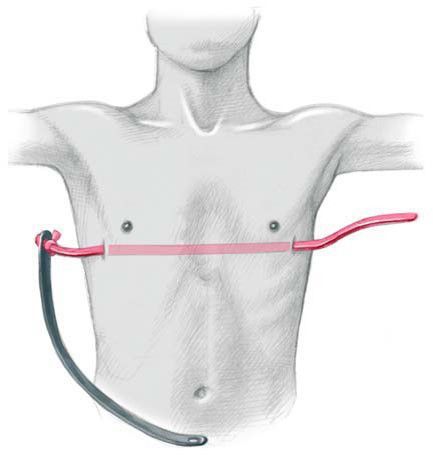
Торакопластика по Нассу с использованием пластины
Операция производится под комбинированным эндотрахеальным наркозом в сочетании с эпидуральной аналгезией. Положение больного на спине. Руки отведены под 90 градусов или приведены к туловищу в случае положения больного на ортопедической подушке. Маркером отмечается дно воронки, самые выступающие точки в проекции наибольшей депрессии грудины, производится разметка межреберий, отмечаются места точек входа и выхода в плевральные полости с каждой стороны и места будущих разрезов, как правило, это проекция IV или V межреберья. Кожные разрезы производятся на боковых поверхностях грудной клетки параллельно ходу ребер длиной до 3 см. Грудные мышцы отслаиваются от ребер, формируются подкожно-мышечные тоннели. В VI межреберье по среднеподмышечным линиям устанавливаются торакопорты 5 мм, накладывается карбокситоракс. При помощи интрадюсера тупым способом прокалывается грудная стенка справа, чуть медиальнее самой выступающей вперед части ребер. Под контролем торакоскопа интрадюсер вводится в плевральную полость и подводится к грудинно-перикардиальной связке или межплевральной перегородке. Плавными движениями под тщательным видеоконтролем производится разделение связки и проведение интрадюсера в левую плевральную полость. При деформации IIА3 и IIB степени во время проведения проводника через средостенье крайне важно, чтоб интрадюсер не касался перикарда во избежание его травматизации. Торакоскоп переставляется в левый порт и под видеоконтролем с мануальной асситенцией через прокол грудной стенки выводится наружу. К концу интрадюсера фиксируется силиконовая трубка, и он извлекается в обратном порядке. К грудной клетке прикладывается металлический шаблон и мануально изгибается по наиболее анатомической форме грудной клетки. Затем изгибается корригирующая пластина по форме заготовленного шаблона. Конец пластины фиксируется к силиконовой трубке справа. Проведение пластины осуществляется путем тракции за силиконовую трубку слева направо и поступательного движения пластины справа налево вдоль сформированного тоннеля выпуклой стороной к позвоночнику. Затем пластина переворачивается на 180º.[14][15][16]
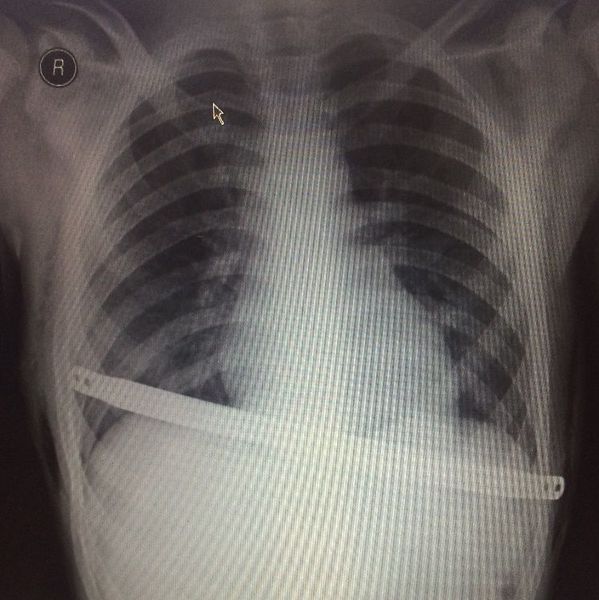
Установленная пластина на рентгенограмме
Давление пластины на заднюю поверхность грудины в месте наибольшей деформации вызывает коррекцию грудино-реберного комплекса сразу же после ее переворота. С учетом увеличения грудной клетки ребенка по мере роста необходимо оставлять концы пластины на 0,5 – 0,8 см от грудной стенки во избежание рестрикции грудной клетки в месте стояния пластины. Концы пластины фиксируются к ребрам ранее проведенной нитью PDS-II 1/0 и укрываются мышцами. После контрольного осмотра плевральных полостей через торакопорты вводятся силиконовые дренажи, погружаются в емкости с физраствором. На этапе ушивания мышц анестезиолог проводит форсированное раздувание легких для удаления воздуха из плевральных полостей. В момент прекращения поступления воздуха из плеваральных полостей дренажи удаляются, раны ушиваются наглухо с оставлением подкожных дренажей. На кожу накладываются косметические швы. Ребенок из операционной переводится в хирургическое отделение. В современной медицине, пролонгированное использование эпидуральной анестезии и малотравматичность операции Насса позволяет избежать применения в послеоперационном периоде наркотических анальгетиков. Эти же факторы позволяют начинать раннюю активизацию пациентов в первые сутки после операции. Во избежание ранних послеоперационных осложнений пациентам через 8-10 часов после операции выполняется контрольный рентген органов грудной клетки в палате лежа. Ранняя активизация пациента, физиолечение, дыхательная гимнастика, ЛФК приводит к сокращению срока пребывания в стационаре, который составляет в среднем 7 суток. Использование антибактериальной терапии цефалоспоринового ряда в послеоперационном периоде позволяет избежать нежелательных осложнений в виде нагноения раны, различных плевритов, пневмонии. Как правило, курс составляет не более 7 дней, при сохраняющемся нейтрофилезе антибактериальную терапию следует продолжить. В таких случаях при отсутствии осложнений пациент выписывается домой с назначением пероральных антибиотиков.
В связи с установкой инородного тела — пластины в организм пациента, показано назначение НПВС длительным курсом. Длительность назначения НПВС контролируется общим анализом крови, при сохраняющемся эозинофилезе, повышенном СОЭ терапию следует продолжить.
Прогноз. Профилактика
Эффективность коррекции воронкообразной деформации можно наблюдать уже непосредственно на операционном столе. Незначительных дефектов грудной клетки в виде небольших «ямок», западения опорного ребра, выпирающей реберной дуги, которые наблюдаются в послеоперационном периоде, не стоит остерегаться. С возрастом, при физических нагрузках и ростом грудной клетки практически все дефекты самостоятельно корригируются либо «прикрываются» мышечной массой. По истечении периода реабилитации пациенты отмечают резкое улучшение самочувствия, пропадает чувство «ощущения сердцебиения», пациенты становятся более выносливыми и могут переносить большие физические нагрузки, что является основным показателем эффективности выполненной операции.
Рентгенография органов грудной клетки в двух проекциях каждые 1-3-6 месяцев позволяет избежать ранних послеоперационных осложнений, отметить рост грудной клетки, заметить возможное смещение пластины по оси, умеренную миграцию и дать нужные рекомендации.
Через полгода после операции большинство пациентов отмечают активный рост и прибавку к массе тела. Это связано с тем, что ткани начинают больше и лучше насыщаться кислородом, и пациент перестает пребывать в состоянии «хронической гипоксии». Помимо того, у пациентов данной группы после операции выравнивается психоэмоциональный фон. Они становятся более контактными и лучше социализируются.
Список литературы
Кондрашин Н.И. Врожденная воронкообразная деформация грудной клетки у детей. Дисс. Д.м.н. 1965
Павлов А.А. Хирургическая коррекция воронкообразной деформации грудной клетки методом Насса. Дисс. К.м.н. 2005
Урмонас В.К., Кондрашин Н.И. Воронкообразная деформация грудной клетки у детей. Вильнюс: Моклас, 1983
Савельева М.С., Разумовский А.Ю. Торакопластика по D. Nuss и ее модификация в разных странах Детская хирургия, 2014.-N 1.-С.34-38
Рудаков С.С. Изолированные и синдромальные дефекты развития грудной клетки и их лечение. Дисс. Д.м.н. 1988
Злотников Е.Н. Оптимизация хирургического лечения воронкообразной деформации грудной клетки у детей. Дисс. К.м.н.2011
M.J. Cartoski, D. Nuss, M.J. Goretsky, V.K. Proud, D.P. Croitoru, T. Gustin, et al. Classification of the dysmorphology of pectus excavatum J Pediatr Surg, 41 (2006), pp. 1573–1581A. Creswick, M.W. Stacey, R.E. Kelly Jr., T. Gustin, D. Nuss, H. Harvey, et al. Family
Study of the inheritance of pectus excavatum J Pediatr Surg, 41 (2006), pp. 1699–1703
Haller Jr., S.S. Kramer, S.A. Lietman Use of CT scans in selection of patients for pectus excavatum surgery: A preliminary report J Pediatr Surg, 22 (1987), pp. 904–906
P.M. Huang, E.T. Wu, Y.T. Tseng, S.W. Kuo, Y.C. Lee Modified Nuss operation for pectus excavatum: Design for decreasing cardiopulmonary complications Thorac Cardiovasc Surg, 54 (2006), pp. 134–137
Nuss Recent experiences with minimally invasive pectus excavatum repair “Nuss procedure” Jpn J Thorac Cardiovasc Surg, 53 (2005), pp. 338–344
Dzielicki, W. Korlacki, I. Janicka, E. Dzielicka Difficulties and limitations in minimally invasive repair of pectus excavatum – 6 years experience with Nuss technique Eur J Cardiothorac Surg, 30 (2006), pp. 801–804
D. Nuss, R.E. Kelly Jr., D.P. Croitoru, M.E. Katz A 10-year review of a minimally invasive technique for the correction of pectus excavatum J Pediatr Surg, 33 (1998), pp. 545–552
H. Kim do, J.J. Hwang, M.K. Lee, D.Y. Lee, H.C. Paik Analysis of the Nuss procedure for pectus excavatum in different age groups Ann Thorac Surg, 80 (2005), pp. 1073–1077
C.C. Ong, K. Choo, P. Morreau, A. Auldist The learning curve in learning the curve: a review of Nuss procedure in teenagers ANZ J Surg, 75 (2005), pp. 421–424
H.J. Park, S.Y. Lee, C.S. Lee Complications associated with the Nuss procedure: Analysis of risk factors and suggested measures for prevention of complications J Pediatr Surg, 39 (2004), pp. 391–39
D.P. Croitoru, R.E. Kelly Jr., M.J. Goretsky, M.L. Lawson, B. Swoveland, D. Nuss Experience and modification update for the minimally invasive Nuss technique for pectus excavatum repair in 303 patients J Pediatr Surg, 37 (2002), pp. 437–445
M.L. Metzelder, J.F. Kuebler, J. Leonhardt, B.M. Ure, C. Petersen Self and parental assessment after minimally invasive repair of pectus excavatum: Lasting satisfaction after bar removal Ann Thorac Surg, 83 (2007), pp. 1844–1849
J. Roberts, A. Hayashi, J.O. Anderson, J.M. Martin, L.L. Maxwell Quality of life of patients who have undergone the Nuss procedure for pectus excavatum: Preliminary findings J Pediatr Surg, 38 (2003), pp. 779–783
Coln, J. Carrasco, D. Coln Demonstrating relief of cardiac compression with the Nuss minimally invasive repair for pectus excavatum J Pediatr Surg, 41 (2006), pp. 683–686
D.L. Sigalet, M. Montgomery, J. Harder Cardiopulmonary effects of closed repair of pectus excavatum J Pediatr Surg, 38 (2003), pp. 380–385
G.D. Rushing, M.J. Goretsky, T. Gustin, M. Morales, R.E. Kelly Jr., D. Nuss When it is not an infection: metal allergy after the Nuss procedure for repair of pectus excavatum J Pediatr Surg, 42 (2007), pp. 93–97
M. Noguchi, K. Fujita A new technique for removing the pectus bar used in the Nuss procedure J Pediatr Surg, 40 (2005), pp. 674–677
J. Bohosiewicz, G. Kudela, T. Koszutski Results of Nuss procedures for the correction of pectus excavatum Eur J Pediatr Surg, 15 (2005), pp. 6–10

