Определение болезни. Причины заболевания
Спинальная мышечная атрофия (СМА; Spinal muscular atrophy) — это тяжёлое наследственное неврологическое заболевание, при котором электрические импульсы от нервных клеток (мотонейронов) не поступают к мышцам. В результате они постепенно слабеют и у ребёнка развиваются симметричные вялые параличи. Нередко такие нарушения приводят к инвалидизации пациента.
![Спинальная мышечная атрофия [20] Спинальная мышечная атрофия [20]](/media/bolezny/sma/spinalnaya-myshechnaya-atrofiya-20_s.jpeg?dummy=1778588363387)
Спинальная мышечная атрофия [20]
СМА относится к орфанным (очень редким) генетическим заболеваниям: она встречается примерно у 1 ребёнка 6–10 тыс. новорождённых [1]. Чаще всего болезнь проявляется у детей, но может встречаться и в других возрастах.
Причина развития СМА
Болезнь обычно возникает из-за дефекта в гене SMN1. Именно он отвечает за нормальную работу мотонейронов. Существуют и более редкие формы СМА, которые связаны с другими генами, например с IGHMBP2, TRPV4 и др.
В большинстве случаев СМА передаётся по аутосомно-рецессивному типу наследования. Это значит, что для развития болезни ребёнок должен получить по одному дефектному гену SMN1 от обоих родителей. У них, как правило, есть лишь один дефектный ген, поэтому сами они не болеют. Если оба родителя — носители, вероятность рождения ребёнка с СМА составляет 25 %.

Аутосомно-рецессивный тип наследования
Реже встречаются другие варианты наследования:
- аутосомно-доминантный — в этом случае достаточно одного дефектного гена, полученного от больного родителя, при этом вероятность передачи повышается до 50 % (встречается реже, например при мутации в гене TRPV4);
- Х-сцепленный — мутация находится в Х-хромосоме, поэтому болезнь чаще проявляется у мальчиков, а женщины с одной мутантной хромосомой обычно остаются здоровыми носительницами.
Иногда болезнь появляется случайно, даже если ни у одного из родителей нет дефектного гена.
Симптомы спинальной мышечной атрофии
СМА может проявиться сразу после рождения или в течение первого года жизни. Однако в зависимости от формы заболевания первые симптомы иногда возникают и в более позднем возрасте.
Ранние симптомы
Заподозрить СМА у новорождённого позволяют слабый крик, трудности с глотанием (особенно при тяжёлых формах) и постоянное выделение слюны.
Одним из главных симптомов является мышечная гипотония (слабый тонус мышц), из-за которой возникают характерные признаки:
- синдром тряпичной куклы — мышцы в теле младенца настолько слабые, что, когда его берут на руки, голова запрокидывается назад, руки и ноги безвольно свисают, а тело будто провисает;
- симптом складного ножа — из-за слабости мышц спины ребёнок буквально складывается пополам, если его слегка приподнять;
- поза лягушки — слабость в мышцах бёдер и таза приводит к тому, что колени ребёнка сгибаются и расходятся в стороны [8].
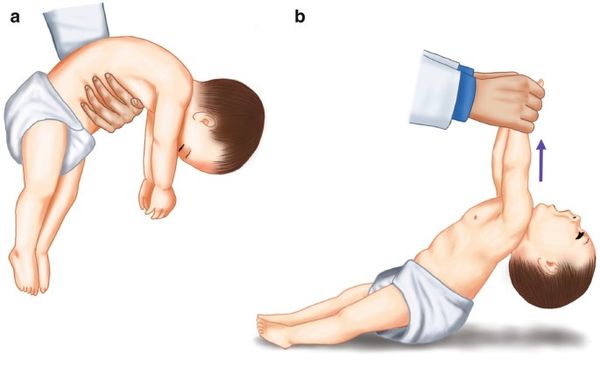
Признаки слабого тонуса мышц у младенца
Врачи (неонатолог, невролог или педиатр) могут заметить снижение мышечного тонуса на плановых осмотрах в 1, 3, 6 и 12 месяцев.
Двигательные нарушения
Основные проявления СМА — это симметричные вялые парезы (снижение силы мышц) и общая слабость. Особенно сильно поражаются проксимальные мышцы (те, что расположены ближе к туловищу): у рук это мышцы плеч и предплечий, у ног — мышцы таза и бёдер [10].
Из-за слабости мышц спины и межрёберных мышц у ребёнка может деформироваться грудная клетка и развиться сколиоз.

Сколиоз
Дополнительно у пациента могут обнаружить:
- фасцикуляции — мелкие ритмичные подёргивания мышц [1];
- постуральный тремор (или мини-полимиоклонус) — проявляется мелкими, быстрыми, неритмичными подёргиваниями пальцев и кистей рук, когда человек пытается удерживать определённую позу (например, вытянутые вперёд руки), этот признак чаще встречается при СМА 2–4-го типов;
- бульбарные нарушения — проблемы с глотанием (дисфагия), голосом (дисфония) и чёткостью речи (дизартрия).
Из-за нарушения глотания у пациента также возникают проблемы с питанием [1].
При этом важно отметить, что интеллект при СМА, как правило, не страдает.
Патогенез спинальной мышечной атрофии
Как уже было сказано выше, СМА — это генетическое заболевание, которое развивается из-за мутаций в определённых генах [16][17].
В подавляющем большинстве случаев болезнь вызвана мутацией или делецией (потерей участка) в гене SMN1. Существуют и более редкие формы СМА, связанные с мутациями в других генах, например в DYNC1H1, VAPB, GARS и т. д. Сейчас известно более 30 различных генетических вариантов этого заболевания [17].
Каждый ген отвечает за производство определённого белка. В случае СМА из-за дефекта гена SMN1 в организме не вырабатывается достаточное количество функционального белка SMN — белка выживаемости мотонейронов (нервных клеток, расположенных в передних рогах спинного мозга) [13]. Без него мотонейроны постепенно погибают.
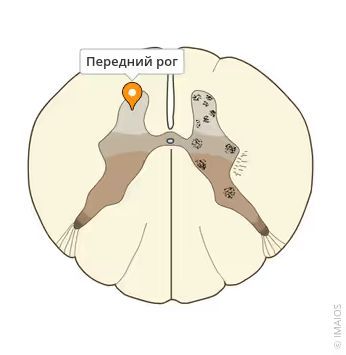
Передние рога спинного мозга
В норме человек может совершить движение после того, как:
- головной мозг посылает команду через центральные мотонейроны к периферическим мотонейронам в спинном мозге;
- периферические мотонейроны передают сигнал мышцам;
- мышцы сокращаются.
При СМА проблема возникает на втором этапе из-за повреждения периферических мотонейронов. В результате мышцы не получают нужных команд и ослабевают. Со временем из-за отсутствия нормальной нервной стимуляции у них также нарушается питание и кровоснабжение, после чего мышцы начинают атрофироваться (уменьшаться в объёме).
При тяжёлых формах СМА могут страдать не только мотонейроны, но и другие органы и ткани. Возможны аномалии развития сердца и сосудов (пороки, нарушения ритма), проблемы с органами желудочно-кишечного тракта, недостаточность работы поджелудочной железы и печени, а также почечная недостаточность [14]. В таких случаях лечение проводят профильные специалисты — кардиолог, гастроэнтеролог, гепатолог и др., иногда требуется хирургическая коррекция.
Роль гена SMN2
В организме есть ещё один ген, который вырабатывает белок SMN (пусть и в меньшем количестве) — это ген SMN2. Чем больше у пациента копий гена SMN2, тем легче протекает заболевание. В зависимости от типа СМА зачастую наблюдается следующая закономерность:
- 1-й тип — у пациента обычно есть всего 2 копии SMN2, поэтому такая болезнь протекает тяжелее остальных;
- 2-й тип — обычно 3 копии;
- 3-й тип — 3–4 копии;
- 4-й тип — 4 и более копий [1].
Классификация и стадии развития спинальной мышечной атрофии
В Международной классификации болезней 11-го пересмотра (МКБ-11) выделяют следующие типы СМА:
- СМА 0-го типа — самая тяжёлая форма. Её можно заподозрить ещё до рождения по сниженной двигательной активности плода. После рождения у ребёнка быстро развиваются грубые нарушения дыхания и глотания, что связано с высоким риском летального исхода.
- СМА 1-го типа (болезнь Верднига — Гоффмана) — проявляется в первые месяцы жизни. У ребёнка отмечается выраженная мышечная слабость, снижение сосательного рефлекса и отставание в двигательном развитии. Часто встречаются врождённые проблемы со стороны сердца. Без активной реабилитации и лечения продолжительность жизни обычно не превышает двух лет.
- СМА 2-го типа (болезнь Дубовица) — чаще всего проявляется до полутора лет. Дети с таким диагнозом могут сидеть и даже стоять с поддержкой, но на ходьбу сил у них не хватает. Из-за слабости мышц спины может развиться сколиоз, а слабость межрёберных мышц приводит к плохой вентиляции лёгких и частым застойным пневмониям. Продолжительность жизни варьируется — от 2 до 40 лет.
- СМА 3-го типа — период дебюта разнится от 18 месяцев до 21 года, но чаще всего проявляется примерно в 3 года. Пациенты сохраняют способность сидеть, стоять и ходить. Мышечная слабость может быть разной степени тяжести. Больше всего страдают мышцы плечевого пояса и бёдер. Эта форма не оказывает существенного влияния на продолжительность жизни [1].
- СМА 4-го типа — самая лёгкая форма. Обычно проявляется в 20–30 лет. У пациентов наблюдаются признаки поражения периферического мотонейрона: мышечная слабость, фасцикуляции, атрофия мышц и снижение рефлексов. Люди с такой формой СМА могут испытывать трудности при подъёме по лестнице, вставании из положения сидя и других нагрузках на мышцы бёдер, но в остальном они могут передвигаться самостоятельно, т. е. качество их жизни остаётся относительно высоким [1].
По преимущественному поражению мышц также выделяют проксимальные и дистальные формы СМА. Классические варианты, описанные выше, относятся к проксимальным. В свою очередь дистальные формы считаются атипичными. При них слабость и атрофия мышц начинаются не с плеч и бёдер, а с кистей рук и стоп. К ним относятся СМА Кеннеди, Финкеля, Джокеля, Хироямы и др.) [17].
Так как СМА является хроническим заболеванием, которое склонно к постепенному прогрессированию в течение всей жизни, стадий у неё нет.
Осложнения спинальной мышечной атрофии
Одним из самых опасных осложнений СМА является дыхательная недостаточность [8]. Нередко возникает апноэ — период, когда дыхание полностью останавливается. Для своевременного выявления таких остановок дыхания используют специальный дыхательный мониторинг. Приборы фиксируют апноэ и при необходимости автоматически подключают искусственную вентиляцию лёгких.
Из-за слабости дыхательных мышц (в том числе межрёберных) грудная клетка плохо расширяется, из-за чего воздух плохо циркулирует в лёгких. Это приводит к его застою и значительно повышает риск инфекций дыхательных путей — бронхитов и пневмоний.
Ещё один частый симптом — гиперсаливация (повышенное слюноотделение). В сочетании с нарушением глотания это создаёт высокий риск аспирации — попадания слюны или пищи в дыхательные пути. Аспирация может стать причиной тяжёлой аспирационной пневмонии.
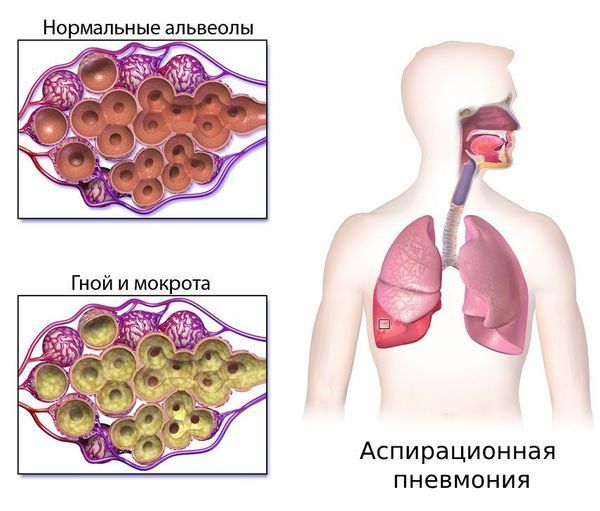
Аспирационная пневмония
Проблемы с глотанием также приводят к трудностям с питанием. Пациенты часто плохо едят, теряют вес и могут испытывать метаболические нарушения — снижение уровня белка, глюкозы и других важных веществ в крови.
К ортопедическим осложнениям относится сколиоз разной степени выраженности. Они наиболее часто встречаются у пациентов со 2-м типом СМА [15].
Диагностика спинальной мышечной атрофии
Диагностика СМА — сложный процесс, который требует участия нескольких специалистов: невролога, педиатра, неонатолога и врача-генетика.
Осмотр невролога включает в себя подробный сбор анамнеза (истории жизни и болезни) пациента. Врач уточняет, как протекала беременность, проводились ли пренатальные скрининги, были ли у ребёнка частые инфекции дыхательных путей.
Далее он проводит осмотр, во время которого оценивает:
- силу и тонус мышц;
- двигательные возможности;
- глотание, голос и слюноотделение;
- сухожильные рефлексы (при СМА они обычно снижены или отсутствуют);
- чувствительность, координацию, походку, а также интеллектуальные и эмоциональные функции.
Генетическое исследование играет решающую роль в подтверждении диагноза [1][13]. Для этого достаточно обычного анализа крови. Лаборатория проверяет 5-ю хромосому, ищет мутации или делецию в гене SMN1 и определяет количество копий гена SMN2. После получения результатов пациента обязательно направляют к врачу-генетику, который правильно интерпретирует анализ и устанавливает тип СМА.
В некоторых случаях также проводят:
- анализ на уровень креатинфосфокиназы (КФК) — фермента, который отражает состояние мышечной ткани, при СМА он может быть умеренно повышен;
- электромиографию и электронейромиографию (ЭМГ и ЭНМГ) — позволяют оценить, насколько хорошо нервный импульс доходит от спинного мозга до мышц.
Однако все эти исследования не являются строго специфичными для СМА и имеют второстепенное значение, так как похожие изменения могут встречаться при других нервно-мышечных заболеваниях.
Чтобы оценить выраженность клинической картины, используют специальные стандартизированные шкалы — CHOP-INTEND и HFMSE [5]. С их помощью врач в баллах измеряет, какие двигательные навыки сохранены, а какие утрачены, и отслеживает динамику заболевания.
Дифференциальная диагностика
Симптомы СМА могут указывать и на другие заболевания, поэтому врачам важно исключить различные миопатии (в том числе мышечные дистрофии Дюшенна, Беккера, Эрба — Рота), другие болезни двигательного нейрона, полинейропатию, болезнь Фридрейха, детский церебральный паралич (ДЦП), миотоническую дистрофию и ряд других заболеваний [11].
Чтобы отличить эти заболевания, врач придерживается следующего алгоритма:
- Сбор анамнеза, неврологический осмотр, выявление возможных родственных связей с носителями патологического гена или больными СМА.
- Генетический анализ на патологию в гене SMN1.
- Если мутация найдена, — исследование на количество копий SMN2, если мутации в гене SMN1 нет, — исследование на другого рода мутации, согласно клинической картине заболевания.
Лечение спинальной мышечной атрофии
Подходы к лечению СМА делятся на 2 группы:
- патогенетическая терапия — воздействует на саму причину заболевания и помогает восстановить выработку белка SMN;
- симптоматическая терапия — меры, направленные на профилактику и лечение осложнений, а также улучшение качества жизни пациента.
Патогенетическое лечение
Это основное и наиболее эффективное направление терапии. В России используют следующие препараты:
- Нусинерсен (Спинраза) — лекарство вводят в спинномозговую жидкость через люмбальную пункцию — уколом в поясницу между 3-м и 4-м поясничными позвонками. Во время процедуры пациент лежит на боку с приведёнными к груди ногами. Среди возможных побочных эффектов выделяют головную боль, болезненность в месте укола и риск инфекции [4][6].

Люмбальная пункция
- Рисдиплам — модификатор правильной работы гена выживаемости двигательных нейронов 2-го типа, т. е. он улучшает работу «запасного» гена SMN2, благодаря чему в организме образуется больше нужного белка. Препарат можно применять в форме таблеток.
- Онасемноген абепарвовек (Золгенсма) — генный препарат на основе аденовируса, который способствует нормальной выработке белка SMN. Данный препарат вводят однократно до 2 лет с помощью капельницы (внутривенно) [6][12].
Эти лекарства заметно улучшают работу мотонейронов и двигательные возможности пациентов. Однако они очень дорогостоящие, а некоторые из них требуют пожизненного применения.
При этом исследования в области лечения СМА продолжаются. Например, сейчас учёные тестирую препарат Апитегромаб (моноклональное антитело), который блокирует миостатин — вещество, тормозящее рост мышц [9].
Симптоматическое лечение
Пациентам со СМА крайне важно поддерживать дыхательную функцию. Для этого используют:
- специальные аспираторы для удаления слизи из дыхательных путей;
- дыхательную гимнастику и кинезиотерапию;
- искусственную вентиляцию лёгких и установку трахеостомы (в тяжёлых случаях) [13].

Трахеостома
Также большое значение имеет поддержка питания. При выраженных нарушениях глотания сначала используют назогастральный зонд, а позже может быть установлена гастростома — специальное отверстие в брюшной стенке для прямого введения питания в желудок [1].
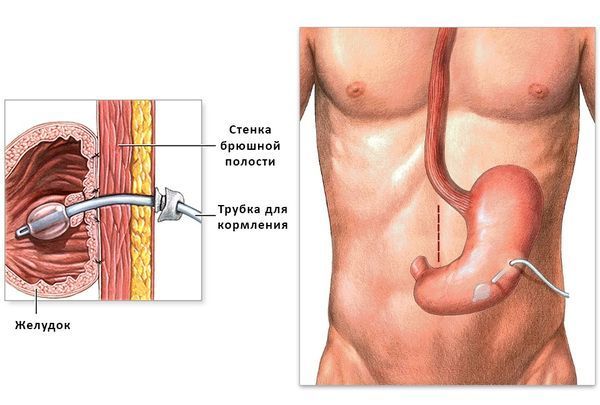
Гастростома
При выраженном сколиозе может потребоваться операция — артродез позвоночника (фиксация позвонков металлоконструкцией). В современных клиниках предпочитают использовать динамические системы фиксации (например, «двойные стержни»), которые лучше сохраняют подвижность [1].
![Фиксация позвонков при сколиозе [19] Фиксация позвонков при сколиозе [19]](/media/bolezny/sma/fiksaciya-pozvonkov-pri-skolioze-19_s.jpeg?dummy=1778571681632)
Фиксация позвонков при сколиозе [19]
Чтобы замедлить прогрессирование заболевания и предотвратить осложнения, назначают:
Прогноз. Профилактика
Прогноз при СМА сильно зависит от типа заболевания. Он может быть как крайне серьёзным, так и относительно благоприятным, когда болезнь лишь немного снижает общее качество жизни.
По данным одного из обзоров:
- при СМА 1-го типа инвалидность в детстве устанавливают у 98 % пациентов, при этом 41 % больных требуется паллиативная помощь (особая поддерживающая терапия);
- СМА 2-го типа — 98 и 34 % пациентов;
- СМА 3-го типа — 61 и 11 % пациентов;
- СМА 4-го типа — 6 % больным требовалась паллиативная помощь [6].
Таким образом, наиболее неблагоприятный прогноз сопровождает 1-й и 2-й типы СМА. При формах с более поздним началом (3-й и 4-й типы) прогноз значительно лучше: многие пациенты сохраняют относительно высокое качество жизни.
Пациентам со СМА присваивают группу инвалидности. При позднем начале заболевания обычно устанавливают 2-ю или 3-ю группу в зависимости от выраженности симптомов. Все пациенты со спинальной мышечной атрофией признаются негодными к военной службе.
Профилактика СМА
Основой профилактики является медико-генетическое консультирование ещё до беременности. Врач-генетик изучает семейный анамнез и оценивает риск рождения ребёнка с этим заболеванием [14]. При подозрении на носительство будущим родителям могут назначить генетический анализ. Если оба партнёра являются носителями, возможны следующие варианты:
- молекулярно-генетическое тестирование плода во время беременности (через ворсины хориона или амниотическую жидкость);
- преимплантационное генетическое исследование эмбрионов при экстракорпоральном оплодотворении (ЭКО) [1].

Амниоцентез
Кроме того, в России с января 2023 года введён обязательный неонатальный скрининг всех новорождённых на СМА [18]. Это позволяет выявить заболевание в первые дни жизни и начать лечение как можно раньше.
Список литературы
Ассоциация медицинских генетиков. 5q-ассоциированная спинальная мышечная атрофия: клинические рекомендации — М., 2024.
Барковская О. С., Зубченко С. В., Маханькова Л. В. Актуальность применения технических средств реабилитации пациентам со спинальной мышечной атрофией (СМА) и родственными синдромами. — М., 2022. — С. 241–244.
Спинальная мышечная атрофия: комплексный подход к заболеванию // Педиатрическая фармакология. — 2021. — № 2. — С. 163–164.
Кузенкова Л. М., Увакина Е. В., Серебренникова Э. Б. и др. Первый опыт применения воспроизведённого препарата Нусинерсен российского производства у пациентов детского возраста со спинальной мышечной атрофией // Неврологический журнал им. Л. О. Бадаляна. — 2025. — № 2. — С. 105–112.
Кокорина А. А., Никитин С. С. Промежуточный анализ результатов лечения детей раннего возраста со спинальной мышечной атрофией 5q, получивших генозаместительную терапию препаратом Онасемноген абепарвовек. Клинические наблюдения // Вопросы современной педиатрии. — 2022. — № 6S. — С. 535–547.
Рылов А. Путь от теории к практике диагностики и лечения пациентов со спинальной мышечной атрофией // Русский журнал детской неврологии. — 2024. — № 2. — С. 80–88.
Витковская И. П., Зеленова О. В., Стерликов С. А. и др. Первое проспективное многоцентровое не интервенционное исследование распространённости спинальной мышечной атрофии в Российской Федерации // Современные проблемы здравоохранения и медицинской статистики. — 2022. — № 3. — С. 393–409.
Бондарь В. А., Борисов И. В., Канарский М. М., Некрасова Ю. Ю. Спинальная мышечная атрофия 1-го типа: медико-социальная проблема современности // Медико-социальная экспертиза и реабилитация. — 2020. — № 2. — С. 4–7.
Crawford T. O., Darras B. T., Day J. W. et al. Safety and Efficacy of Apitegromab in Patients With Spinal Muscular Atrophy Types 2 and 3: The Phase 2 TOPAZ Study // Neurology. — 2024. — № 5. — Р. e209151.ссылка
Соколова М. Г., Лобзин С. В., Литвиненко И. В. и др. Клинический и биохимический полиморфизм спинальной мышечной атрофии // Неврология, нейропсихиатрия, психосоматика. — 2017. — № 1. — С. 50–54.
Шпилюкова Ю. А., Иллариошкин С. Н. Спинальная мышечная атрофия у взрослых: проблемы ранней диагностики // Нервно-мышечные болезни. — 2022. — № 4. — С. 37–45.
В России зарегистрирован первый генозаместительный препарат для терапии спинальной мышечной атрофии // Лечащий врач. — 2021.
Спинальная мышечная атрофия — больше, чем двигательные нарушения // Русский журнал детской неврологии. — 2024. — № 2. — С. 89–96.
Маретина М. А., Киселев А. В., Ильина А. В. и др. Современные тенденции в диагностике, скрининге и лечении спинальной мышечной атрофии // Вестник Российской академии медицинских наук. — 2022. — № 2. — С. 87–96.
Шаймурзин М. Р., Туруспекова С. Т. Модель прецизионной терапии костно-мышечных осложнений у детей со спинальными мышечными атрофиями 2 и 3-го типа // Вестник Казахского национального медицинского университета. — 2021. — № 4. — С. 333–339.
Афонина Ю. И., Болотина Е. В., Колоколов О. В. Генетическая гетерогенность и фенотипический полиморфизм спинальных мышечных атрофий. — Саратов: Саратовский государственный медицинский университет им. В. И. Разумовского, 2025. — С. 710–711.
Пономарёва Т. И., Амелина М. А., Медоян А. В. и др. Генетическая гетерогенность спинальной мышечной атрофии (СМА не 5q) (обзор литературы) // Живые и биокосные системы. — 2024. — № 50.
Министерство здравоохранения РФ. Об утверждении порядка оказания медицинской помощи пациентам с врождёнными и (или) наследственными заболеваниями: приказ от 21.04.2022 № 274н (ред. от 19.12.2025).
Bona E. Girl, 15, with crooked spine warns parents of simple sign to look out for // Echo. — 2018.
Опря И., Слепов Ю., Пушкин М. 12 месяцев. Спинально-мышечная атрофия. Часть первая: невыживаемость мотонейронов // Indicator. — 2023.

