Определение болезни. Причины заболевания
Синдром Ландау — Клеффнера (ЛКС) — редкое заболевание, которое проявляется приступами эпилепсии с постепенной или внезапной регрессией речевого развития. Нарушение выражается в афазии — неспособности понять и использовать речь. Точные причины ЛКС неизвестны. До описания синдрома Уильямом Ландау и Фрэнком Клеффнером в 1957 году снижение и/или утрата речи на фоне судорог не выделялось в отдельное заболевание. Патологию относили к проявлению эпилепсии и называли "приобретённой эпилептической афазией".
Синдром Ландау — Клеффнера является очень редкой формой эпилепсии и поражает 1 из 200 (0,5 %) детей с эпилепсией в возрасте от 2 до 8 лет. С 1957 г. зарегистрировано около 200 случаев. Мужчины страдают от ЛКС чаще, чем женщины [2]. Клиника эпилепсии состоит из приступов по типу абсанса — замирания или застывания пациента с регистрацией на ЭЭГ пароксизмальной активности (хаотично нарастающей электрической активности больших полушарий головного мозга) или тонико-клонических эпизодов (конвульсий), которые регистрируются во время сна.
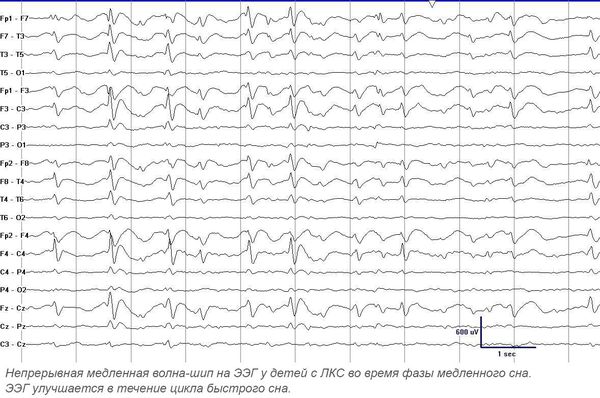
ЭЭГ во время фазы медленного сна у детей с ЛКС
Симптомы синдрома Ландау — Клеффнера
Как правило, дети с ЛКС развиваются нормально, но затем без видимой причины теряют речевые навыки. Многие пациенты страдают от судорог, но у некоторых болезнь протекает без них. Наиболее распространённым типом судорог, наблюдаемых при синдроме Ландау — Клеффнера, является фокальный моторный приступ. Он проявляется сокращением одной мышцы или группы мышц, например в шее или руке. Очаговые приступы могут прогрессировать, затрагивая оба полушария мозга, и/или распространяясь на соседние области. Когда это происходит, клиническая картина включает тонико-клонические приступы — резкие сокращения мышц в начале приступа с последующими их ритмическими сокращениями [1].
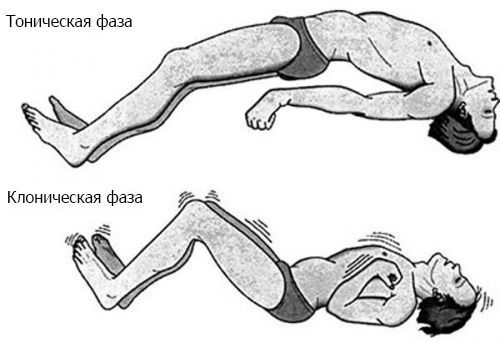
Тонико-клонические приступы
ЛКС сложен для диагностики. При постановке диагноза опираются на следующие симптомы:
- нормальное развитие до начала заболевания;
- ночные вздрагивания, судороги, приступы (могут отсутствовать или быть однократными);
- отсроченный и прогрессирующий дефицит высших психических функций, соответствующих возрасту ребёнка, с акцентом на речевую функцию.
Если электроэнцефалограмма показывает аномалии в лобных отделах головного мозга, то пациент имеет поведенческие проблемы, такие как синдром дефицита внимания и гиперактивности (СДВГ). Нарушения проявляются в снижении концентрации, гиперактивности, агрессии или импульсивности. В старшем возрасте в поведении могут преобладать аутистические черты [19].
Патогенез синдрома Ландау — Клеффнера
Патогенез Синдрома Ландау — Клеффнера полностью не изучен. Фундаментальные научные исследования находятся в стадии разработки, многие авторы связывают развитие заболевания с нейровоспалением. Причины воспаления в нервной ткани при ЛКС не выявлены, но есть предположение о воздействии аутоиммунных факторов [15]. Исследования показали, что у детей с ЛКС наблюдается повышенный уровень аутоантител, направленных против нейротрофического фактора мозга (белка, стимулирующего и поддерживающего развитие нейронов) [16]. Потенциальное вовлечение иммунной системы и/или воспалительные каскады реакций при ЛКС объясняют эффективность гормональной терапии [17].
Предполагается, что причиной ЛКС являются врождённые пороки развития головного мозга, генетические нарушения или метаболические состояния. Точная ассоциация ЛКС с генетическим фактором неизвестна, но за последнее время обнаружены новые генетические мутации, характерные для данного заболевания. В основном доказана связь с геном GRIN2A [11]. Ген кодирует белок GluN2A (ранее известный как NR2A). GluN2A содержится в нервных клетках головного и спинного мозга, в том числе в областях мозга, участвующих в формировании речи, и является одним из компонентов NMDA-рецепторов. Эти рецепторы регулируют нейрональную возбудимость и синаптическую пластичность [13]. В подтверждение гипотезы исследователи выявили троих неродственных пациентов с различными делециями шестнадцатой хромосомы (утраты её участка), включая ген GRIN2A.

Делеция хромосомы
Больные страдали ранней фокальной эпилепсией, тяжёлой умственной нетрудоспособностью, отсутствием речи или задержкой речевого развития [11]. Помимо гена GRIN2A, изучается ряд дополнительных генов-кандидатов: RELN, BSN, EPHB2 и NID2 предположительно ассоциированных с ЛКС [20][12].
Классификация и стадии развития синдрома Ландау — Клеффнера
Диагноз ЛКС в соответствии с МКБ-10 относят в отдел "Специфические расстройства развития речи и языка", рубрику (F80). Диагноз звучит так: "Приобретённая афазия с эпилепсией [Ландау — Клефнера]" (F80.3).
Специальная группа по классификации Международной лиги против эпилепсии предложила группу синдромов, называемых эпилептическими энцефалопатиями, которые включают эпилепсию с непрерывным всплеском во время медленного сна и синдром Ландау — Клеффнера.
Согласно данным, размещённым Международной противоэпилептической лигой от 2017 года, эпилепсии подразделяют на следующие виды [28]:
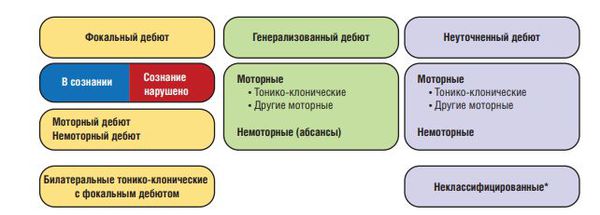
Базовая рабочая классификация типов приступов Международной Противоэпилептической Лиги 2017 г.
Фокальные приступы возникают в сетевых структурах, ограниченных одним полушарием. Они могут быть локализованы, либо же распространяться на соседние зоны или другое полушарие мозга. Первично-генерализованные приступы возникают одномоментно, с быстрым вовлечением сетевых структур обоих полушарий. Немоторные приступы могут проявляться вегетативными симптомами, заторможенностью поведенческих реакций, когнитивными, эмоциональными и сенсорными нарушениями.
Утверждённой классификации по данным ЭЭГ нет. Изменения на ЭЭГ при ЛКС имеют чёткую зависимость от возраста: возникают в 3–9 лет и, как правило, постепенно исчезают к 13–15 годам [1][7][8]. Продолжительность максимально выраженных диффузных ЭЭГ-аномалий составляет в среднем от 1 до 5 лет. Обычно максимальная выраженность диффузной эпилептиформной активности на ЭЭГ у больных ЛКС наблюдается в возрасте 7–8 лет [7].
Осложнения синдрома Ландау — Клеффнера
Синдром Ландау — Клеффнера может привести к развитию энцефалопатии. Энцефалопатия — это заболевание, проявляющееся дистрофией нервной ткани в верхних слоях головного мозга или в коре больших полушарий с постепенным снижением функции коры. Злокачественное течение энцефалопатии обусловлено тем, в каком возрасте началась эпилепсия — ранний дебют заболевания имеет более серьёзные последствия. Эпилепсия младенчества с мигрирующими очаговыми припадками является крайне тяжёлым синдромом развития.
Важно отметить, что клинические проявления (афазия) не зависят от тяжести и частоты судорог. У некоторых детей наблюдается тяжёлая афазия с полной потерей речи и её понимания, несмотря на отсутствие судорог. Таким образом, эпилептическая активность, а не судороги, вероятно, коррелирует с нарушением языка и его степенью [5].
ЛКС может вызывать изменение настроения, беспокойство и депрессию, нарушения сна, ухудшение рабочей памяти (но не долговременной), гиперчувствительность к звукам [21][22].
Следует учитывать дозозависимый эффект и взаимодействие противоэпилептических препаратов с другими медикаментами для предотвращения побочного действия лекарственных средств. Эффективность противоэпилептических препаратов измеряется, прежде всего, по его влиянию на частоту приступов, а не по воздействию на картину нарушения на ЭЭГ.
Диагностика синдрома Ландау — Клеффнера
Синдром Ландау — Клеффнера требует привлечения различных специалистов: педиатра, нейропсихолога, детского психиатра, психолога, логопеда, эрготерапевта (специалиста по восстановлению социальных, бытовых, рабочих, функциональных и двигательных навыков), отоларинголога.
Основной метод диагностики — электроэнцефалография (ЭЭГ). Повышенная эпилептиформная активность может быть подтверждена длительным ЭЭГ видео-мониторингом (суточным или ночным). Эпилептиформная активность представляет собой электрические колебания головного мозга в виде острых волн и пиков. Она значительно (более чем на 50 %) отличается от фоновой активности и, как правило, обнаруживается на ЭЭГ у лиц, страдающих эпилепсией. Ночной мониторинг выполняется в виде непрерывной регистрации электроэнцефалограммы в течение ночи. При ЛКС в период сна происходит увеличение патологической активности — появление непрерывного всплеска и пик-волновой активности во время медленного сна, в основном с частотой 1,5-2,5 Гц. В 70-80 % случаев ЛКС сопровождают моторные эпилептические припадки.
Другим методом диагностики является магниторезонансная томография (МРТ). Описаны случаи уменьшения объёма областей мозга, ответственных за развитие речи. Эти данные, однако, не несут диагностической пользы, но нужны для исключения структурных поражений, таких как опухоли головного мозга [4].
Дифференциальный диагноз при ЛКС включает в себя следующие заболевания:
- Эпилептический синдром с усилением эпилептиформной активности во время сна — по сравнению с ЛКС отсутствуют речевые нарушения.
- Доброкачественная затылочная эпилепсия детского возраста с ранним дебютом (синдром Панайотопулоса) — также отсутствуют речевые нарушения.
- Доброкачественная эпилепсия с центро-темпоральными спайками (роландическая эпилепсия) — отсутствуют речевые нарушения.
- Детская затылочная эпилепсия с дебютом в старшем возрасте (тип Гасто).
- Синдромом Леннокса-Гасто — крайне редки моторные приступы.
- Синдром Ретта — более раннее начало.
- Расстройство аутистического спектра.
- Дефекты слуха.
Диагностика степени тяжести энцефалопатии проводится при помощи ЭЭГ и проявляется различными аномалиями электроэнцефалограммы в виде медленноволновой активности чаще всего вокруг височно-теменных областей головного мозга.
Лечение синдрома Ландау — Клеффнера
В большинстве случаев для лечения используется противоэпилептическая (ПЭП) или стероидная терапия. Эффект после фармакотерапии является переменным и непредсказуемым. В исследовании Marescaux et al. (1990) сообщается, что использование противосудорожных средств обычно не приводит к улучшению языковых способностей. Применение высоких доз гормональной терапии кортикостероидов может улучшить общее состояние детей, но речевые и интеллектуальные нарушения при этом сохраняются [3].
Есть исследования о более длительном эффекте от терапии кортикостероидов, в сравнении с терапией ПЭП [6]. Кортикостероиды (например, преднизон перорально 1 мг / кг / день в течение 6 месяцев или преднизолон перорально 2 мг / кг / день в течение не менее трёх месяцев перед постепенным снижением) могут быть полезны для улучшения и/или стабилизации речевой функции, когнитивных и поведенческих навыков [23]. Их применение в сочетании с бензодиазепинами (БДЗ) рекомендуется при эпилептической активности и языковых нарушениях, сохраняющихся более 10 месяцев, несмотря на терапию [24].
При тяжёлом течении применяют хирургическое лечение:
- Стимуляция блуждающего нерва. Операция заключается в том, что нерв, по которому импульсы поступают в головной мозг, окутывается электродом. Через него в головной мозг из стимулятора, вшиваемого под кожу, посылаются противоэпилептические стимулы. Это предупреждает развитие судорожного припадка. Методика применяется с 1990 года.
- Метод множественного субпиального транскортикального рассечения. Данный метод предназначен для устранения способности кортикальной ткани генерировать патологическую активность нейронов или субклиническую эпилептиформную активность. При этом сохраняются корковые функции оперируемых областей. Предварительно проводится трепанация черепа в проекции оперируемой области под общим наркозом, эффект достигается благодаря рассечению и, следовательно, предотвращению распространения пароксизмальной активности на соседние области головного мозга.
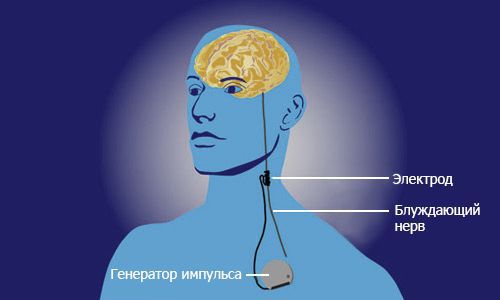
Стимуляция блуждающего нерва
После операции большое значение имеет речевая реабилитация, включающая как занятия с логопедом, так и специализированный массаж и артикуляционную гимнастику. Методы логопедии заметно улучшают речевые способности большинства людей с ЛКС, однако зачастую в полном объёме речь не восстанавливается. Результаты речевой реабилитации зависят от многих факторов: уровня манифестации заболевания, стратегии гормональной терапии, начала и интенсивности реабилитационных мероприятий.
Спорным методом лечения является кетогенная диета. Кетогенная диета (КД) используется с 1920-х годов для терапии резистентных к лечению видов эпилепсии [14]. При КД пациент потребляет большое количество жиров (90 %) и низкое содержание белков и углеводов. Данные некоторых исследователей показывают, что индивидуально подобранная КД является хорошей альтернативой нехирургическому и после хирургическому вмешательству фармакорезистентных пациентов с эпилепсией [10]. Однако другие исследователи отмечают нехватку клинических данных, чтобы можно было сделать такие выводы [14].
При лечении заболевания требуется наблюдение клинического фармаколога. Специалист поощряет соблюдение правил приёма лекарств, проверяет взаимодействие медикаментов и предупреждает врача и пациента о препаратах, которые могут усугубить состояние. Специалисты по неврологии могут помочь в мониторинге лечения, а также в консультировании пациентов и/или родителей.
Кроме того, важную роли играет социальная служба. Социальный работник должен помочь пациенту обеспечить дома адекватные для восстановления условия и доступ к вспомогательным услугам.
Прогноз. Профилактика
Синдром редкий, поэтому точного прогноза нет. Патологию считают доброкачественной с точки зрения развития эпилептической энцефалопатии. Прогноз варьируется в основном в отношении афазии. У детей может наблюдаться постепенное снижение внимания, памяти, мышления и общей когнитивной функции через 1–2 года после начала судорог. Результаты послеоперационного лечения в раннем детском возрасте показывают, что улучшение функции речи чаще всего наблюдается через годы после операции. У некоторых детей речевые нарушения могут сохраниться и со временем приобрести более тяжёлое течение. У других пациентов возможно восстановление большей части речевых навыков, хотя реабилитация занимает длительное время. В некоторых случаях может произойти ремиссия с последующим рецидивом.
Прогноз улучшается, если расстройство наступило после шести лет, а также при ранней реабилитации и сопровождении логопеда. Судороги обычно исчезают в зрелом возрасте, к тому времени эпилептическая активность на ЭЭГ также снижается.
Наряду с исследованием причин заболевания многими лабораториями проводятся испытания по лечению ЛКС. Для детей с рефрактерной эпилептической энцефалопатией исследуется применение каннабидиола (фаза 1, открытое исследование по увеличению дозы) [5]. Другое рандомизированное исследование оценивает ацетазоламид (перорально 8-10 мг/кг в течение 4-8 недель) в сравнении с противоэпилептическим препаратом — диазепамом (перорально 0,5 мг/кг в течение четырёх недель). Результаты показали умеренные улучшения у трети пациентов с ЛКС. Исследования с новыми нефармакологическими мультимодальными подходами, безусловно, являются ещё одним вариантом для изучения.
Поскольку заболевание связано с генетическими нарушениями, его профилактики на данный момент нет. При высоком генетическом риске во время планирования беременности обязательна консультация врача-генетика.
Список литературы
Мухин К. Ю., Холин А. А., Петрухин А. С.и др. Электро-клиническая характеристика синдрома Ландау — Клеффнера // Журнал неврологии и психиатрии им. С.С. Корсакова, 2003. —103 (9): 16–27.
Beaumanoir A. The Landau Kleffner syndrome. In: Roger J, Beureau M, Dravet C, Dreifuss F, Perret A, Wolf P, editors. Epileptic syndromes in infancy, childhood and adolescence. 2nd ed. London: John Libbery; 1992; p. 231–243.
Marescaux C, Hirsch E, Finck S, Maquet P, Schlumberger E, Sellal F, et al. Landau-Kleffner syndrome: a pharmacologic study of five cases. Epilepsia 1990; 31: 768–77.ссылка
Maria Rosaria Muzio; Marco Cascella; Yasir Al Khalili. Landau Kleffner Syndrome, 2020.ссылка
Muzio, M. R., Cascella, M., & Al Khalili, Y. Landau Kleffner Syndrome. In StatPearls [Internet]. StatPearls Publishing, 2019.
Lerman, P., Lerman‐Sagie, T., & Kivity, S. Effect of early corticosteroid therapy for Landau‐Kleffner syndrome. Developmental Medicine & Child Neurology, 1991; 33(3), 257-260. ссылка
Fejerman N., Caraballo R., Dalla Bernardina B. Atypical evolutions of benign focal epilepsies in children. In: Benign focal epilepsies in infancy, childhood and adolescence. Ed. By N. Fejerman, R.H. Caraballo. Montrouge: JL Eurotext, 2007; P. 179–219.ссылка
Imataka G., Arisaka O. Serial EEG study in a girl with Landau–Kleffner syndrome associated with continuous spikes and waves during slow sleep. Eur Rev Med Pharmacol Sci 2014;18(15): 2145–2147.ссылка
Armeno M., Caraballo R., Vaccarezza M., Alberti M. J., Ríos V., Galicchio S., et al. [National consensus on the ketogenic diet]. Rev. Neurol, 2014; 59: 213–223.ссылка
D'Andrea Meira I, Romão TT, Pires do Prado HJ, Krüger LT, Pires MEP, da Conceição PO. Ketogenic Diet and Epilepsy: What We Know So Far. Front Neurosci, 2019.ссылка
Reutlinger C, Helbig I, Gawelczyk B, Subero JI, Tönnies H, Muhle H, Finsterwalder K, Vermeer S, Pfundt R, Sperner J, Stefanova I, Gillessen-Kaesbach G, von Spiczak S, van Baalen A, Boor R, Siebert R, Stephani U, Caliebe A. Deletions in 16p13 including GRIN2A in patients with intellectual disability, various dysmorphic features, and seizure disorders of the rolandic region. Epilepsia, 2010; 51 (9): 1870-1873. ссылка
Turner S., Mayes A., Verhoeven A., Mandelstam S., Morgan AT, Scheffer I. GRIN2A: an aptly named gene for speech dysfunction. Neurology, 2015; 84 (6): 586-93.
Wyllie DJ, Livesey MR, Hardingham GE. Influence of GluN2 subunit identity on NMDA receptor function. Neuropharmacology, 2013; 74: 4-17. ссылка
Lagae L. Rational treatment options with AEDs and ketogenic diet in Landau‐Kleffner syndrome: Still waiting after all these years. Epilepsia, 2009; 50, 59-62.ссылка
Husari KS, Dubey D. Autoimmune Epilepsy. Neurotherapeutics, 2019;16 (3).
Granata T, Cross H, Theodore W, Avanzini G. Immune-mediated epilepsies. Epilepsia, 2011.
Bakker D., Catsman-Berrevoets C., Neuteboom R. Effectiveness of a hybrid corticosteroid treatment regimen on refractory childhood seizures and a review of other corticosteroid treatments. Eur. J. Paediatr. Neurol, 2015.
Scheffer, I. E., Boysen, K. E., Schneider, A. L., Myers, C. T., Mehaffey, M. G., Rochtus, A. M., ... & Poduri, A. BRAT 1 encephalopathy: a recessive cause of epilepsy of infancy with migrating focal seizures. Developmental Medicine & Child Neurology, 2019.
Ballaban-Gil K., Tuchman R. Epilepsy and epileptiform EEG: association with autism and language disorders. Ment Retard DevDisabil Res. Rev, 2000; 6 (4): 300–308.ссылка
Conroy, J., McGettigan, P. A., McCreary, D., Shah, N., Collins, K., Parry‐Fielder, B., ... & Webb, D. Towards the identification of a genetic basis for L andau‐K leffner s yndrome. Epilepsia, 2014; 55 (6): 858-865.
Besag F., Vasey M. Social cognition and psychopathology in childhood and adolescence. Epilepsy Behav, 2019.ссылка
Cockerell I, Bølling G, Nakken KO. Landau-Kleffner syndrome in Norway: long-term prognosis and experiences with the health services and educational systems. Epilepsy Behav, 2011; 21(2):153-159.
Sinclair D., Snyder T. Corticosteroids for the treatment of Landau-kleffner syndrome and continuous spike-wave discharge during sleep. Pediatr. Neurol, 2005; 32 (5): 300-306. ссылка
Escobar Fernández L, Coccolo Góngora A, Vázquez López M, Polo Arrondo AP, Miranda Herrero MC, Barredo Valderrama E, Castro de Castro P. [Continuous spike-waves during slow-wave sleep: Experience during 20 years]. An Pediatr (Barc), 2019; 91(3): 180-188. ссылка
Landau VW, Kleffner FR. (1957) Syndrome of acquired aphasia with convulsive disorder in children. Neurology 7: 523– 530.
Nakato S, Okuno T, Mikawa H. Landau–Kleffner syndrome: EEG topographic studies. Brain Dev, 1989; 11: 43-50.
Feekery C., Parry‐Fielder B., Hopkins I. Landau–Kleffner syndrome: six patients including discordant monozygotic twins. Pediatr Neurol 9, 1993; 49-53.ссылка
Классификация эпилепсии Международной противоэпилептической лиги: пересМотр и обновление 2017 года Авакян Г.Н., Блинов Д.В., Лебедева А.В., Бурд С. Г., Авакян Г. Г. ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России, Москва.

