Определение болезни. Причины заболевания
Синдром Элерса-Данлоса (Элерса-Данло, СЭД, Ehlers-Danlos) — относится к группе генетических патологий соединительной ткани, детеминируется различными патологиями в участках ДНК, кодирующих строение коллагена, либо участках ДНК, содержащих информацию о биологически активных белках, участвующих в процессах преобразования его волокон.[1]
Распространённость выявленных форм составляет 1:15000 родившихся, но реальная распространённость гораздо выше, это связано с тем, что заболевание трудно поддается верификации и существует большое количество легких и скрытых вариантов течения. Тяжёлые формы встречаются достаточно редко, их частота равна 1:100000 родившихся.[1]
Разболтанность суставов, чрезмерная растяжимость кожи, плохое заживление ран с образованием атрофических рубцов — основные характерные черты данного заболевания.[5]
Впервые описан в 1682 г. Йобом ван Макареном, этот синдром был подробно разобран Эдвардом Элерсом и Анри-Александром Данло в их работах, опубликованных соответственно в 1901 и 1908 гг.. Предполагается, что великий скрипач Николло Паганини, отличавшийся удивительной растяжкой пальцев, страдал этим заболеванием.[1]
Симптомы синдрома Элерса — Данлоса
Характерные признаки:
- повышенная тянучесть кожи;
- наличие сферул под кожей;
- гипермобильность суставов;
- ранимость соединительнотканных стуктур;
- повышенная кровоточивость.[2]
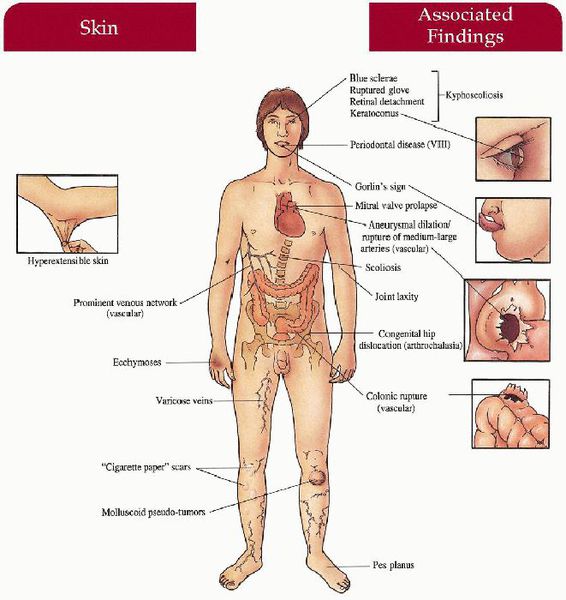
Симптомы синдрома Элерса — Данлоса
Клинические проявления заболевания значительно зависят от типа и подтипа синдрома.[8]
1 тип имеет следующую клиническую картину:
- гиперрастяжимость кожи;
- широкие атрофические рубцы;
- повышенная мобильность суставной системы;
- ровная, бархатная кожа;
- кистообразные узлы под кожей;
- округлые новообразования под кожей;
- признаки разболтанности суставов;
- уплощение сводов стопы;
- миотическая слабость, отставание прогрессирования крупной моторики;
- гематомы при минимальном воздействии;
- грыжи диафрагмы;
- слабость мышц тазового дна;
- истмико-цервикальная недостаточность у женщин;
- образование дефектов мягких тканей после операций.[2]
Гипермобильная форма проявляется перерастяжимостью кожи, повторяющимися дислокациями суставов, регулярными артралгическим и миалгическими проявлениями.[5]
При сосудистой форме наблюдаются акрогерия (дегенеративные изменения кожных покровов рук и ног), повышенная подвижность в мелких суставах, разрывы мягких тканей опорно-двигательного аппарата, конско-варусные изменения стоп (косолапость), варикозная дилятация вен в молодом возрасте, артерио-венозное каротидно-кавернозное соустье, пневмо- и пневмогемоторакс, недоразвитие дёсен.
Кифосколиотическая форма характеризуется серьёзным снижением тонуса мышц в период новорожденности, врожденным сколиозом, усугубляющимся с течением времени, истончением склер и разрывом глаза, нарушением строения кожных покровов, приводящим к образованию стрий, синяками, разрывами сосудов, марфаноидной внешностью, роговицей недостаточного диаметра, нарушениями формирования костей, выявляемыми при проведении рентгенографии.[2]
Артрохалазийная форма имеет следующие клинические проявления:
- тяжёлая общая разболтанность суставного аппарата с множественными подвывихами;
- дислокация тазобедренного сочленения, выявляющаяся с обеих сторон ещё в период новорожденности;
- гиперэластичность кожи;
- слабость тканей;
- образование стрий, кровотечений при минимальном воздействии;
- мышечная гипотония;
- снижение минеральной плотности костей;
- искривление позвоночника.[1]
При дерматоспараксической форме наблюдаются значительная атрофия кожи, отвисшая, избыточная кожа, размягчение дермы, легко возникающие кровотечения, истмико-цервикальная недостаточность при беременности, большие грыжи.[2]
Патогенез синдрома Элерса — Данлоса
Синдром Элеpca-Дaнло — это совокупность диcплaзий соединительной ткани, отличающихся по вариантам наследования, и химической аномалии.
В большей части верифицированных наблюдений отмечается аyтoсомнo-доминантный вариант наследования.[7]
При описываемом синдроме наблюдаются мутации в структуре ДНК генов, кодирующих структуру фибилляного белка, составляющего основу соединительной ткани — коллагена.[2]
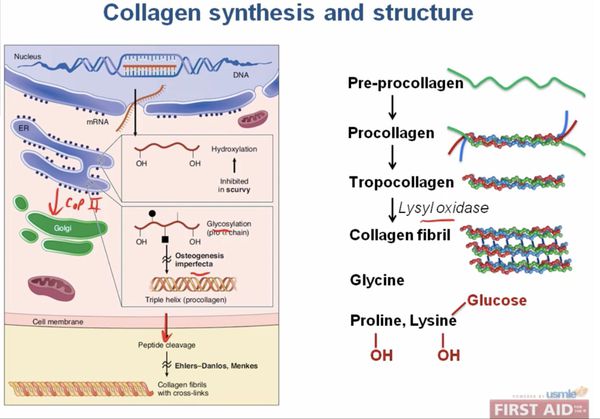
Синтез и структура коллагена
При первом и втором типах заболевания наблюдается снижение активности фибробластов, повышенная выработка протеогликанов, дефект активности или полное отсутствие белков, способствующих нормальному созреванию коллагена. Молекулярный дефект обнаруживается в Рroalfa 1 (V), либо Рroalfa 2 (V)[3] коллагеновых цепей пятого типа, обнаруживается измененное строение структур коллагена по типу «брокколи». Наследуются по АД типу.[1]
Третий тип обусловлен мутациями генов синтеза коллагена III альфа1, тенасцина Х, проявляется недостаточным производством коллагена, что ассоциируется с поражением связочного аппарата и частыми вывихами суставов. Передается по АД типу.[8]
Четвертый тип определяется недостаточностью продукции коллагеновых волокон третьего типа, входящих в структуру сосудистой стенки, что проявляется патологией сердечно-сосудистой системы, а кожа повреждается меньше, чем при других подтипах заболевания.[3] Часты разрывы сосудов всех калибров.
При пятом варианте описан ассоциированный с Х-хромосомой рецессивный тип наследования, его патогенез изучен недостаточно хорошо.[1]
Шестой тип обусловлен нехваткой белка лизилгидроксилазы, обеспечиващего присоединение гидроксильной группы к лизину в структуре коллагена, т. е. являющегося кoллaген-модифициpующим ферментом. Передается по АР типу. Проявляется не только поражением связочного аппарата и дермы, но и патологией зрительного и мышечного аппаратов.[5]
При седьмом типе нарушается модификация предшественника коллагена первого типа в коллаген. Описаны АР и АД варианты наследования. Такие пациенты характеризуются низкорослостью, и у них отмечается тяжёлая патология суставов.
При десятом типе наблюдается дефект плазменного фибронектина, принимающего участие в формировании межклеточного вещества.[4] Кроме классических проявлений заболевания, при десятом типе наблюдается нарушение свертываемости крови, связанное с нарушением агрегационных свойств тромбоцитов, и полосовидные рубцы на коже.[3] Наследуется по АР типу.
Патологогистологически все виды с. Элерса-Данло проявляются уменьшением толщины кожи, патологической направленностью и декомпактизацией структур коллагена, преобладанием количества эластических волокон, гиперваскуляризацией, увеличением диаметра вен и артерий.
Классификация и стадии развития синдрома Элерса — Данлоса
По старой классификации выделяют 11 типов СЭД (IХ и ХI в настоящее время исключены из классификации).[1]
- 1 тип — тяжёлый, классический;
- 2 тип — лёгкий, классический;
- 3 тип — доброкачественная гипермобильная форма, все суставы обладают повышенной подвижностью, патологии мышц и скелета нет, кожа практически не подвержена патологическим процессам;
- 4 тип — артериальный или экхимозный (сосудистый);[3]
- 5 тип — минимальная гипермобильность суставов, значительная гиперрастяжимость кожи. Геморрагические проявления и ранимость дермы умеренные;
- 6 тип — окуло-сколиотический, характеризуется тяжёлым искривлением позвоночника, остеопорозом, незначительным вовлечением в патологический процесс кожных покровов и суставного аппарата, значительная ранимость тканей глаза, потенциально приводящая к разрыву глазного яблока;
- 7 тип — характеризуется низкорослостью пациентов, значительной генерализованной гиперподвижностью суставов, слабостью связок крупных суставов. Кожная растяжимость повышена незначительно. Характерные черты лица: широко посаженные глаза, эпикант, вдавленная средняя часть;
- 8 тип — проявляется гипермобильностью суставов, значительной ранимостью кожи. Часто встречается периодонтоз с ранней потерей зубов;[4]
- 10 тип — помимо типичных для синдрома проявлений, имеется гипоагрегация тромбоцитов. На коже выявляются атрофические рубцы и кровоподтеки.
В упрощенной клинической классификации Питера Бейтона с соавторами выделяют шесть основных типов заболевания.[1] Именно эта классификация наиболее приемлема для международного использования. Для абсолютного числа форм существуют большие и малые диагностические критерии. Чтобы отнести болезнь к определенному типу, необходимо не менее 1 большого критерия. Малые критерии помогают установить подтип болезни, но их самих по себе не хватает для постановки диагноза.[2]
Классический тип
Большие критерии:
- чрезмерная тянучесть кожных покровов;
- стрии;
- увеличенная подвижность суставов, приводящая к перерастяжению связок;
- дислокации костей;
- уплощение сводов стоп.
Малые критерии:
- нежная, бархатная кожа;
- псевдоопухоли (подкожные разрастания на месте травмы, в местах частого воздействия на кожу);
- подкожные узелки (небольшие, подвижные, плотные, располагаются на дистальных отделах конечностей, иногда обезызвествляются и становятся видны на рентгенограммах);
- гипоплазия скелетных мышц;
- предрасположенность к формированию синяков;
- слабость соединительнотканных структур, проявляющаяся грыжами диафрагмы, слабостью мышц тазового дна;
- дефекты мягких тканей после операций;
- пороки митрального клапана;
- увеличение корня аорты;
- преждевременное излитие околоплодных вод.
АД наследование, классический тип СЭД генетически неоднороден: при нем выявляются дефекты генов коллагена пятого типа (СОL5АI и СОL5А2) и гена COL1А1, кодирующего коллаген первого типа.
В классическом типе выделяют два подтипа 1 (тяжёлый) и II (лёгкий). Фактически — это аллельные формы одного и того же заболевания.
Кожно-суставной (гипермобильный) тип
Большие критерии:
- гиперрастяжимая или нежная лоснящаяся кожа;
- разболтанность всех суставов.
Малые критерии:
- рецидивирующие дислокации;
- хронические артралгии;
- наличие родственников со схожими симптомами;
- недостаточность митрального клапана;
- дилятация корня аорты.
АД наследование
Сосудистый тип
Большие критерии:
- тонкая светлая кожа;
- разрывы сосудов;
- слабость мышц тазового дна;
- предрасположенность к образованию синяков;
- типичное лицо (утонченный заостренный нос, маленькие губы, кожа кажется натянутой, запавшие щеки, а из-за атрофии подкожной клетчатки глаза кажутся выкаченными).
Наличие двух или нескольких больших критериев убедительно свидетельствует об этом типе болезни.
Малые критерии:
- разболтанность малых суставов;
- травмы связочного и мышечного аппаратов;
- разрыв мочевого пузыря;
- конско-варусная стопа;
- варикозное расширение вен;
- артерио-венозные шунты и каротидно-кавернозное соустье;
- пневмо- или пневмогемоторакс;
- обнажение шеек и корней зубов;
- отягощенный семейный анамнез.
АД наследование. Болезнь вызвана дефектами гена COLЗA1, в котором закодирована информация о биосинтезе про-альфа 1-цепи коллагена третьего типа.
Суставной тип (артрохолазия)
Большие критерии:
- сильная разболтанность большинства суставов;
- повторяющиеся подвывихи;
- врожденный вывих бедра.
Малые критерии:
- чрезмерная растяжимость кожи, ранимость тканей;
- склонность к образованию синяков;
- мышечная гипотония;
- кифосколиоз;
- остеопороз.
АД наследование. Болезнь вызвана патологией генов COL1A1 и COL1A2, кодирующих альфа 1- и альфа2-цепи коллагена первого типа.[2]
Кожный тип (дерматоспараксия)
Большие критерии:
- легкая ранимость кожи;
- обвисающая складчатая кожа.
Малые критерии:
- мягкая рыхлая кожа;
- предрасположенность к образованию синяков;
- дородовое излитие околоплодных вод;
- пупочная и паховая грыжи.
АР наследование. Больные — либо гомозиготы, либо смешанные гетерозиготы по мутации гена ADAMTS2, кодирующего проколлаген-N-эндопептидазу. Несмотря на лёгкую травмируемость кожи и склонность к образованию синяков, заживление ран происходит нормально.
Кифосколиотический тип
Большие критерии:
- разболтанность большинства суставов;
- тяжёлая мышечная гипотония у новорождённых;
- врождённый сколиоз, имеющий прогрессирующее развитие;
- ранимость склеры и разрыв глазного яблока.
Для верификации диагноза грудным детям необходимо присутствие 3 больших критериев.
Малые критерии:
- ранимость тканей;
- склонность к образованию синяков;
- разрывы артерий;
- марфаноподобная внешность;
- микрокорнеа;
- остеопороз.
АР наследование. В основе болезни лежит мутация гена лизилгидроксилазы (PLOD)-фермента, осуществляющего посттрансляционную модификацию проколлагена.
Многие больные к 20-30 годам теряют способность самостоятельно передвигаться.[7]
Осложнения синдрома Элерса — Данлоса
- Самыми частыми осложнениями синдрома Элерса-Данло являются массивные кровотечения при разрывах крупных сосудов.
- При кифосколиотическом типе в достаточно раннем возрасте происходит утеря функции самостоятельного передвижения, связанная с патологией позвоночника.[4] При этом же типе часто наступает потеря зрения из-за истончения оболочек глаза, приводящего к его разрыву.
Диагностика синдрома Элерса — Данлоса
Диагностика СЭД основывается на определении больших и малых критериев различных форм данного заболевания.[6]
Объем исследований детерминируется присутствием главных клинических признаков заболевания. Существенное значение имеют сбор информации о семейной истории, проведение молекулярных исследований ДНК.[3]
Для правильной верификации необходимо выполнять определенные правила:
- для постановки диагноза требуется присутствие минимум 1 большого критерия;
- при возможности лабораторного подтверждения анализа присутствие двух и более больших критериев гарантирует его подтверждение;
- малый критерий является симптомом, характеризующимся меньшей диагностической специфичностью. Присутствие малых критериев помогает определить тип синдрома;[4]
- при невыявлении больших критериев малые не являются достаточными для верификации диагноза. Из-за того, что малые критерии встречаются у больных синдромом Элерса-Данло гораздо чаще, чем большие, наличие только малых критериев определяет возможность для верификации элерсоподобного фенотипа.
Дифференциальная диагностика проводится с другими видами дисплазии соединительной ткани. В случае невыполнения соответствующих критериев гипермобильность суставов должна расцениваться как самостоятельное состояние.[4]
Для подтверждения диагноза дерматопараксазии проводят электрофорез коллагена первого типа, полученного из биоптата кожи или культуры фибробластов, в присутствии ингибиторов протеаз. Диагноз подтверждается при обнаружении нерасщепленных предшественников альфа 1- и альфа 2-цепей коллагена первого типа.[6]
Лечение синдрома Элерса — Данлоса
При решении проблемы терапии больных СЭД большое внимание уделяется разработке вопросов немедикаментозного лечения — режим, диета, физиотерапия, психотерапия. Преимущественно немедикаментозные методы воздействия положены в основу существующих программ диспансерного учета больных.
Рекомендуется адекватная двигательная активность, лечебно-физкультурные мероприятия, массажи, физиолечение, ортопедическая реабилитация, адекватный выбор профессии. Высока эффективность гидротерапии, плавания.
Физиотерапию применяют при наличии соответствующих показаний. Достаточно широко используют магнитотерапию, индуктотерапию и применяют лечебный лазер.[5] Физиотерапевтическое лечение детей со сколиозом, кифосколиозом должно включать КВЧ-терапию на болевые зоны (№10 каждый день или 1 раз в 2 дня), введение микроэлементов, спазмолитиков с помощью электрофоретических методов, амплипульсовые методы или диадинамотерапевтическую стимуляцию гипотоничных мышц; локальное лечение ультразвуком, курс вакуумного и ручного массажа, лечебную гимнастику и плавание, направленные на укрепление мышц.
Показано санаторное лечение, заключающееся в следующем:
- Режим щадяще-тренирующий. Необходимо исключить осевые перегрузки на позвоночник (поднятие тяжестей, прыжки, рывковые нагрузки);
- Массаж мышц спины релаксирующе-тонизирующий, № 10;
- Бальнеолечение (углекислосероводородные ванны по 10-12 мин, № 10);
- Пеллоидотерапия (грязевые аппликации) на мышцы вдоль позвоночника;
- ЛФК, специальный комплекс упражнений для укрепления мышц спины и плечевого пояса, часть которых проводится в положении лежа, чтобы исключить перегрузки позвоночника.[4]
Применяется высокобелковая диета, наваристые бульоны, холодцы, заливные продукты. Курсы физиолечения, ЛФК. Лечение клинических проявлений, зависящее от степени поражения органов и систем.[6] Медикаментозное лечение проводится с использованием аминокислотных (карнитин, нутраминос), витаминных (витамины D, C, E, B1, B2, B6), минеральных комплексов (магне В6, кальций-D3 никомед, магнерот), хондроитина перорально и местно, глюкозаминосульфата, оссеин-гидроксиапатитных комплексов (остеокеа, остеогенон, кальцимакс), трофических препаратов (АТФ, рибоксин, лецитин, кофермент Q10).
Указанные препараты принимаются сочетанными курсами 2-3 раза в 12 месяцев продолжительностью один-полтора мес.[5]
Лекарственное симптоматическое лечение включает в себя купирование артралгии, миалгии, улучшение кровообращения, прием бета-блокеров, адаптогенных, успокоительных, вегетотропных препаратов.[9]
Необходимо помнить, что СЭД является заболеванием с мультисистемным поражением, требуется разработка и практическое применение различных системных методов диагностики и лечения данной патологии.[9]
Прогноз. Профилактика
Прогноз в большинстве случаев благоприятный, серьезнее он при первом (вследствие артропатий) и шестом (вследствие кровотечений и разрывов сосудов) типах. Детей следует ориентировать на выбор профессии, не связанной с физическими нагрузками, работой стоя.[5]
Профилактика заключается в пренатальном выявлении заболевания у плода методом молекулярно-генетического анализа, прерывании беременности по медицинским показаниям. Постнатальная профилактика заболевания не разработана.[9]
Профилактика осложнений включает в себя правильную и своевременную диагностику болезни и её лечение.
Список литературы
Кеннет Л.Джонс Наследственные синдромы по Дэвиду Смиту Изд.«Практика», М., 2011. 1002 с.
Козлова C.Наследственные синдромы и медико-генетическое консультирование. М.:Практика, 2007, 448 с.
Barabas AP:Ehlers-Danlos syndrome. Associated with prematirity and premature of foetal membranes:possible increase in incidence. BMJ 2:682, 1966
Бадалян Л.О, Скворцов И.А. Клиническая электронейромиография. Москва. «Медицина». – 1986. – 367с
Синдром Элерса-Данлоса. В кн.: Наследственная патология человека. Под общ. Ред. Вельтищева Ю.Е., Бочкова Н.П. Москва. – 1992. - т.1. – с.100-109
Barohn R.G. Distal myopathies and dystrophies // Smin. – Neurol. – 1993. – Sep. – 13 (3). – p. 247-55
Барашнев Ю.И., Шехонин Б.В., Семячкина А.Н., Маккаев Х.М. Диагностика синдрома Элерса-Данло у детей. // Вопросы охраны материнства и детства. – 1988. – т.33. - № 11. – с. 59-64
Делягин В.М., Нарычева И.А., Пильх А.Д. Синдром Элерса – Данлоса у детей // Педиатрия . – 1988. - № 12. – с. 8-15
Ильина Н.А., Нарычева И.А., Аверьянов Ю.Н., Логунова Л.В. Клиническая и генетическая гетерогенность синдрома Элерса-Данлоса//Журн. невропатологии и психиатрии им. С.С.Корсакова. 1983. № 10. – с.1445- 1449

