Определение болезни. Причины заболевания
Синдром внезапной детской смерти (СВДС; Sudden infant death syndrome) — это внезапная смерть ребёнка в возрасте от 7 дней до одного года жизни, причина которой неизвестна [1].
Этот диагноз устанавливают путём исключения. Сначала эксперты тщательно ищут возможные объяснения, например травму, удушье, генетические мутации, инфекции и пороки развития. При посмертном расследовании проводят комплексное вскрытие, осмотр кроватки ребёнка, а также внимательно изучают всю информацию о состоянии здоровья малыша и его семьи [6][11]. Если никакая из возможных причин не подтверждается, то ставят СВДС [2][3].
По международному соглашению экспертов Сан-Диегского консенсуса от 2004 года утверждено, что при любом, даже малейшем, подозрении на объективную причину смерти нельзя ставить диагноз «СВДС» [9]. Из-за таких тщательных исследований всех возможных факторов семья малыша и врачи находятся под постоянным психологическим давлением до тех пор, пока не выяснят причину или не поставят СВДС. Когда расследование завершается, стресс от потери ребёнка на годы остаётся тяжёлым грузом для родителей.
Распространённость синдрома внезапной детской смерти
Этот синдром является причиной примерно трети всех случаев летальных исходов в младенчестве [1]. Статистика СВДС сильно разнится: от 0,6 до 7 случаев на 1 тыс. новорождённых [5]. Такая вариативность связана с особенностями ухода за младенцами и распространённостью профилактических программ. В регионах, где родители строже следят за деталями сна ребёнка, например принципиально не кладут малыша спать на животе, показатели СВДС существенно ниже. Однако даже внутри одной страны ситуация может значительно отличаться, к примеру в России в зависимости от региона число таких трагедий отличается в десятки раз: от 0,06 до почти 3 случаев на тысячу малышей [1][5][7]. Статистика показывает, что этому синдрому больше подвержены мальчики [14].
Причины и факторы риска развития СВДС
Внезапная смерть малыша — итог воздействия целого каскада факторов. Как правило, учёные придерживаются гипотезы, которая называется моделью тройного риска (Triple Risk Model) [19][20]. В 1990-х годах её выдвинули Джеймс Филиано и Ханна Кинни. Она заключается в предположении о том, что для такого происшествия нужно совпадение трёх факторов: врождённой или приобретённой ослабленности организма малыша, возрастного окна повышенной уязвимости и внешнего провоцирующего фактора.
Первое звено цепи — факторы, которые могут ослабить организм ребёнка. К ним относятся:
- генетическая предрасположенность, например наличие ночного апноэ (остановки дыхания во сне) у родственников;
- особенности течения беременности, в том числе многоплодность;
- степень зрелости при рождении (недоношенность повышает риск);
- наличие гипоксии (кислородной недостаточности), влияющей на нервную систему ребёнка;
- особенности метаболических (обменных) процессов;
- состояние иммунитета;
- другие скрытые состояния [14][18][19][21][22][23].
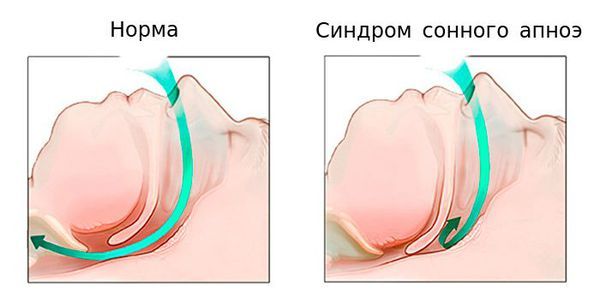
Нормальное поступление воздуха и синдром сонного апноэ
Вторым компонентом модели СВДС является критический период — так называемое окно повышенной уязвимости в начале жизни ребёнка, когда максимально важно внимательно ухаживать за малышом и снижать влияние неблагоприятных факторов, если их невозможно устранить полностью. Примерами стрессоров этого периода являются зимнее время года и ночное апноэ длительностью более 9–12 секунд на первой неделе жизни.
Статистика показывает, что примерно 80 % трагических случаев происходит в первые четыре месяца после рождения, а примерно 90 % — в первые полгода [1][6]. В это время в центральной нервной системе (ЦНС) малыша идёт перестройка, формируются новые нейронные связи, настраиваются сложные системы контроля дыхания и жизненных рефлексов. Однако защитные механизмы ещё не особо развиты, они чувствительны к любым изменениям, особенно к метаболическим. Именно поэтому организм новорождённого в эти месяцы уязвим перед третьим элементом модели — внешними провоцирующими факторами [11]. К ним относятся бытовые факторы, которые может исключить родитель:
- поза во сне (особенно сон на животе или на боку);
- перегрев или переохлаждение малыша;
- искусственное вскармливание;
- мягкая поверхность для сна, большое количество одеял, подушек и мягких бортиков вокруг ребёнка;
- наличие игрушек в кроватке;
- приём лекарств, назначенных малышу (терапию можно отменять только после консультации с врачом);
- пассивное курение ребёнка или матери, а также активное курение и приём алкоголя во время беременности и грудного вскармливания;
- совместный сон со взрослыми (особенно если родители курят или употребляют алкоголь) и т. д. [5]
Например, если ребёнок спит на животе, риск СВДС может возрасти в 14 раз [1][8][11]. Сон в такой позе может привести к разным последствиям: от затруднённого дыхания до сдавливания позвоночной артерии, при котором к мозговому стволу поступает меньше крови. У многих малышей не срабатывает защитный механизм пробуждения, из-за чего нарушения продолжают прогрессировать.
В случае пассивного курения у ребёнка нарушается работа серотонинергической системы мозга (сети нервных клеток, которая использует серотонин для передачи сигналов и регулирует сон, настроение и другие механизмы), из-за чего он хуже реагирует на угрожающие сигналы вроде гипоксии [9].

Серотонинергическая система головного мозга
Симптомы СВДС
Парадокс этого серьёзного диагноза заключается в том, что никаких типичных симптомов у СВДС нет. Многочисленные исследования выявили только механизмы и возможные каскады патологических процессов, которые приводят к смерти. Современные системы мониторирования позволили увидеть некоторые предвестники СВДС. Учёные Европейского союза отмечают, что абсолютное большинство трагедий случается именно ночью, причём в промежутке между полуночью и шестью утра.
Одним из подобных настораживающих симптомов является прогрессирующая брадикардия — медленное, но необратимое замедление сердечного ритма. Изменение работы сердца связано с тем, что из-за недостатка кислорода нарушается работа сердечной мышцы. Непосредственно перед СВДС наблюдаются приступы учащённого дыхания, которые возникают из-за тотального угнетения дыхательного центра. Терминальные проявления отражают уже необратимые изменения. К таким симптомам относятся остановка дыхания, изменение цвета кожи, в частности синюшность (цианоз), снижение мышечного тонуса, рвота и дефекация [8][9].

Нормальный ритм и брадикардия
Таким образом, заранее предугадать СВДС невозможно, но его можно предупредить.
Патогенез СВДС
Учёные выделяют несколько основных гипотез о механизмах развития СВДС.
Одной из них является предположение о нейробиологической незрелости. У части детей «центр пробуждения» мозга развит недостаточно. Причинами недоразвития могут быть генетические мутации, метаболические нарушения и аномалии строения мозга. Однако ключевую роль играет серотонинергическая система, которая регулирует дыхание, сердцебиение и реакцию пробуждения при опасности. Если она работает некорректно, может произойти трагическая ситуация, например во время сна на животе ребёнок может уткнуться в матрас или подушку, что затруднит дыхание и приведёт к недостатку кислорода. При нарушении работы этой системы у малыша сигнал к пробуждению слабый или вообще не передаётся, поэтому ребёнок не переворачивается, а гипоксия прогрессирует.

Механизм развития СВДС при гипоксии
Другая гипотеза рассматривает механизм СВДС через призму кардиологической причины. Около 10–15 % случаев этого синдрома вызваны каналопатиями — невидимыми генетическими дефектами ионных каналов сердца, которые в основном связаны с мутациями в генах SCN5A и KCNQ1 [18][19]. Малыш может нормально развиваться и внешне ничем не отличаться от других детей. Однако в какой-то момент внешний фактор может стать причиной смертельной аритмии, особенно после высокой температуры в раннем возрасте.
Также существует гипотеза о метаболических причинах развития СВДС. В её основе лежит дефицит особого фермента MCAD (среднецепочечной ацил-КоА-дегидрогеназы), из-за которого нарушается окисление жирных кислот. Организм малыша не может получить энергию для сердца и головного мозга из основных источников — глюкозы и кетонов, которые получаются в ходе переработки накопленных жиров.
Если у ребёнка не хватает этого фермента и он долго ничего не ест, организм впадает в стресс и пытается переключиться на режим выживания. В этот момент уровень глюкозы в крови падает, но и кетоны не вырабатываются (из-за ферментного сбоя). В результате возникает гипокетонемическая гипогликемия, при которой малыш не может ниоткуда получить энергию.
На этом фоне запускается цепочка негативных реакций. Из-за энергетического дефицита возникают токсические эффекты: сердце может реагировать нарушением ритма или снижением сократимости, а влияние на мозг может проявляться судорогами или потерей сознания. В итоге все жизненно важные системы работают неправильно. Без энергии быстро развивается мозговая дисфункция (может привести к коме), серьёзно страдают органы внутренней секреции, может возникнуть почечная недостаточность. Если вовремя не оказать помощь, могут произойти необратимые изменения, многократно повышающие риск летального исхода [21][22].
Ещё одна гипотеза рассматривает инфекционно-токсический механизм развития СВДС. У некоторых малышей могут быть скрытые предрасположенности: уязвимость дыхательного центра в мозге, особенности иммунитета или генетическая предрасположенность.
На этом фоне может казаться, что ребёнок легко переносит обычную простуду, например насморк с кашлем, однако вирусная инфекция может серьёзно вредить организму. Вирус сначала атакует слизистые носа и горла, нарушает их защитный барьер и ослабляет местный иммунитет. В результате «спящие» условно-патогенные бактерии, которые до этого обитали на слизистых (например, золотистый стафилококк или кишечная палочка), получают возможность быстро размножаться и выделять суперантигены, провоцирующие активную реакцию иммунитета. В итоге развивается так называемый цитокиновый шторм, который разносит воспаление по всему организму. У ребёнка может резко упасть давление, нарушиться работа сердца и дыхательного центра в мозге. Таким образом, небольшой внешний фактор может стать фатальным для ребёнка с предрасположенностью к СВДС. В таких случаях родители говорят: «У малыша была простуда, мы думали она уже проходит». За этими словами стоит сложная биология детской уязвимости перед невидимой цепочкой реакций организма [23].
Классификация и стадии развития СВДС
Проблема СВДС актуальна во всём мире, но особенности классификации и подходы к диагностике различаются в зависимости от страны [15].
Международная классификация основана на иерархическом подходе, где СВДС является подкатегорией более широкого понятия — внезапной неожиданной смерти младенца (Sudden Unexpected Infant Death; SUID), при которой учитывают все непонятные причины детской смертности до года и проводят дифференциальную диагностику со случайной асфиксией, инфекционными, метаболическими и кардиологическими причинами.
Сан-Диегская классификация, принятая в большинстве стран Евросоюза, включает четыре категории, которые учитывают не только изменения в органах, обнаруженные при вскрытии, но и качество исследования:
- Категория I-A. К её характеристикам относится нормальный клинический анамнез (история болезни и жизни), отсутствие патологии и полное расследование, при котором не наблюдаются признаки других заболеваний и насильственной смерти. Подтверждается диагноз «синдром внезапной детской смерти».
- Категория I-B. Клинический анамнез не изменён, но расследование неполное: собрана не вся информация об обстоятельствах смерти, либо отсутствует одно или несколько лабораторных исследований. В таком случае ставят вероятный СВДС.
- Категория II. Все характеристики первой категории, но есть нетипичные признаки: возраст до 21 дня или старше 6 месяцев, наступление смерти в положении на спине, симптомы болезни или отягощённый акушерский анамнез. Диагностируют сомнительный СВДС.
- Неклассифицируемая внезапная смерть младенцев (USID). К ней относят детские смерти, при которых альтернативные диагнозы сомнительны, но ни к одной из вышеперечисленных категорий случай не подходит. Тогда СВДС тоже сомнительный, требуется дополнительное медицинское посмертное расследование.
В России применяют упрощённую систему, которую разработали Александр Цинцерлинг и Всеволод Воронцов в 1980-х годах. По ней выделяются две группы:
- I группа — полное отсутствие клинических и патологоанатомических признаков какого-либо заболевания;
- II группа — наличие минимальных неспецифических изменений (например, лёгкого бронхита или микровоспаления), недостаточных для объяснения смерти.

Воспаление бронха у ребёнка
Таким образом, подходы к классификации СВДС в мировой практике различны. Наиболее полным считается протокол концепции SUID [2].
Так как СВДС является внезапным и необъяснимым событием с летальным исходом, его клинические стадии не выделяют.
Осложнения СВДС
СВДС сам по себе является трагическим диагнозом и терминальным осложнением в виде летального исхода [4][10][11][12][24].
Последствия этого синдрома представляют собой многолетнюю психологическую травму для семьи малыша. Родители часто винят себя в случившемся [25]. У матерей, потерявших ребёнка, без специализированной психологической помощи возрастает риск самоубийства или смерти от несчастного случая.
Диагностика СВДС
СВДС не диагностируют при жизни, его можно установить только в ходе посмертного расследования после исключения всех других возможных причин [1][5].
В России используют стандартный комплексный подход к диагностике, включающий:
- патологоанатомическое вскрытие с макроскопическим и гистологическим исследованием органов и тканей;
- осмотр места происшествия;
- тщательный сбор анамнеза.
В Европейском союзе применяют международные, более подробные протоколы SUIDIRF (CDC/NIH), которые учитывают дополнительные лабораторные исследования, генетическое обследование, а также углублённое изучение причин и места происшествия.
Лечение СВДС
Специфического лечения СВДС не существует.
Если летальный исход наступил дома, то реанимационные мероприятия малоэффективны, так как возникшая гипоксия в момент обнаружения уже необратима. Однако если ребёнок находится в условиях, где рядом есть реанимационная бригада, то интенсивная терапия может спасти ему жизнь [1].
По всем российским и международным рекомендациям, главная помощь при СВДС — это психологическая поддержка семьи после случившейся трагедии [25].
Прогноз. Профилактика
Прогноз СВДС оценивают для семьи, потерявшей ребёнка. Врачи определяют психологические, репродуктивные и генетические риски, в том числе для последующих детей. Изучение причины и своевременное оказание психологической помощи родителям значительно снижает риски повторных случаев СВДС.
Профилактика синдрома внезапной детской смерти
Профилактика является единственной эффективной стратегией снижения смертности. Она основывается на устранении внешних факторов риска и своевременном выявлении скрытых патологий [8]. Это особенно важно в период наибольшего риска, когда внешние триггеры могут наложиться на критический этап развития младенца.
Абсолютное большинство случаев СВДС приходится на возраст между 1-м и 6-м месяцами жизни ребёнка, самый опасный период — 2–4-й месяцы. В это время родители немного выдыхают после тревожного начала: малыш начинает расти, выглядит бодрым, меньше просыпается ночью для кормлений. Однако практика показывает, что именно в этом возрасте риск СВДС максимален, поэтому важно придерживаться простых правил безопасного сна [1][6][7].
Международным сообществом сформулированы следующие рекомендации по снижению рисков СВДС:
- сон на спине — снижает риск в 14 раз;
- жёсткая поверхность для сна без мягких предметов и игрушек в кроватке — в 5 раз;
- избегание перегрева и пассивного курения — в 2–5 раз;
- отдельная кроватка в родительской комнате — на 50 %;
- грудное вскармливание (до 6 месяцев) — на 36–50 %;
- пустышка во время сна — на 30 % [8][16][26][17].
Особое внимание уделяют вторичной профилактике СВДС у братьев и сестёр умершего ребёнка, так как риск повторения трагедии в этом случае в 4–6 раз выше, потому что причиной СВДС могут быть как генетические особенности, так социальные особенности конкретной семьи [13].
Синдром внезапной детской смерти предсказать почти невозможно, но мировая практика показывает значительную эффективность профилактики СВДС в странах с национальными кампаниями: с 1994 года смертность снизилась на 50–70 % [8].
Список литературы
Баранов А. А., Багненко С. Ф. Синдром внезапной смерти младенцев: клинические рекомендации. — М., 2015. — 12 с.
Кравцова Л. А. Синдром внезапной смерти младенцев (SIDS): что нового? // Российский вестник перинатологии и педиатрии. — 2021. — Т. 66, № 2. — С. 13–20.
Шакирова Э. М., Харин Г. М., Шакирова А. З. Внезапная смерть грудного ребёнка // Практическая медицина. — 2010. — № 6 (45). — С. 14–18.
Ровда Ю. И., Зеленина Е. М., Миняйлова Н. Н., Крекова Н. П. Синдром внезапной детской смерти (СВДС) // Мать и дитя в Кузбассе. — 2018. — № 1 (72). — С. 96–106.
Травенко Е. Н., Породенко В. А., Быстрова Е. И., Ильина А. В. и др. Синдром внезапной смерти детей: учебное пособие. — Краснодар: КубГМУ, 2021. — 109 с.
Кораблева Н. Н. Оптимизация диагностики и профилактика жизнеугрожающих кардиореспираторных состояний у детей первого года жизни: дис. … д-ра мед. наук: 14.01.08. — Сыктывкар, 2020. — 232 с.
Блох Р. А., Цыбина Н. А., Соломаха А. Ю., Блох М. Е. Синдром внезапной детской смерти: эпидемиология, факторы риска, профилактика // Медицина: теория и практика. — 2021. — Т. 6, № 2. — С. 38–45.
Мальцев С. В., Мансурова Г. Ш. Современный взгляд на причины и профилактику синдрома внезапной смерти младенцев // Практическая медицина. — 2022. — Т. 20, № 5. — С. 22–28.
Opdal S. H., Stray-Pedersen A., Eidahl J. M. L., Vege Å., Ferrante L., Rognum T. O. The vicious spiral in sudden infant death syndrome // Frontiers in Pediatrics. — 2025. — Vol. 13.ссылка
Fraile-Martinez O., García-Montero C., Castellanos Díez S., Bravo C. et al. Sudden infant death syndrome (SIDS): state of the art and future directions // Int J Med Sci. — 2024. — Vol. 21, № 5. — P. 848–861.ссылка
Olecká I., Dobiáš M., Lemrová A., Ivanová K. et al. Indeterminacy of the diagnosis of sudden infant death syndrome leading to problems with the validity of data // Diagnostics (Basel). — 2022. — Vol. 12, № 7.ссылка
Beckwith J. B. Defining the sudden infant death syndrome // Arch Pediatr Adolesc Med. — 2003. — Vol. 157, № 3. — P. 286–290.ссылка
Glinge C., Rossetti S., Oestergaard L. B., Stampe N. K. et al. Risk of sudden infant death syndrome among siblings of children who died of sudden infant death syndrome in Denmark // JAMA Netw Open. — 2023. — Vol. 6, № 1.ссылка
Duncan J. R., Paterson D. S., Hoffman J. M., Mokler D. J. et al. Brainstem serotonergic deficiency in sudden infant death syndrome // JAMA. — 2010. — Vol. 303, № 5. — P. 430–437.ссылка
WHO. International Classification of Diseases for Mortality and Morbidity Statistics (ICD-11). — 8-th revision. — 2022.
Moon R. Y., Carlin R. F., Hand I. Sleep-related infant deaths: updated 2022 recommendations for reducing infant deaths in the sleep environment // Pediatrics. — 2022. — Vol. 150, № 1.ссылка
Vennemann M. M., Bajanowski T., Brinkmann B., Jorch G. et al. Does breastfeeding reduce the risk of sudden infant death syndrome? // Pediatrics. — 2009. — Vol. 123, № 3. — P. e406–e410.ссылка
Liebrechts-Akkerman G., Liu F., van Marion R., Dinjens W. N. M., Kayser M. Explaining sudden infant death with cardiac arrhythmias: complete exon sequencing of nine cardiac arrhythmia genes in Dutch SIDS cases highlights new and known DNA variants // Forensic Sci Int Genet. — 2020. — Vol. 46. ссылка
Wilders R. Cardiac ion channelopathies and the sudden infant death syndrome // ISRN Cardiology. — 2012. — Vol. 2012.ссылка
Guntheroth W. G., Spiers P. S. The triple risk hypotheses in sudden infant death syndrome // Pediatrics. — 2002. — Vol. 110, № 5.ссылка
Chang I. J., Lam C., Vockley J. Medium-chain acyl-coenzyme A dehydrogenase deficiency // GeneReviews. — 2024.ссылка
Mason E., Hindmarch C. C. T., Dunham-Snary K. J. Medium-chain acyl-CoA dehydrogenase deficiency: pathogenesis, diagnosis, and treatment // Endocrinol Diabetes Metab. — 2023. — Vol. 6, № 1.ссылка
Raza M. W., Blackwell C. C. Sudden infant death syndrome, virus infections and cytokines // FEMS Immunol Med Microbiol. — 1999. — Vol. 25, № 1–2. — P. 85–96.ссылка
Zhao F., Li M., Jiang Z., Tsien J. Z., Lu Z. Camera-based, non-contact, vital-signs monitoring technology may provide a way for the early prevention of SIDS in infants // Front Neurol. — 2016. — Vol. 7. ссылка
Gandino G., Diecidue A., Sensi A., Venera E. M. et al. The psychological consequences of sudden infant death syndrome (SIDS) for the family system: a systematic review // Front Psychol. — 2023. — Vol. 14.ссылка
Moon R. Y., Tanabe K. O., Yang D. C., Young H. A. et al. Pacifier use and SIDS: evidence for a consistently reduced risk // Matern Child Health J. — 2012. — Vol. 16, № 3. — P. 609–614.ссылка

