Определение болезни. Причины заболевания
Рак плевры (Pleural cancer) — это простонародное название группы злокачественных онкологических заболеваний плевры — тонкой ткани, которая покрывает лёгкие снаружи и грудную клетку изнутри, образуя замкнутое пространство (плевральную полость). Наиболее часто злокачественное поражение плевры сопровождается скоплением жидкости в плевральный полости (злокачественным плевральным выпотом). В таком случае пациенты жалуются на тяжесть в груди, чувство нехватки воздуха и одышку.
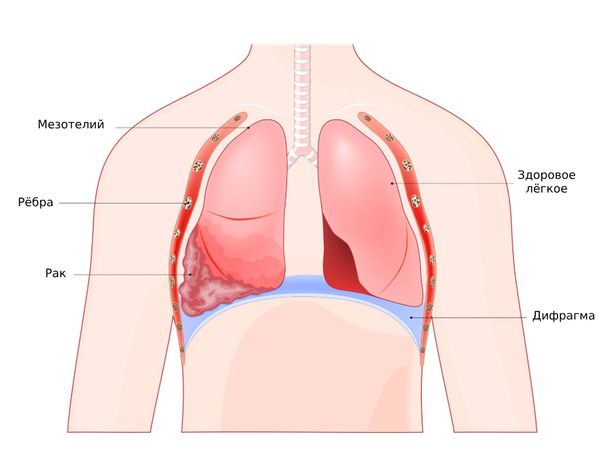
Рак плевры (мезотелиома)
В норме в плевральной полости также есть жидкость. Её объём составляет 15–20 мл. По составу она сходна с плазмой крови, но уровень белка в ней ниже. Эта жидкость необходима для нормальной работы лёгких.
Так как в плевре есть болевые рецепторы, в отличие от ткани лёгкого, её поражение может сопровождаться болью — это второй наиболее частый симптом заболеваний плевры, в том числе онкологических.
Распространённость рака плевры
Все варианты злокачественного онкологического поражения плевры можно разделить на 2 группы:
- Первичные злокачественные опухоли. Это редкие заболевания, среди которых чаще других встречается мезотелиома и солитарная фиброзная опухоль плевры. Распространённость мезотелиомы в разных странах не превышает 10 (от 3 до 9) случаев на 100 тыс. населения. Общедоступной статистики этой болезни в России нет, но она относится к редким заболеваниям [1][2]. Частота встречаемости солитарной фиброзной опухоли не превышает 0,2 случаев на 100 тыс. населения. В России описаны только отдельные случаи или серии наблюдений [3].
- Вторичное (метастатическое) поражение плевры при злокачественных опухолях других органов. Наиболее часто метастазы проникают в плевру при лимфоме, раке лёгкого, молочной железы и яичников. Ежегодно в США регистрируют 150 тыс., а в Англии — 50 тыс. новых случаев метастатического плеврита. Считается, что около 15 % всех злокачественных онкологических заболеваний осложняются метастатическим плевритом [4]. Среди пациентов с раком лёгких вторичное поражение плевры бывает у каждого 3-го пациента (37 %), а с раком молочной железы — у каждого 4-го (25 %) [5][6]. В России ежегодно регистрируют более 100 тыс. людей с метастатическим плевритом [22].
Причины развития рака плевры
Среди причин первичного опухолевого поражения плевры, в первую очередь мезотелиомы, самое важное значение имеют генетические факторы (мутации BRCA1‐ассоциированного белка BAP‐1), некоторые вирусы (например полиомавирус SV40), воздействие асбеста и радиации [1]. Метастатическое поражение плевры указывает на прогрессирование онкологического заболевания другого органа, т. е. метастатическое поражение плевры говорит о том, что первичная опухоль достигла 4-й стадии.
К факторам риска также относят табакокурение, частые стрессы и лучевое облучение по поводу лечения других онкологических заболеваний [21].
Вторичное злокачественное поражение плевры встречается гораздо чаще первичного, при этом их симптомы, стратегия диагностики и лечения во многом схожи, поэтому статья будет в первую очередь посвящена метастатическому поражению плевры.
Симптомы рака плевры (метастатического плеврита)
Самыми частыми симптомами метастатического поражения плевры являются одышка, чувство нехватки воздуха или затруднение дыхания (иногда даже в спокойном состоянии): они возникают у 50 % пациентов. Одышка нередко сопровождается ощущением тяжести в груди, обычно со стороны поражения. Причиной этих симптомов является скопление большого количества плевральной жидкости (плеврит), которая сдавливает лёгкое, смещает диафрагму вниз и давит на грудную клетку [4].
При мезотелиоме часто возникает боль на стороне поражения, причём иногда она появляется ещё до развития плеврита и одышки [6].
К сожалению, бывают случаи, когда начальные стадии болезни протекают бессимптомно. В большей степени это характерно для метастатического плеврита, так как должно пройти некоторое время, пока жидкости в плевральной полости не станет слишком много.
Также у пациентов с метастатическим плевритом могут быть общие симптомы онкологического заболевания: значимое снижение массы тела, общая слабость, отсутствие аппетита, тошнота, рвота и другие проявления раковой интоксикации [6].
Патогенез рака плевры (метастатического плеврита)
Плевра состоит из двух листков: париетальный (наружный) листок выстилает грудную клетку изнутри, а висцеральный (внутренний) покрывает лёгкое снаружи. В плевральной полости постоянно находится около 10–20 мл жидкости, которая выполняет роль смазки, т. е. уменьшает трение лёгкого о грудную клетку при дыхании. Плевральная жидкость постоянно образуется и всасывается со скоростью около 0,6 мл/час, причём производят эту жидкость оба листка плевры, а за обратное её всасывание отвечает только париетальный слой, у которого есть для этого специальные лимфатические дренажные микроотверстия. Скопление большого количества жидкости указывает на плеврит. Плевра получает кровоснабжение из большого круга кровообращения: париетальная её часть — из межрёберных артерий, а висцеральная — из бронхиальных [7].

Плеврит
При формировании метастатического поражения плевры опухолевые клетки распространяются через системный кровоток: как по большому кругу кровообращения, так и по малому. Сложный механизм «приклеивания» и закрепления циркулирующих опухолевых клеток ясен не до конца, однако известно, что он реализуется путём сложных межклеточных взаимодействий [6].
Кроме того, при метастатическом поражении плевры:
- лимфатические сосуды закупориваются, что усиливает скопление жидкости, характер которой меняется (в ней повышается количество хилезной жидкости — лимфы, содержащей жиры);
- проницаемость капилляров повышается;
- поверхность плевры изъязвляется за счёт гибели опухолевых клеток, из-за чего плеврит становится кровянистым;
- часть лёгкого сдавливается, т. е. развивается ателектаз с повышением давления в лёгочных сосудах, что усиливает образование плевральный жидкости [6];
- из-за перекрытия опухолью крупного бронха давление в плевральной полости может снизиться [23].
Мезотелиома плевры, как и другие первичные опухолевые поражения плевры, связаны с перерождением нормальных клеточных элементов плевры в опухолевые. В зависимости от преобладающего типа клеток выделяют три основных гистологических вида мезотелиомы: эпителиоидную, саркоматоидную и смешанную [9].
Классификация и стадии развития рака плевры (метастатического плеврита)
Как уже было сказано, злокачественное онкологическое поражение плевры принципиально классифицируется на первичное и вторичное.
Первичные злокачественные опухоли плевры (мезотелиома, солитарная фиброзная опухоль плевры) встречаются довольно редко. Для стадирования мезотелиомы применяют традиционную в онкологической практике TNM-классификацию, где T (tumor) — сама опухоль, а именно её распространённость и степень врастания в окружающие ткани, N (node) — наличие или отсутствие метастатического поражения внутригрудных или надключичных лимфатических узлов, а M (metastasis) — наличие или отсутствие отдалённых метастазов в других органах и тканях организма [1].
Солитарная фиброзная опухоль ранее условно подразделялась на два варианта: доброкачественный и злокачественный. В современной клинической практике такую классификацию не применяют, однако используют разные методы, которые помогают предположить риск прогрессирования или рецидива (возврата) опухоли после лечения. Эти методы носят исключительно специфический медицинский характер [11][12].
Также опухоли плевры делят на диффузные (выглядят как серозное утолщение без чётких контуров) и локализованные (формируются в виде узлов, которые имеют узкое или широкое основание). Чаще встречаются диффузные опухоли [22].
Вторичное злокачественное поражение плевры не имеет специфической классификации. Условно его можно разделить:
- По частоте возникновения:
- рецидивирующий — возникает повторно после удаления жидкости из плевральной полости;
- не рецидивирующий — жидкость в плевральный полости повторно не скапливается.
- По составу:
- хилезный — в жидкости содержится большой уровень лимфоцитов и триглицеридов;
- геморрагический — в жидкости присутствует большое количество элементов крови;
- серозный — в жидкости нет никаких примесей.
- По стороне поражения:
- левосторонний;
- правосторонний;
- двусторонний.
- По размеру:
- небольшой — занимает менее 2/3 объёма плевральный полости;
- большой — занимает более 2/3 объёма плевральный полости;
- массивный — занимает весь или почти весь объём плевральный полости [6].
Осложнения рака плевры (метастатического плеврита)
Основным осложнением является злокачественный плеврит, который развивается и при первичном, и при вторичном поражении плевры. Наличие плеврита в свою очередь приводит к дыхательной недостаточности и одышке, которая может быть выражена в лёгкой или тяжёлой степени.
Шкала одышки mMRC (Modified Medical Research Council)
| Степень | Тяжесть | Описание |
|---|---|---|
| 0 | Нет | Одышка появляется только при очень интенсивной нагрузке |
| 1 | Лёгкая | Одышка возникает при быстрой ходьбе или при подъёме на небольшое возвышение |
| 2 | Средняя | Из-за одышки пациенту приходится идти медленнее других людей того же возраста или ему необходимы остановки для отдыха |
| 3 | Тяжёлая | Одышка начинает беспокоить уже через несколько минут ходьбы по ровной поверхности |
| 4 | Очень тяжёлая | Одышка такой степени не позволяет пациенту выйти за пределы дома, она появляется уже при одевании или раздевании |
Другими специфическими осложнениями опухолевого поражения плевры могут быть:
- выраженный болевой синдром;
- нагноение с формированием эмпиемы плевры (скопления гноя в плевральной полости);
- кровотечение с развитием анемии или гемоторакса (скопления крови в плевральной полости);
- сдавление лёгкого с формированием частичного или полного ателектаза лёгкого;
- сдавление или смещение органов средостения с развитием сердечной недостаточности вплоть до остановки сердца;
- нарушения глотания (дисфагия);
- нарушения дыхания (стеноз, сдавление трахеи или бронхов) [6];
- пневмоторакс;
- асцит (скопление жидкости в брюшной полости), что также может вызвать тромбоз воротной вены [23].

Ателектаз
Диагностика рака плевры (метастатического плеврита)
При подозрении на опухолевое поражение плевры необходимо обратиться к торакальному онкологу или торакальному хирургу, который проведёт первичное обследование пациента и сформирует дальнейший план диагностических мероприятий.
В рамках первичного общения врач уточняет у пациента симптомы и давность их возникновения, а также наличие предрасполагающих факторов (частое взаимодействие с асбестом, работа в условиях радиации, случаи онкологических заболеваний у ближайших кровных родственников и у самого пациента).
Далее врач выполняет ультразвуковое исследование (УЗИ) плевральной полости, которое служит начальным инструментальным методом обследования. Если по результатам УЗИ у пациента подозревают поражение плевры, его направляют на компьютерную томографию (КТ), мультиспиральную компьютерную томографию (МСКТ) или магнитно-резонансную томографию (МРТ).
Компьютерная томография (КТ, МСКТ или ПЭТ-КТ с 18F-ФДГ) позволяет получить максимальный объём информации о характере и распространённости поражения плевры. Если в плевре наблюдается патологическое накопление ФДГ (контраста), это указывает на злокачественный характер поражения.

ПЭТ-КТ
МРТ может служить альтернативным методом исследования, однако стоимость и сложность выполнения (длительности процедуры, необходимость нахождения в замкнутом пространстве «трубы» магнитного томографа) ограничивает её применение в рутинной клинической практике [6]. При этом в сравнении с КТ у МРТ есть один плюс: во время МРТ пациент не подвергается воздействию рентгеновских лучей.
Так как чаще всего развивается вторичное злокачественное поражение, пациенту могут назначить обследование других органов, например УЗИ/МРТ/МСКТ/КТ органов брюшной полости, сердца, головного мозга и т. д. [24]
Важным и обязательным этапом диагностики опухолевого поражения плевры является морфологическое исследование биологического материала. Для этого проводят:
- пункцию плевральной полости с забором жидкости для последующего цитологического, иммуноцитохимического и биохимического исследования (эффективность ИЦХ не превышает 30–50 %);
- биопсию плевры (с помощью иглы Абрамса или в ходе торакоскопии), которая позволяет максимального достоверно установить диагноз [4].
Торакоскопию выполняют в условиях внутривенной седации («во сне») при сохранении самостоятельного дыхания пациента. На грудной клетке под местной анестезией делают один прокол размером 5–6 мм, после чего в плевральную полость вводят тонкую видеосистему, которая позволяет осмотреть всю плевру и при необходимости сделать биопсию. Это позволяет отказаться от пункции под контролем УЗИ и видеоторакоскопии, требующей полноценного наркоза и искусственной вентиляции лёгких пациента, что сопряжено с большим количеством осложнений и длительным пребыванием в стационаре [6][9].
Однопрокольная торакоскопия с биопсией плевры доступна в специализированных центрах и отделениях, в которых есть соответствующее оборудование. Показанием к её выполнению является наличие плеврита или подозрение на опухолевое поражение плевры.
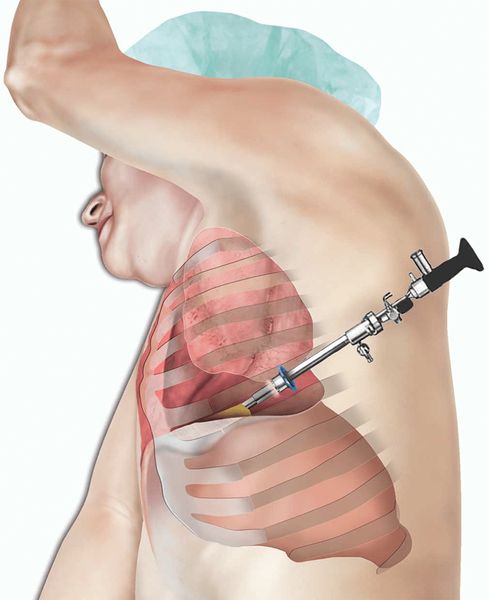
Торакоскопия
Лабораторные исследования в этом случае не имеют самостоятельного значения, их выполняют лишь как подготовительный этап перед проведением инструментальной диагностики в рамках стандартов обследования пациентов.
Однако при подозрении на мезотелиому или иное первичное опухолевое поражение материал биопсии исследуют на наличие молекулярных маркеров (онкобелка p16 и BRCA1-ассоциированного белка), определяемых при иммуногистохимическом исследовании. Этот метод помогает отличить доброкачественное деление клеток мезотелия от мезотелиомы плевры [8][10].
Дифференциальная диагностика
Опухолевые заболевания плевры необходимо отличить от ряда других заболеваний с похожей симптоматикой. К таким болезням относятся:
- плеврит или эмпиема плевры — накопление жидкости или гноя в плевральный полости;
- серозный плеврит (гидроторакс) — следствие сердечной или белковой недостаточности (например, у пациентов с циррозом печени);
- хилоторакс — проявление лимфангиолейомиоматоза (кистозного разрушения лёгочной ткани с поражением лимфатической системы и появлением опухолевидных образований органов брюшной полости), патологии грудного лимфатического протока или внутригрудных лимфатических узлов;
- гемоторакс — следствие травмы грудной клетки или поражения плевры на фоне экстрагенитального эндометриоза;
- утолщение плевры — результат перенесённого гнойного заболевания плевры, эмпиемы плевры, спаечного процесса после травмы грудной клетки или операции на лёгком;
- туберкулёзный плеврит — специфическое поражение плевры при туберкулёзе;
- поражение плевры при саркоидозе;
- силикоз с поражением плевры.
Лечение рака плевры (метастатического плеврита)
В отношении солитарной фиброзной опухоли основным методом лечения является хирургический, т. е. удаление опухоли в пределах здоровых тканей. В некоторых случаях такая операция требует удаления участка диафрагмы, грудной стенки, части или всего лёгкого. Однако при полном иссечении опухолевых клеток удаётся достичь хорошего долгосрочного результата: 10-летняя безрецидивная выживаемость составляет 70–80 %. Если в крае резекции обнаружили опухолевые клетки или в организме остался фрагмент опухоли, может применяться лучевая терапия.
Эффективность химиотерапии в отношении солитарной фиброзной опухоли не высока, оптимальные схемы химиотерапии не разработаны, поэтому в этом случае используют протоколы для лечения сарком мягких тканей [11][12].
Злокачественная мезотелиома ассоциирована с плохим прогнозом: около 50 % пациентов с этим заболеванием живут не дольше полутора лет. Для её радикального лечения применяют комбинированные схемы — сочетание химиотерапии с лучевой терапией или одним из вариантов хирургического лечения. При этом недавнее исследование выявило, что изолированное химиотерапевтическое лечение показывает лучшие результаты 2-летней выживаемости по сравнению с комплексным химиотерапевтическим и хирургическим лечением [13]. Для эпителиоидного варианта мезотелиомы основными препаратами являются Цисплатин + Пеметрексед, для неэпителиоидных вариантов — Ниволумаб или Ипилимумаб.
Вариантами радикальной операции при мезотелиоме плевры могут быть:
- Плевропневмонэктомия — удаление всего лёгкого вместе с костальной плеврой, покрывающей рёбра, диафрагмой и перикардом со стороны поражения. Это очень травматичная операция, сопряжённая с крайне высоким риском послеоперационной смерти пациента (до 12 %) или развитием тяжёлых осложнений (до 80 %), в связи с чем выполнение этой операции ограничено.
- Плеврэктомия (частичная или полная) — удаление плевры, покрывающей лёгкое и грудную клетку (декортикация и костальная плеврэктомия). Это более щадящий метод хирургического лечения, который в комбинации с химиолучевой терапией позволяет добиться хорошего результата без компромисса с качеством жизни пациента [14].
Терапия метастатического поражения плевры, как и симптоматическое лечение злокачественного плеврита при мезотелиоме, направлена на устранение одышки и дыхательной недостаточности и решает в первую очередь задачу по улучшению качества жизни. Соответственно, вариантами лечения могут быть:
- Торакоцентез — прокол и дренирование плевральный полости с удалением из неё жидкости. В большинстве случаев его выполняют в амбулаторных условиях под местной анестезией. Возможно проведение многократных повторных процедур. Это безопасный метод лечения, эффективный для быстрой помощи пациенту с дыхательной недостаточностью, вызванной большим количеством жидкости в плевральной полости. Однако торакоцентез сам по себе может быть причиной рецидивов накопления этой жидкости.
- Постановка долговременного плеврального дренажа — дренаж обеспечивает постоянный отток скапливающейся жидкости в плевральный полости. Оптимальным вариантом является установка туннелированного плеврального дренажа: до входа в плевральную полость 10–12 см трубки проводится под кожей (в «туннеле»). Это позволяет снизить риск инфицирования. Снаружи дренаж подключают к ёмкости через однонаправленный клапан. Другим вариантом долговременного дренирования может быть установка подкожной плевральной порт-системы (центрального венозного катетера, который полностью расположен под кожей) [5]. Однако туннелированные дренажи обладают преимуществом, так как более просты в установке, не требуют повторного посещения стационара и частой замены или промывания из-за закупорки фибриновыми сгустками [6]. Постановка дренажа — это безопасная и эффективная процедура, которая может проводиться даже у очень ослабленных пациентов, однако она сопряжена с постоянным чувством инородного тела в плевральной полости и риском инфицирования.

Дренаж плевры
- Плевродез — «запаивание» плевральный полости за счёт формирования спаек между висцеральной и париетальной плеврой. Процедуру проводят с помощью химических агентов (химиопрепаратов, Доксициклина, Тетрациклина, талька) или физических методов (абразии, коагуляции, аргоноплазменной коагуляции). В рамках кокрановского мета-анализа исследователи доказали, что наиболее оптимальным агентом для плевродеза является тальк [15]. Взвесь талька можно ввести в плевральную полость через дренаж или распылить сухой тальк в ходе торакоскопии [16]. Хотя клинической разницы между этими методами нет, распыление с помощью торакоскопии позволяет сразу же провести биопсию плевры и полноценный осмотр плевральной полости [9]. Плевродез является наиболее оптимальным методом лечения пациентов со злокачественным поражением плевры и рецидивирующими плевритами, так как он обеспечивает максимальную эффективность и безопасность.

Плевродез
- Плеврэктомия (частичная или полная) — проводится также, как и при первичном опухолевом поражении, но при метастатическом плеврите имеет определённые ограничения, так как обладает высоким уровнем травматизации, сопряжена с риском выраженного болевого синдрома и других осложнений в послеоперационном периоде [6].
В соответствии с современными рекомендациями Европейского респираторного и Американского торакального обществ, постановка долговременного плеврального дренажа или плевродез — основные способы лечения пациентов с метастатическим поражением плевры и симптомами дыхательной недостаточности. Окончательный выбор терапевтического метода основывается на предпочтениях пациента и клинической целесообразности [6].
Также нужно отметить, что исследования по разработке новых методов лечения продолжаются. К таким относится:
- приём противоопухолевых препаратов [17][18];
- фотодинамическая терапия — метод лечения, при котором специальные фармпрепараты накапливаются в опухолевой ткани, а лазерное излучение запускает в ней каскад реакций с выделением синглетного кислорода, избирательно уничтожающего только поражённые клетки;
- иммунохимиотерапия — метод усиливает воздействие химиолечения, повышает иммунитет и снижает устойчивость опухолевых клеток к химиотерапии;
- генная терапия — введение в клетку нормального гена, подавляющего развитие опухоли [26].
Прогноз. Профилактика
Прогноз зависит от варианта опухоли. Так, солитарная фиброзная опухоль отличается благоприятным прогнозом с достижением высоких показателей выживаемости, а злокачественная мезотелиома сопряжена с крайне плохим прогнозом: большинство пациентов умирает примерно через 9–18 месяцев после постановки диагноза [11][19].
Метастатическое поражение плевры указывает на то, что злокачественная опухоль другого органа уже достигла 4-й стадии, поэтому оно также сопряжено с неблагоприятным прогнозом: по усреднённым данным Всемирной организации здравоохранения (ВОЗ), 5-летняя выживаемость для всех видов рака не превышает 10–13 %.
Профилактика рака плевры
Чтобы избежать развития первичного опухолевого поражения плевры, в первую очередь мезотелиомы, следует избегать воздействия асбестовой пыли и радиации.
Профилактика вторичного опухолевого поражения плевры основана на профилактике развития первичных опухолей других органов, в первую очередь рака лёгких и молочной железы. Например, необходимо отказаться от курения, избегать воздействия различных канцерогенов, вовремя лечить хронические заболевания, защищаться от ионизирующего излучения и т. д. Кроме того, нужно регулярно проходить медицинские обследования, в том числе делать флюорографию или рентгенографию лёгких [26].
Список литературы
Волков Н. М., Барболина Т. Д., Борисова Т. Н. и др. Практические рекомендации по лекарственному лечению мезотелиомы плевры, брюшины и других локализаций // Злокачественные опухоли. — 2023. — № 3s2. — С. 72–88.
Пикин О. В., Рябов А. Б., Хороненко В. Э. и др. Внутриплевральная гипертермическая химиотерапия после циторедуктивных операций у больных с опухолевым поражением плевры // Онкология. Журнал им. П. А. Герцена. — 2015. — № 4. — С. 22–26.
Печетов А. А., Леднев А. Н., Данилов И. И. Гигантская солитарная фиброзная опухоль плевры. Редкое клиническое наблюдение // Онкология. Журнал им. П. А. Герцена. — 2023. — № 2. — С. 39–42.
Ефтеев Л. А., Есаков Ю. С., Блинова Е. В., Базылюк А. В., Блинов К. Д. Сравнительная характеристика методов лечения метастатического плеврита (обзор литературы) // Хирургия. Журнал им. Н. И. Пирогова. — 2024. — № 7. — С. 141–147.
Печерица Е. Д., Лукин А. А., Гнатюк Я. А., Галкин А. О. Интраплевральные порт-системы как технология контроля рецидивирующего метастатического экссудативного плеврита. Первый опыт // Уральский медицинский журнал. — 2021. — № 2. — С. 54–58.
MacRosty C., Rivera M. P. Lung Cancer. — Switzerland: Springer Nature, 2023. — Р. 211–228.
Broaddus V. C. Mechanism of pleural liquid turnover in the normal state // UpToDate. — 2024.
Litzky L. A. Pathology of malignant pleural mesothelioma // UpToDate. — 2024.
Loddenkemper R., Mathur P. N., Noppen M., Lee P. Medical thoracoscopy/pleuroscopy: manual and atlas. — Stuttgart: Thieme, 2010. — 192 р.
Husain A. N., Colby T. V., Ordonez N. G. et al. Guidelines for pathologic diagnosis of malignant mesothelioma 2017 update of the Consensus statement from the International Mesothelioma Interest Group // Arch Pathol Lab Med. — 2018. — № 1. — Р. 89–108.ссылка
Demicco E. G., Meyer C. Solitary fibrous tumor // UpToDate. — 2024.
Салимов З. М., Пикин О. В., Рябов А. Б. и др. Солитарная фиброзная опухоль плевры (клиника, диагностика, лечение) // Хирургия. Журнал им. Н. И. Пирогова. — 2020. — № 8. — С. 35–41.
Lim E., Waller D., Lau K. et al. Extended pleurectomy decortication and chemotherapy versus chemotherapy alone for pleural mesothelioma (MARS 2): a phase 3 randomised controlled trial // Lancet Respir Med. — 2024. — № 6. — Р. 457–466.ссылка
Pass H. I., Tsao A. S., Rosenzweig K. Initial management of malignant pleural mesothelioma // UpToDate. — 2024.
Dipper A., Jones H. E., Bhatnagar R. et al. Interventions for the management of malignant pleural effusions: a network meta-analysis // Cochrane Database Syst Rev. — 2020. — № 4. — Р. CD010529. ссылка
Bhatnagar R., Piotrowska H. E. G., Laskawiec-Szkonter M. et al. Effect of Thoracoscopic Talc Poudrage vs Talc Slurry via Chest Tube on Pleurodesis Failure Rate Among Patients With Malignant Pleural Effusions: A Randomized Clinical Trial // JAMA. — 2020. — № 1. — Р. 60–69. ссылка
Murthy P., Ekeke C. N., Russell K. L. et al. Making cold malignant pleural effusions hot: driving novel immunotherapies // Oncoimmunology. — 2019. — № 4. — Р. E1554969.ссылка
Ge S., Zhao Y., Liang J. et al. Immune modulation in malignant pleural effusion: from microenvironment to therapeutic implications // Cancer Cell Int. — 2024. — № 1. — Р. 105.ссылка
Sterman D. H., Litzky L. A., Kaizer L. R. Presentation, initial evaluation and prognosis of malignant pleural mesothelioma // UpToDate. — 2024.
Лазарев А. Ф. и др. Мезотелиома плевры: этиология, заболеваемость, диагностика, лечение, выживаемость // Российский онкологический журнал. — 2013. — № 5. — С. 15–20.
Яблонский П. А., Петров А. С. Злокачественная мезотелиома плевры // Практическая онкология. — 2016. — № 3. — С. 179–188.
Клименко В. Н., Иванов О. В. Опухолевые плевриты: современный взгляд на проблему // Вестник хирургии имени И. И. Грекова. — 2014. — № 2. — С. 114–117.
Carbone M., Kratzke R. A., Testa J. R. The pathogenesis of mesothelioma // Semin Oncol. — 2002. — № 1. — P. 2–17.ссылка
Чучалин А. Г. Рациональная фармакотерапия заболеваний органов дыхания: руководство для практикующих врачей. — 2-е издание, исправленное и дополненное. — М.: Литтерра, 2013. — 872 с.
Козлова Н. А., Козлов А. А. Злокачественная мезотелиома. Опыт клинических наблюдений // Вестник российских университетов. Математика. — 2013. — Т. 8.
Яблонский П. К. Национальные клинические рекомендации. Торакальная хирургия. — М.: ГЭОТАР-Медиа, 2014. — 160 с.

