Определение болезни. Причины заболевания
Бронхолёгочная дисплазия (БЛД; Bronchopulmonary dysplasia) — это хроническое заболевание, которое развивается у недоношенных детей и характеризуется повреждением ещё незрелых лёгких в результате интенсивной терапии, необходимой для выживания после преждевременных родов. Его диагностируют на 28-е сутки жизни ребёнка или 36-й неделе гестационного возраста — периода, измеряемого в неделях от первого дня последней менструации матери до момента рождения ребёнка [1][10]. Впервые это заболевание описал американский педиатр Уильям Нортвей в 1967 году [9].
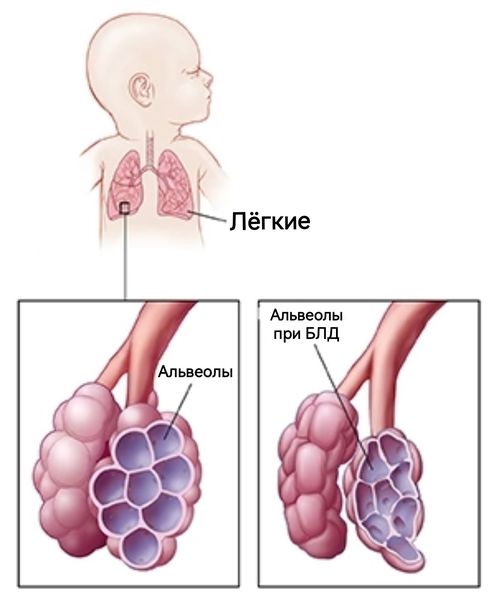
Бронхолёгочная дисплазия
Диагноз БЛД выставляют недоношенным новорождённым на основании:
- кислородозависимости;
- потребности в искусственной или вспомогательной вентиляции лёгких;
- рентген-картины, на которой видно признаки поражения интерстициальной (соединительной) ткани, которая поддерживает структуру лёгких [10].
При благоприятном течении заболевания симптомы уменьшаются, несмотря на то, что некоторые проблемы с дыханием и структурные изменения в лёгких (эмфизема, фиброз) сохраняются.
Распространённость БЛД
Данные о распространённости бронхолёгочной дисплазии разнятся в зависимости от методик исследования и выборки пациентов, используемых в различных исследованиях.
Согласно российским клиническим рекомендациям, БЛД диагностируют у 20 % недоношенных детей, родившихся раньше 30-й недели беременности с массой тела менее 1500 г. При уменьшении гестационного возраста и массы тела частота заболевания значительно возрастает: у детей, рождённых на 22–24-й неделе, вероятность развития болезни достигает 80 % [3].
Один из последних систематических обзоров включает в себя сведения из 105 статей и баз данных с января 1990 года по сентябрь 2019 года. Исследователи проанализировали историю болезни 780 936 пациентов и пришли к выводу, что риск развития БЛД у детей, рождённых на 28-й неделе, составляет 35 %, а у детей, рождённых на 36-й неделе, вероятность снижается до 21 % [2].
Факторы риска БЛД
Есть несколько видов факторов, которые способствуют развитию бронхолёгочной дисплазии. Их делят на управляемые и неуправляемые, эндогенные (внутренние) и экзогенные (внешние) [3].
Экзогенные факторы:
- внутриутробные инфекции, например уреаплазмоз (Ureaplasma urealyticum) и цитомегаловирус, которые больше других связаны с развитием БЛД [5];
- агрессивная кислородотерапия, включая искусственную вентиляцию лёгких (ИВЛ) более 3 суток при высоких параметрах FiO₂ и PIP (т. е. доля вдыхаемого кислорода превышает 50 %, а пиковое давление вдоха — 30 см вод. ст.) [3];
- недостаточность питания и дефицит витаминов в период новорождённости [1].
Неуправляемые эндогенные факторы:
- недоношенность (особенно, если гестационный возраст менее 32 недель) и экстремально низкая масса тела при рождении (менее 1000 г) [3];
- задержка внутриутробного развития и незрелость лёгочной ткани [1];
- генетическая предрасположенность [4][6];
- пол ребёнка: у мальчиков риск развития БЛД выше [3].
Управляемые факторы:
- курение матери во время беременности;
- дефицит сурфактанта — поверхностно-активного вещества, которое предотвращает спадение альвеол [13];
- сопутствующие патологии, например респираторный дистресс-синдром и лёгочное кровотечение [12].
Симптомы бронхолёгочной дисплазии
Развитие бронхолёгочной дисплазии можно заподозрить у недоношенного ребёнка, который долгое время (в течение 10–14 дней) находится на ИВЛ по поводу респираторного дистресс-синдрома, при этом его состояние значительно не улучшается [1].
Основные симптомы БЛД:
- повышение частоты дыхательных движений до 80–100 вдохов и выдохов в минуту;
- западение уступчивых мест грудной клетки при вдохе (грудной клетки, межреберья и яремной ямки);
- бледность или цианоз (синюшность) кожи;
- частые эпизоды апноэ (остановки дыхания), которые при тяжёлом течении болезни сопровождаются значительным снижением кислорода в крови [3][10][11];
- сухие и влажные хрипы [1];
- плохая прибавка в весе;
- отёки из-за задержки воды в организме.

Западение уступчивых мест грудной клетки
Также возможно развитие сердечной недостаточности с увеличением размеров сердца, печени и селезёнки [10].
Симптомы после выписки из стационара:
Патогенез бронхолёгочной дисплазии
Бронхолёгочная дисплазия развивается в результате комбинации нескольких факторов: незрелости лёгочной ткани, развития респираторного заболевания и агрессивной кислородотерапии [3].
Виды повреждений лёгких при кислородотерапии:
- баротравма — поражение лёгочной ткани развивается из-за высокого давления при ИВЛ;
- волюмотравма — перерастяжение альвеол из-за поступления слишком большого объёма воздуха;
- ателекторавма — спадение лёгочной ткани (ателектаз), из-за чего уменьшается полезная площадь, необходимая для проведения газообмена, т. е. дыхания;
- биотравма — воспалительный процесс, вызванный высвобождением цитокинов и других медиаторов воспаления («цитокиновый шторм») [3].

Ателектаз
Всё это приводит к следующим последствиям:
- эпителий дыхательных путей повреждается и его замещает фиброзная (рубцовая) ткань, которая не участвует в обмене кислорода и углекислого газа, из-за чего лёгкие не могут эффективно насыщать кровь кислородом;
- эластичность лёгочной ткани снижается и формируются «воздушные ловушки» (эмфиземы);
- лёгкие не могут осуществлять газообмен в нужном объёме, что приводит к хронической гипоксемии (снижению уровня кислорода в артериальной крови) и недостаточному поступлению питательных веществ к другим тканям и органам [1][7].

Эмфизема лёгких
Таким образом формируются порочные круги патогенеза БЛД:
- Агрессивная кислородотерапия — повреждение лёгких — воспаление — нарушение восстановления ткани — фиброз.
- Гипоксемия — нарушение питания — повышенная уязвимость тканей — углубление повреждений.

Фиброз лёгких
Все эти факторы не позволяют незрелой лёгочной ткани нормально развиться [3][7].
Классификация и стадии развития бронхолёгочной дисплазии
Классификация БЛД претерпела изменения с учётом новых диагностических подходов и методов лечения. Сейчас степень тяжести болезни устанавливают на основании типа респираторной терапии и параметров кислородной поддержки.
Типы респираторной терапии:
- кислородная палатка — специальный воздухонепроницаемый тент, который дозирует подачу кислорода; её используют при лечении малышей до 3 лет;
- оксигенотерапия через носовые (назальные) канюли — может способствовать увлажнению дыхательных путей, облегчая отхождение мокроты;
- неинвазивная искусственная вентиляция лёгких — поддерживает дыхание с помощью аппарата ИВЛ, который фильтрует воздух и подаёт его через маску;
- инвазивная искусственная вентиляция лёгких — газовую смесь подают непосредственно в лёгкие через эндотрахеальную трубку или трахеостому;
- неинвазивная вспомогательная вентиляция постоянным положительным давлением (CPAP, СИПАП-терапия) — воздух поступает под постоянным положительным давлением через специальную маску, что позволяет держать дыхательные пути открытыми, предотвращая их смыкание и возникновение пауз в дыхании;
- неинвазивная вентиляция с положительным давлением (NIPPV) — это вспомогательное средство для поддержки дыхания, которое обеспечивает два уровня давления: более высокое на вдохе и более низкое на выдохе.
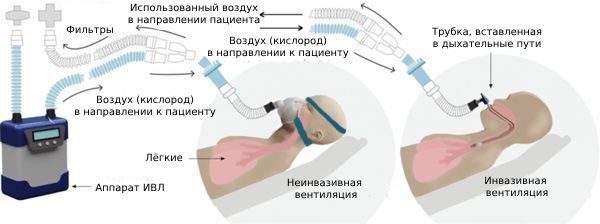
Виды ИВЛ
Классификация по степени тяжести (по Jensen, 2019 год):
- лёгкая степень — используется назальная канюля с потоком кислородной смеси менее 2 л/мин;
- средняя степень — требуется CPAP, NIPPV или оксигенотерапия через назальные канюли с потоком 2 л/мин или более;
- тяжёлая степень — необходима инвазивная ИВЛ [14].
Классификация по параметрам внешней поддержки (авторы — исследователи Национального института по проблемам детского здоровья и развития человека, 2018 год):
- Лёгкая степень:
- доля вдыхаемого кислорода (FiO₂) составляет 22–29 % при использовании кислородной палатки;
- доля вдыхаемого кислорода составляет 22–70 % при использовании назальной канюли с потоком кислородной смеси менее 1 л/мин;
- доля вдыхаемого кислорода равна 21 %, поток кислородной смеси составляет 3 л/мин и более.
- Средняя степень:
- доля вдыхаемого кислорода равна или больше 30 % при любой форме кислородной терапии;
- доля вдыхаемого кислорода равна или больше 70 % при использовании назальной канюли с потоком кислородной смеси менее 1 л/мин;
- доля вдыхаемого кислорода составляет 22–29 % при использовании CPAP, NIPPV или назальной канюли с потоком кислородной смеси 3 л/мин и более;
- доля вдыхаемого кислорода равна 21 % при использовании инвазивной ИВЛ.
- Тяжёлая степень:
- доля вдыхаемого кислорода равна или больше 30 % при использовании CPAP, NIPPV или назальной канюли с потоком кислородной смеси 3 л/мин и более;
- доля вдыхаемого кислорода больше 21 % при использовании инвазивной ИВЛ [14].
Обе эти классификации указывают на одну и ту же зависимость: чем выше степень тяжести, тем более серьёзные меры нужны по поддержке дыхания и тем тяжелее прогноз, потому что длительное использование ИВЛ и высокие параметры кислорода повышают риск развития осложнений.
Ранее в терапевтической практике также использовали классификации, основанные на морфологических (структурных) особенностях лёгких, однако сейчас они утратили актуальность.
В современной практике появилась «новая» форма БЛД, связанная с использованием сурфактантной терапии при респираторном дистресс-синдроме у недоношенных детей. Суть в том, что введение сурфактанта помогает лёгким работать лучше, из-за чего врач может назначить более мягкие параметры кислородной терапии. В этом случае изменения в лёгочной ткани становятся менее выраженными, но не исчезают полностью, поэтому также могут повлечь за собой серьёзные последствия [14].
Осложнения бронхолёгочной дисплазии
Бронхолёгочная дисплазия, особенно её тяжёлая форма, может вызвать разные краткосрочные и долгосрочные последствия.
В первую очередь страдает дыхательная система человека. К респираторным осложнениям относятся:
- хроническая дыхательная недостаточность — несмотря на адекватное лечение, у некоторых детей ещё долгое время (иногда на всю жизнь) сохраняются ограничения в работе лёгких, из-за чего им нужно регулярно осматриваться у пульмонолога и контролировать уровень кислорода;
- рецидивирующие инфекции дыхательных путей (например, пневмония или бронхиолит) — у таких пациентов, особенно у детей, инфекции развиваются быстрее и протекают тяжелее, что связано с ослаблением иммунной защиты и повреждением лёгочной ткани [5];
- бронхиальная обструкция — БЛД способствует сужению бронхов, что связано со спазмом, отёком или структурными изменениями парного органа; это состояние сопровождается эпизодами свистящего дыхания и гипоксией;
- лёгочная гипертензия — при тяжёлом течении БЛД у пациента может повышаться давление в сосудах лёгких;
- астма и астмаподобные состояния — у детей, перенёсших БЛД, значительно повышается риск развития этих заболеваний в зрелом возрасте [3][10].
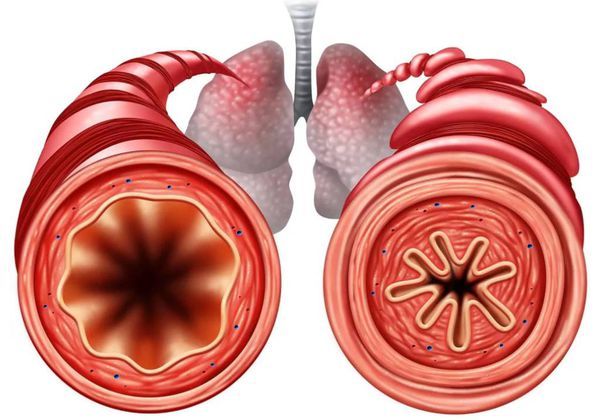
Сужение бронхов
Хроническое повреждение лёгких увеличивает нагрузку на сердце и сосуды, из-за чего может развиться сердечная недостаточность, стеноз (сужение) лёгочных вен и системная артериальная гипертензия. Всё это также вызывает гипоксемию и влияет на состояние других органов и систем организма [3][7][10].
Например, развиваются:
- неврологические осложнения: задержка психомоторного развития, судорожный синдром, нарушение мышечного тонуса (гипо- или гипертонус), повышается риск формирования других неврологических, когнитивных и поведенческих нарушений;
- пищевые и метаболические нарушения: белково-энергетическая недостаточность (из-за неё ребёнок недостаточно быстро растёт и мало прибавляет в весе), проблемы желудочно-кишечного тракта (проявляются частичными срыгиваниями, рвотой и гастроэзофагеальным рефлюксом — все эти симптомы могут усугубиться из-за длительной кислородной терапии) [1][3].
Долгосрочные последствия:
- хроническая обструктивная болезнь лёгких (ХОБЛ) — у людей, перенёсших БЛД, повышается риск развития ХОБЛ во взрослом возрасте;
- снижение физической активности — у части подростков и взрослых с БЛД в анамнезе снижается переносимость физических нагрузок [10].
Диагностика бронхолёгочной дисплазии
В клинической практике есть чёткие критерии диагностики БЛД:
- Гестационный возраст ребёнка на момент рождения составляет менее 32 недель.
- Потребность в кислородотерапии или респираторной поддержке сохраняется на 28-й день жизни, при этом для поддержания сатурации (насыщенности крови кислородом) на уровне 90–95 % дыхательная смесь должна содержать не менее 21 % кислорода.
- Рентгенологическое обследование обнаруживает признаки поражения лёгочной ткани, включая участки ателектаза (спадения ткани лёгкого), эмфиземы и интерстициального фиброза [1][3].
Инструментальная диагностика
Всем детям с подозрением на БЛД обязательно проводят рентгенографию грудной клетки и повторяют её не реже 1–2 раз в месяц (при определённых показаниях её могут делать чаще) [3].
При БЛД рентгенограмма показывает:
- гипервоздушность лёгких (увеличенные межрёберные промежутки напоминают грубую губку);
- очаговые уплотнения и нерегулярность рисунка лёгкого;
- признаки эмфиземы и ателектазов.
Эти изменения обычно наблюдают на 3–4-й неделе жизни [1][9].
Рентгенологические стадии БЛД
| Стадия | Возраст ребёнка | Рентгенологическая картина | Патологические признаки |
|---|---|---|---|
| 1 | 2–3 дня | Гранулярный лёгочный рисунок — в лёгочной ткани видны мелкие, зернистые или узелковые тени, напоминающие гранулы | Ателектазы, гиалиновые мембраны (плотные, стекловидные отложения, которые выстилают внутреннюю поверхность альвеол), расширение лимфатических сосудов |
| 2 | 4–10 дней | Просветление — на снимке лёгких появляются светлые участки, что говорит о хроническом повреждении ткани из-за длительной кислородной терапии или ИВЛ | Некроз (отмирание) и восстановление эпителия альвеол, сохраняющиеся гиалиновые мембраны |
| 3 | 10–20 дней | «Нежная губка» — лёгочная ткань выглядит как мелкоячеистая структура, напоминающая губку с тонкими, равномерными перегородками. На рентгене видны мелкие очаги просветления (воздушные полости) и тонкие фиброзные тяжи, создающие сетчатый рисунок | Слияние альвеол, ателектаз смежных альвеол, видоизменение и разрастание слизистой оболочки бронхиол |
| 4 | Свыше 30 дней | «Грубая губка» — лёгочная ткань приобретает более выраженную, крупноячеистую структуру, напоминающую губку с толстыми, неровными перегородками. На рентгене видны крупные зоны просветления (кисты или буллы) и более плотные фиброзные тяжи | Эмфизематозные альвеолы, интерстициальный фиброз, разрастание слизистой оболочки бронхов и средней оболочки артериол |
![Рентген-картина БЛД лёгкой степени [1] Рентген-картина БЛД лёгкой степени [1]](/media/bolezny/bronholyogochnaya-displaziya/rentgen-kartina-bld-lyogkoy-stepeni-1_s.jpeg)
Рентген-картина БЛД лёгкой степени [1]
Несмотря на то, что Уильям Нортвей выделил эти стадии в далёком 1967 году, врачи их используют до сих пор [9].
Также проводят:
- пульсоксиметрию — медицинский персонал постоянно проверяет уровень сатурации;
- эхокардиографию и электрокардиографию (Эхо-КГ и ЭКГ) — позволяют исключить лёгочную гипертензию и оценить состояние сердца [3][10];
- компьютерную томографию (КТ) — её проводят, чтобы исключить другие заболевания, когда выздоровление затягивается или же в случае осложнений [10];
- полисомнографию — применяют, если у ребёнка наблюдаются эпизоды апноэ [11].
Лабораторная диагностика
Чтобы оценить общее состояние ребёнка, проводят:
- анализ на газовый состав крови — показывает уровень снижения кислорода (гипоксемию), а также указывает на развитие респираторного ацидоза, при котором увеличивается концентрация углекислого газа и повышается кислотность крови;
- исследование кислотно-основного равновесия — при БЛД возможны компенсаторные изменения в виде метаболического алкалоза (защелачивания крови), из-за чего у ребёнка могут появиться судороги, головокружение и спутанность сознания;
- общий анализ крови — позволяет обнаружить анемию, повышение уровня нейтрофилов и умеренный рост эозинофилов;
- биохимический анализ крови — при БЛД возможно снижение уровня калия, натрия, общего белка и альбумина [1];
- исследование N-терминального фрагмента мозгового натрийуретического пептида (NT-proBNP) — необходимо для контроля лёгочной гипертензии [3].
Кроме того, медицинский персонал постоянно следит за дыханием, частотой сердечных сокращений и артериальным давлением ребёнка [3].
Дифференциальная диагностика
При постановке диагноза врач исключает другие болезни с похожими проявлениями:
- респираторный дистресс-синдром;
- врождённые пороки сердца (например, дефект межпредсердной перегородки);
- пневмонию и другие инфекционные заболевания;
- муковисцидоз;
- трахеобронхомаляцию и другие аномалии верхних дыхательных путей [3][10].
Таким образом, диагностика БЛД требует комплексного обследования с привлечением мультидисциплинарных специалистов, включая педиатра, пульмонолога и реаниматолога.
Лечение бронхолёгочной дисплазии
Лечение БЛД преследует несколько важных целей:
- минимизировать повреждения лёгочной ткани;
- поддерживать дыхание;
- предотвратить развитие осложнений;
- обеспечить нормальный рост и развитие ребёнка.
Терапию проводят в несколько этапов: сначала в отделении реанимации, а затем в отделении патологии новорождённых, в дальнейшем лечение продолжается дома. Срок пребывания ребёнка в стационаре зависит от тяжести его состояния и может длиться от нескольких недель до нескольких месяцев [3][5].
В первую очередь ребёнку оказывают респираторную поддержку. На начальном этапе применяют CPAP или NIPPV, которые не повреждают лёгочную ткань [3]. Однако в случае тяжёлой дыхательной недостаточности появляется необходимость использовать инвазивную ИВЛ. Аппарат ИВЛ настраивают таким образом, чтобы он подавал минимальный уровень кислорода, необходимый для поддержания сатурации на уровне 90–95 %. Такие щадящие параметры позволяют избежать повреждения лёгочной ткани избыточным кислородом, но при этом предотвращают развитие гипоксии [5]. Также у аппарата ИВЛ есть два режима вентиляции: SIMV или PSV.
В режиме SIMV аппарат ИВЛ синхронизируется с дыхательными попытками пациента и выполняет лишь необходимое количество вдохов в минуту по заданным параметрам (частоте дыхания, времени вдоха и т. д.). Например, если пациент не может сам вдохнуть в заданное время, аппарат делает это за него.
PSV — это режим, при котором аппарат поддерживает каждый спонтанный вдох пациента, добавляя заданное давление для облегчения дыхания, т. е. вентиляция полностью зависит от инициативы пациента, а аппарат лишь помогает ему [3][10].
Последующее «отлучение» от кислородной терапии проводят под постоянным наблюдением врача [3].
В особенно тяжёлых случаях, когда необходима длительная вентиляция, используют трахеостомию: в трахее создают отверстие и устанавливают в неё специальную трубку (трахеостомическую канюлю), подключённую к аппарату ИВЛ. Это позволяет воздуху поступать в лёгкие напрямую, минуя нос, рот и гортань [3][13].
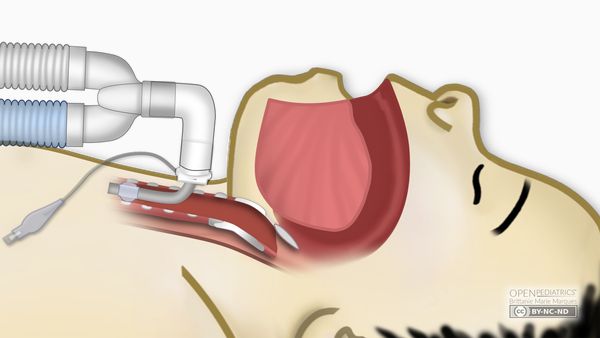
Трахеостомия
К сожалению, не во всех родильных домах и перинатальных центрах могут оказать специализированную помощь при БЛД. Полный спектр мероприятий, включая ИВЛ и сурфактантную терапию, доступны только в крупных медицинских учреждениях, отделениях реанимации и интенсивной терапии новорождённых [3][13].
Детям с БЛД также назначают медикаментозную терапию:
- Ингаляционные кортикостероиды (Будесонид) — они снижают потребность организма в кислороде, предупреждают развитие фиброзных изменений и снимают бронхообструктивный синдром. Продолжительность применения зависит от клинической картины [1][3].
- Системные кортикостероиды (Дексаметазон) — также снижают потребность организма в кислороде и улучшают газообмен. Обычно их назначают на 7–14-й день жизни самыми короткими курсами, чтобы свести к минимуму такие побочные эффекты, как инфекции или нарушение роста [1][3][13].
- Диуретики (например, Фуросемид или Верошпирон) — их используют для уменьшения отёков, в том числе в соединительной ткани лёгких, снижения лёгочной гипертензии и облегчения дыхания [1][13].
- Бронхолитики (например, Сальбутамол или Ипратропия бромид) — их применяют при наличии бронхообструкции, но только короткими курсами [3][5].
- Кофеин — введение этого препарата помогает уменьшить периодичность эпизодов остановки дыхания и потребность в ИВЛ, поэтому его используют для профилактики апноэ у детей с массой тела менее 1250 г [1][3].
Кроме того, особое внимание уделяют питанию малыша. Калорийность его рациона повышают до 140–150 ккал/кг в сутки. Если нет возможности поставлять пищу непосредственно в желудочно-кишечный тракт, используют парентеральное, т. е. внутривенное, питание. Предпочтительнее всего кормить ребёнка грудным молоком, поскольку оно способствует развитию лёгких [1][3].
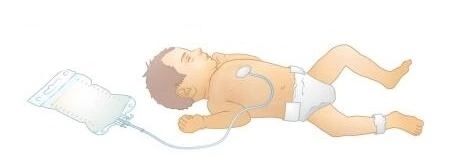
Парентеральное питание
Также медицинский персонал контролирует объём вводимой жидкости и при необходимости ограничивает его, чтобы не допустить развития отёков и перегрузки лёгких.
В отделении патологии новорождённых малышу продолжают оказывать респираторную поддержку. Ребёнка выписывают, когда:
- он перестаёт нуждаться в кислороде, а уровень сатурации остаётся выше 90 % при свободном дыхании, т. е. когда ребёнок может дышать комнатным кислородом;
- рентген-картина не меняется в худшую сторону;
- малыш начинает питаться самостоятельно, т. е. может сосать;
- отмечается положительная динамика в весе;
- нет признаков острой инфекции [10].
Тогда же решается вопрос вакцинации и профилактики респираторно-синцитиального вируса с помощью введения Паливизумаба. Иммунизацию от пневмококка и гриппа обычно проводят в стационаре, где ребёнок должен находиться от 48 до 72 часов после вакцинации [10].
Лечение на дому
В тяжёлых случаях ребёнок может перейти в статус паллиативного пациента, требующего длительной инвазивной вентиляции лёгких, которую проводят дома с помощью портативного аппарата ИВЛ. Это позволяет минимизировать стресс, связанный с длительным пребыванием в стационаре, и обеспечить более комфортные условия [1]. При этом родители или опекуны должны регулярно контролировать параметры дыхания и уровень сатурации с помощью пульсоксиметра.
В некоторых случаях ребёнок также продолжает лечиться медикаментами:
- ингаляционными кортикостероидами, чтобы не допустить обострения бронхообструкции [5];
- бронхолитиками в случае эпизодов бронхообструкции по рекомендациям врача;
- диуретиками при наличии отёков и признаков сердечно-лёгочной недостаточности [1].
Кроме того, родителям или опекунам дают общие рекомендации по питанию и питьевому режиму малыша. Очень важно обеспечить ему высококалорийное питание, которое будет включать все необходимые макро- и микроэлементы, также необходимо регулярно контролировать динамику массы тела и роста ребёнка.
Реабилитация
До трёх лет все дети, перенёсшие БЛД, должны наблюдаться в стационаре каждые полгода-год, где они проходят различные реабилитационные мероприятия. Осмотры у педиатра и пульмонолога проводят не реже 2–3 раз в год. Также необходимо наблюдение у кардиолога, чтобы не допустить развитие лёгочной гипертензии и сердечной недостаточности.
Если же респираторная симптоматика сохраняется (дыхательная недостаточность, эпизоды бронхиальной обструкции) и после 5 лет, ребёнку показано проведение спирографии (измерение объёма лёгких и скоростных показателей дыхания), а также консультация аллерголога-иммунолога и пульмонолога [10].
Прогноз. Профилактика
Прогноз для детей с БЛД зависит от тяжести заболевания, своевременности диагностики и уровня оказания медицинской помощи. У большинства детей с лёгкой и средней формой заболевание постепенно регрессирует к 2–3 годам, однако могут сохраняться эпизоды бронхиальной обструкции, респираторные инфекции и снижение физической активности, в то время как тяжёлая форма БЛД ассоциирована с развитием ХОБЛ в зрелом возрасте [1][3].
Современные подходы, включая респираторную поддержку, медикаментозную терапию и коррекцию питания, значительно улучшают выживаемость и качество жизни детей с БЛД. По некоторым данным, около 60–70 % детей с лёгкой или средней формой болезни в дальнейшем ведут обычный образ жизни с минимальными ограничениями в физической активности, например им может быть противопоказан профессиональный спорт. Людям с БЛД в анамнезе рекомендуется заниматься аэробными видам спорта (плаванием, ходьбой или лёгким бегом), которые благоприятно влияют на функциональные показатели дыхательной системы [1].
Согласно данным исследования, смертность от БЛД в первые три месяца жизни составляет 4,1 %, а к первому году жизни — 2,6 % [3]. Вероятность летального исхода зависит от степени тяжести болезни, а также от наличия осложнений: сердечно-сосудистой недостаточности и тяжёлых вирусных инфекций, таких как респираторно-синцитиальный вирус (РСВ) [12].
Прогностические признаки неблагоприятного прогноза:
- длительное использование высоких параметров ИВЛ;
- жёсткие параметры вентиляции или высокие концентрации кислорода;
- хроническое апноэ с брадикардией, которые часто приводят к гипоксии, что может повлиять на работу центральной нервной системы и усугубить состояние ребёнка [1][11].
Эти факторы не только затрудняют лечение, но и повышают вероятность долгосрочных последствий, таких как лёгочная гипертензия, снижение физической активности, задержка развития, судорожный синдром и т. д.
Профилактика БЛД
Чтобы не допустить развития БЛД у ребёнка, необходимо предпринимать необходимые меры ещё во время беременности. Например, при возникновении риска преждевременных родов женщине назначают кортикостероидные препараты, которые помогают продлить беременность. Это важная профилактическая мера, так как БЛД чаще всего развивается у недоношенных детей на фоне респираторного дистресс-синдрома [3].
Также важно регулярно наблюдаться у врачей, чтобы своевременно выявить и начать лечение гестационной гипертензии и других осложнений беременности [10][12].
Если ребёнок всё же родился раньше срока, проводят:
- сурфактантную терапию — сурфактант помогает снизить риск повреждения лёгких; его вводят в первые 20 минут жизни всем детям, родившимся на 26-й неделе, а также малышам, рождённым с 27-й по 30-ю неделю, если им требуется интубация трахеи [12][13];
- введение Кофеина — этот препарат обязательно вводят новорождённым с низкой массой тела (менее 1250 г), чтобы предотвратить развитие апноэ [10];
- контроль кислородотерапии — важно поддерживать минимальные параметры респираторной поддержки, чтобы не допустить повреждения лёгочной ткани;
- вакцинацию — против пневмококка, гриппа и других инфекций, а также вводят Паливизумаб, который не допускает развитие РСВ, особенно опасного для детей с БЛД [3].
Также важное значение имеет питание: грудное молоко более предпочтительно, чем искусственные смеси, так как оно способствует развитию тканей лёгких и лучше удовлетворяет потребности ребёнка.
Особое внимание необходимо уделять социальной поддержке семей, столкнувшихся с этой болезнью. Важно обучить родителей или опекунов уходу за детьми: как правильно оказывать первую помощь и работать с респираторными средствами. Так как все члены семьи в такой ситуации испытывают сильный стресс, необходимо обеспечивать им психоэмоциональную поддержку, например, с помощью консультаций психолога. Это обезопасит их от выгорания.
Список литературы
Ашерова И. К., Бабак О. А., Богданова А. В., Бокерия Е. Л. и др. Бронхолёгочная дисплазия: монография. — М., 2020. — 175 с.
Moreira A., Noronha M., Joy J., Bierwirth N. et al. Rates of bronchopulmonary dysplasia in very low birth weight neonates: a systematic review and meta-analysis // Respir Res. — 2024. — № 1. — Р. 219.ссылка
Ассоциация «Здоровье детей». Бронхолёгочная дисплазия: клинические рекомендации. — М., 2024. — 97 с.
Бондарь В. А., Давыдова И. В., Басаргина М. А., Фисенко А. П. и др. Роль генетических предикторов в доклинической диагностике бронхолёгочной дисплазии // Кремлевская медицина. Клинический вестник. — 2022. — № 1. — С. 5–9.
Устинович А. А., Устинович Ю. А. Бронхолёгочная дисплазия у новорождённых и детей раннего возраста: учебно-методическое пособие. — Минск: БГМУ, 2003. — 18 с.
Lal C. V., Bhandari V., Ambalavanan N. Genomics, microbiomics, proteomics, and metabolomics in bronchopulmonary dysplasia // Semin Perinatol. — 2018. — № 7. — Р. 425–431.ссылка
Овсянников Д. Ю., Кравчук Д. А., Николаева Д. Ю. Клиническая патофизиология органов дыхания недоношенных детей // Неонатология: новости, мнения, обучение. — 2018. — № 3. — С. 74–98.
Jobe A. H., Bancalari E. Bronchopulmonary dysplasia // Am J Respir Crit Care Med. — 2001. — № 7. — P. 1723–1729.ссылка
Northway W. H. Jr., Rosan R. C., Porter D. Y. Pulmonary disease following respiratory therapy of hyaline membrane disease // N Engl J Med. — 1967. — № 7. — Р. 357–368. ссылка
Союз педиатров России. Ведение детей с бронхолёгочной дисплазией: федеральные клинические рекомендации. — М.: Педиатр, 2014. — 31 с.
Петрова Н. А., Добродеева И. В., Шабалов Н. П. и др. Апноэ у новорождённых и детей раннего возраста с бронхолёгочной дисплазией разной степени тяжести // Артериальная гипертензия. — 2013. — № 4. — С. 348–355.
Российская ассоциация специалистов перинатальной медицины. Ведение новорождённых с респираторным дистресс-синдромом: клинические рекомендации. — М., 2016. — 48 с.
Виноградова И. В., Виноградов Д. А., Емельянова В. С. и др. Профилактика бронхолёгочной дисплазии у новорождённых с низкой и экстремально низкой массой тела при рождении путём «позднего» введения сурфактанта // Российский вестник перинатологии и педиатрии. — 2015. — № 5. — С. 55–60.
Kurihara C., Zhang L., Mikhael M. Newer bronchopulmonary dysplasia definitions and prediction of health economics impacts in very preterm infants // Pediatr Pulmonol. — 2021. — № 2. — Р. 409–417.ссылка
Thébaud B., Goss K. N., Laughon M. et al. Bronchopulmonary dysplasia // Nat Rev Dis Primers. — 2019. — № 1. — Р. 78. ссылка

