Определение болезни. Причины заболевания
Аденокарцинома лёгкого (Lung adenocarcinoma) — это подтип рака лёгкого, который развивается из клеток железистого эпителия, выстилающих слизистую бронхов.

Аденокарцинома лёгкого
Распространённость рака всё ещё растёт. В 2020 году в мире зарегистрировали 2,2 млн человек с таким диагнозом. При этом рак лёгкого является абсолютным лидером по смертности. По данным ВОЗ, ежегодно он уносит почти 2 млн жизней [1].
В XIX–XX веках, когда курение табака было более распространено, чаще всего встречался плоскоклеточный вариант рака лёгких, особенно у мужчин. По мере просвещения населения, активной антитабачной позиции государств и организаций здравоохранения ситуация изменилась. Теперь самым распространённым видом рака лёгкого является аденокарцинома. На её долю приходится около 40 % случаев всех видов рака лёгкого: у курящих людей аденокарционму находят в 65 % случаев, у некурящих — в 93 % [2][19].
Причины развития аденокарциномы лёгкого
Ведущей причиной рака лёгкого, в том числе аденокарциномы остаётся курение. Однако он развивается и у некурящих людей. Например, в Азии более 30 % пациентов с раком лёгких никогда не курили [20][22]. Почему так происходит, до конца неизвестно, но есть некоторые факторы, повышающие риск возникновения онкологического заболевания: плохая экология, облучение, хронические заболевания лёгких, контакт с асбестом, постоянное воздействие с дымом огня или костра и т. д.
Большую роль также играет наследственность. Если у родителей до 50 лет диагностировали рак, у детей также повышается риск развития болезни [3].
Симптомы аденокарциномы лёгкого
Разницы в симптомах между аденокарциномой и другими видами рака лёгких нет, поэтому определить подтип опухоли можно только при патоморфологическом исследовании (изучении структуры её ткани).
Симптомы на ранних стадиях зачастую отсутствуют, но могут возникнуть, если опухоль расположена в главных бронхах. В остальных случаях симптомы появляются при больших размерах опухоли, метастазировании в лимфоузлы или другие органы [4].

Строение лёгких
К основным симптомам относятся:
- кашель, который не проходит на фоне лечения более 2–4 недель;
- выраженная общая слабость;
- кровохарканье (при прорастании опухоли в крупный бронх);
- боли в грудной клетке, не связанные с травмой и положением тела (при попадании раковых клеток в париетальный (наружный) листок плевры и рёбра);
- осиплость голоса (при поражении внутригрудных лимфоузлов);
- потеря веса за короткий промежуток времени без изменения рациона питания и образа жизни;
- боли в костях;
- головные боли или острая неврологическая симптоматика (головокружение, нарушение речи, странности поведения, слабость или неспособность нормально двигать руками или ногами и т. д.).
Патогенез аденокарциномы лёгкого
Причин и путей развития рака лёгкого достаточно много, но подавляющая роль в его образовании отводится влиянию канцерогенов. Они могут попасть в организм при курении (в табачном дыме содержится более 20 канцерогенов), при вдыхании асбеста, выхлопных газов и пр. Эти вещества образуют новые соединения со структурой ДНК клеток лёгкого, т. е. возникают генетические мутации [5]. Возникновение таких соединений взаимосвязано с активацией этих канцерогенов белками — цитохромами Р450, кодируемыми семейством генов CYP, ферментами и глутатион-S-трансферазами (GSTs), цель которых вывести токсины из организма [5][6].
Если эти соединения сохраняются и вернуть структуру ДНК к исходной форме невозможно, могут появляться критические ошибки, которые необходимы для запуска преобразования клетки в злокачественную.

Развитие рака
Простыми словами: при вдыхании канцерогенов они вступают в реакцию с клетками и нарушают их нормальную жизнедеятельность, основная часть которой отводится на постоянное создание спирали ДНК.
Однако не каждая мутация вызывает рак. Часть из них никак не влияет на жизнь клеток. По некоторым данным, для возникновения онкологической (злокачественной) опухолевой клетки и дальнейшего развития заболевания необходимо от 5 до 9 мутаций в структуре ДНК клетки [7]. При этом развитие нескольких онкологических клеток не гарантирует формирование рака, если организм способен их уничтожить. Онкологическое заболевание развивается только в том случае, когда иммунитет человека не может распознать мутирующие клетки как злокачественные и не борется с ними, что приводит к росту опухоли.
Метастазирование
Когда опухоль достигает определённого размера, она вырабатывает специальные вещества, которые запускают процесс неолимфангиогенеза и неоангиогенеза — образования новых лимфатических и кровеносных сосудов, растущих возле опухоли для её питания и дальнейшего развития. Когда стенки этих сосудов прорастают, злокачественные клетки могут попадать в кровеносное русло и лимфатическую систему. Однако для этого должно сложиться несколько факторов: снижение местного иммунитета, активация и прикрепление белков, формирующих внеклеточные структуры ткани.
Если опухолевые клетки, попавшие в кровеносное русло или лимфатический проток, не погибли и сумели имплантироваться в новом месте, они могут как остаться в состоянии «сна» на уровне нескольких клеток (микрометастазы), так и получить дальнейшее развитие с образованием опухолевых новообразований (макрометастазы).
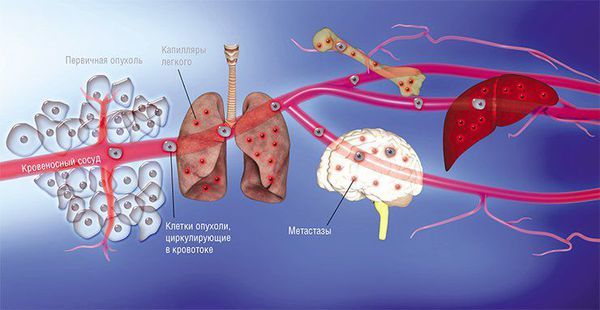
Метастазирование
Метастазы имеют сходную природу и строение, как и у первичной опухоли, поэтому системная лекарственная противоопухолевая терапия (химиотерапия) оказывает эффект на все новообразования сразу.
Классификация и стадии развития аденокарциномы лёгкого
По прорастанию аденокарцинома, как и другие формы рака лёгких, может быть:
- неинвазивной (рак in situ) — злокачественные клетки не перемещаются вглубь тканей;
- минимально инвазивной — небольшая опухоль, которая прорастает вглубь, но не больше чем на 5 мм;
- инвазивной — стелящаяся, типичная, папиллярная, микропапиллярная или солидная (уплотнённая) опухоль, которая прорастает в ткани лёгкого больше чем на 5 мм.
Стадии развития
Современное стадирование проводится согласно международным стандартам TNM [10].
T (размер новообразования):
- Тx — оценить опухоль не представляется возможным (заподозрить рак можно при обнаружении злокачественных клеток в мокроте, но при бронхоскопии новообразование не видно).
- Т0 — первичная опухоль не определяется.
- Tis — карцинома (т. е. злокачественная опухоль).
- Т1 — опухоль ≤ 30 мм, окружена лёгочной паренхимой или висцеральной плеврой, при этом новообразование не расположено в главном бронхе:
- Т1mi — минимально инвазивная аденокарцинома.
- Т2:
- опухоль размером от 31 до 50 мм;
- новообразование с вовлечением главного бронха без поражения карины (выступа стенки трахеи);
- опухоль с поражением висцеральной плевры, покрывающей лёгкое;
- новообразование с потерей объёма лёгкого или обструктивным пневмонитом; опухоль располагается в прикорневых отделах, вовлекает часть или все лёгкое.
- Т3 — опухоль от 51 до 70 мм в диаметре или прорастает в грудную стенку.
- Т4 — новообразование более 70 мм или поражает диафрагму, средостение, сердце, крупные сосуды, трахею, возвратный гортанный нерв, пищевод, тело позвонка, бифуркацию трахеи или висцеральный перикард, а также имеет метастатические узлы в других долях на стороне опухоли.
N (вовлечение близлежащих лимфатических узлов):
- Nx — невозможно дать оценку лимфоузлам.
- N0 — метастазов нет.
- N1 — метастазы в лимфоузлах, расположенных около бронхов и корня лёгкого на стороне опухоли.
- N2 — метастазы в лимфоузлах, расположенных в средостении и под трахеей.
- N3 — метастазы в лимфоузлах, расположенных средостении и у корня лёгкого на противоположной от опухоли стороне, или в надключичных лимфоузлах.
M (отдалённые метастазы):
- М0 — нет отдалённых метастазов.
- М1 — отдаленные метастазы есть:
- М1а — опухолевые узлы в лёгком на противоположной от опухоли стороне, опухолевое узелковое поражение плевры, метастатический плевральный или перикардиальный выпот (жидкость в полости перикарда);
- M1b — одиночный отдалённый опухолевый узел (т. е. расположенный вне лёгких);
- М1с — множественные внелёгочные метастазы в одном или нескольких органах.
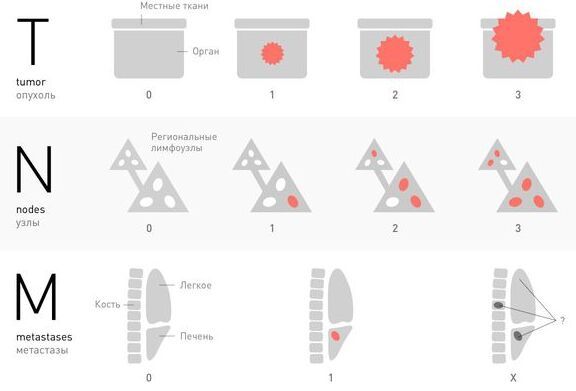
Классификация TNM
Для уточнения локализации отдалённого метастатического очага применяют дополнительную градацию:
- ADP — почки;
- BRA — головной мозг;
- HEP — печень;
- LYM — лимфатические узлы;
- MAR — костный мозг;
- OSS — кости;
- OTH — другие органы;
- PER — брюшная полость;
- PLE — плевра;
- PUL — лёгкое;
- SADP — надпочечники;
- SKI — кожа.
По результатам всех исследований и определения каждого показателя TNM, устанавливают стадию (1, 2, 3 или 4-я), которая влияет на дальнейшую терапию.
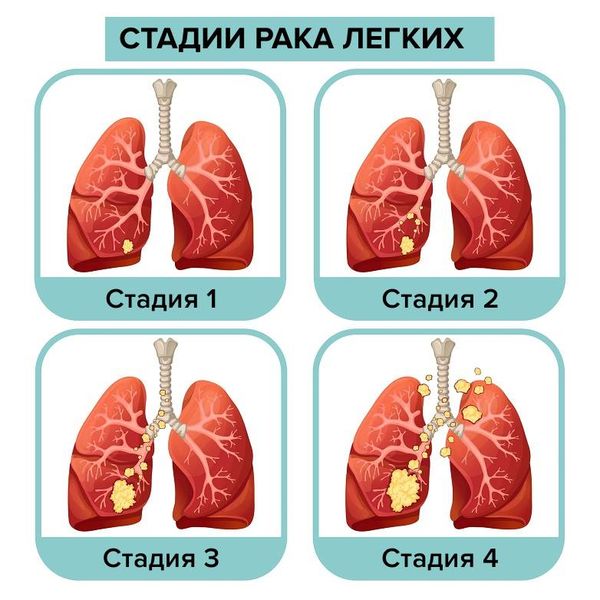
Стадии рака лёгкого
При подборе тактики лечения также оценивают уровень экспрессии белка Pd-L1 в структуре опухолевых клеток, который помогает опухоли ускользнуть от иммунного контроля. Таким образом, этот показатель отражает, насколько опухоль будет чувствительна к лечению иммунотерапией:
- менее 1 % — низкий уровень экспрессии;
- от 1 до 50 % — средний уровень экспрессии;
- более 50 % — высокий уровень экспрессии [9].
При среднем и высоком уровне ожидаемый результат лечения иммунотерапией лучше, чем при низком. Такое лечение позволяет добиться значительного успеха при борьбе с раком, но не гарантирует, что пациент точно выздоровеет.
Кроме того, важное значение имеет наличие или отсутствие активирующих драйверных мутаций, которые способствуют тому, что опухоль перестаёт реагировать на ранее успешное лечение.
Осложнения аденокарциномы лёгкого
Осложнения могут возникать как из-за первичной опухоли, так и в связи с метастазами.
Первичная опухоль может прорастать и сдавливать окружающую лёгочную паренхиму, сосуды, нервы, бронхи и даже рёбра, что в свою очередь приводит к нарушению вентиляции участка лёгкого, кровотечению, кровохарканью и боли.
Осложнения, связанные с метастазами, различны и зависят от того, где появились метастатические очаги. Например:
- поражение лимфатических узлов средостения сопровождается трудностями при глотании еды и воды, нарушением дыхания (от одышки до удушья) и стенозом (сдавлением) бронхов, которое может протекать бессимптомно, а может вызывать одышку или кровохарканье;
- поражение головного мозга — онемением и неподвижностью рук и ног, проблемами с памятью, головной болью и т. д.;
- печени — печёночной недостаточностью, сдавлением желчных протоков с развитием желтухи и т. д.
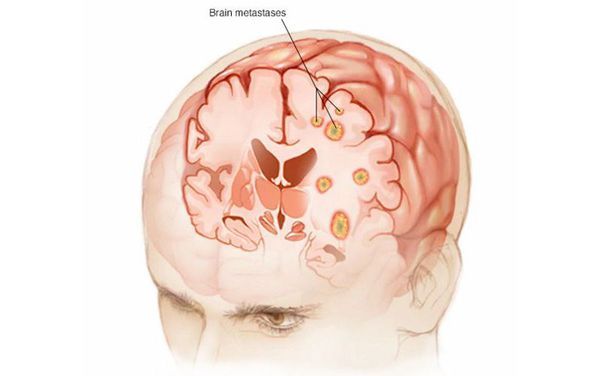
Метастазы мозга
Вариантов расположения метастазов очень много, однако чаще всего поражаются лимфоузлы, печень, головной мозг и кости [11].
Диагностика аденокарциномы лёгкого
При подозрении на онкологическое заболевание лёгкого необходимо обратиться к онкологу. Он назначит все необходимые методы, которые позволят определить расположение новообразования, стадию рака и дальнейшую тактику лечения.
Диагностика включает в себя:
- КТ или МРТ головного мозга с контрастированием — исключают метастазы;
- КТ грудной клетки, брюшной полости и малого таза с контрастированием — определяет другие заболевания, другие злокачественные новообразования в разных органах, не связанные между собой, и отдалённые метастатические очаги, если они есть;
- ПЭТ-КТ — проводят при сомнительном диагнозе или неясной картине по данным КТ того или иного участка тела;
- трахеобронхоскопию — помогает изучить трахеобронхиальное дерево и провести биопсию новообразования при его прорастании в просвет бронха;
- трепан-биопсию новообразования (при возможности выполнения и близком расположении к рёбрам) — позволяет провести гистологическое исследование и определить дальнейшую тактику лечения;
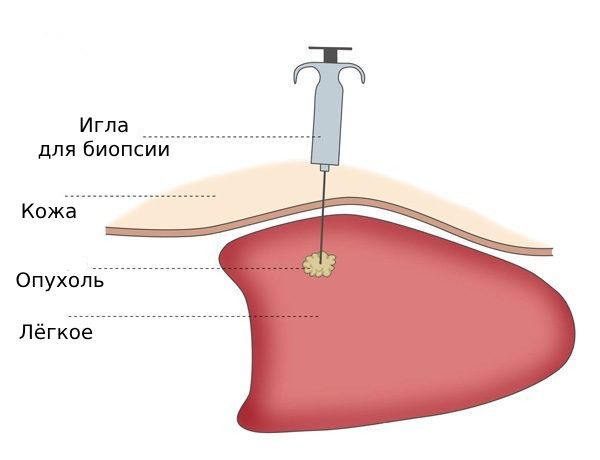
Биопсия лёгкого
- гистологическое исследование материала с проведением иммуногистохимического исследования (ИГХ) и молекулярно-генетического исследования (МГИ) — рекомендуется всем пациентам, у которых подтвердили аденокарциному лёгкого; анализы помогают определить транслокации и мутации генов, а также оценить уровень экспрессии PD-L1;
- спирометрию — оценивает объём воздуха, который человек вдыхает и выдыхает, а также скорость его прохождения по дыхательным путям; необходима для определения дальнейшей тактики лечения (например, низкий показатель спирометрии (менее 1,5 л) говорит о невозможности удаления доли лёгкого);
- анализы крови на маркеры опухоли — определение уровня NSE (нейронспецифической енолазы), растворимого фрагмента цитокератина 19 (CYFRA 21-1) и антигена плоскоклеточной карциномы (SCC) [12].
Дальнейшее дообследование зависит от выбранной тактики лечения.
Дифференциальная диагностика
Аденокарциному лёгкого важно отличить от туберкулёза, доброкачественных новообразований и паразитарных заболеваний лёгкого (например, токсоплазмоза и эхинококкоза), а также метастазов в лёгком (т. е. когда аденокарцинома лёгкого является метастазом другой опухоли)
Лечение аденокарциномы лёгкого
Лечение аденокарциномы, как и любого рака лёгкого, регламентировано отечественными клиническими рекомендациями, которые также учитывают клинические онкологические рекомендации зарубежных коллег.
Тактика лечения пациента в первую очередь зависит от стадии заболевания и функциональных возможностей организма. Учитывая, что онкологические заболевания лёгких возникают в основном у взрослых и пожилых людей, зачастую аденокарцинома сопровождается другими патологиями различной степени выраженности, которые влияют на состояние организма и, как следствие, на тактику лечения.
При отсутствии абсолютных противопоказаний врач назначает максимально радикальный метод лечения [13][14].
При 1-й стадии новообразование удаляют хирургическим способом. Обычно проводят лобэктомию (удаление доли), однако в зависимости от расположения, формы, гистологического подтипа, сопутствующей патологи и других факторов объём операции может как уменьшиться, так и увеличиться. Данный вопрос решается индивидуально.
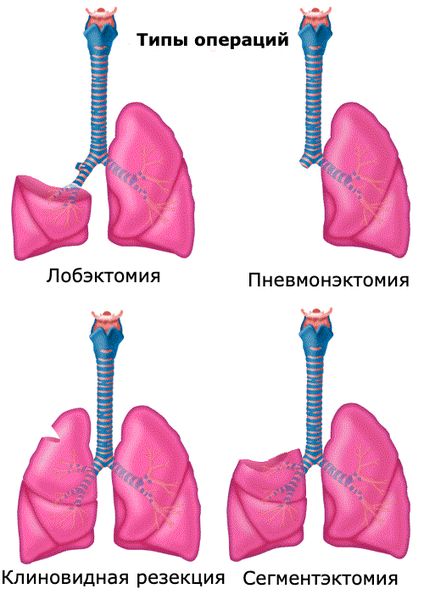
Виды операций при раке лёгкого
В случае 2-й стадии рекомендуется комплексное лечение с использованием химиотерапии и хирургического лечения. Порядок этапов врач определяет в индивидуальном порядке, но их последовательность никак не влияет на результат, т. е. комбинации «операция + химиотерапия» и «химиотерапия + операция» являются одинаково эффективными.
В последние годы также набирает популярность стереотаксическая лучевая терапия. Её проводят при начальных формах рака (1–2-й стадии). Это «концентрированный» вариант лучевой терапии с большими разовыми дозами излучения, но более коротким периодом лечения. Некоторые авторы говорят о сопоставимых результатах лучевого и хирургического методов лечения, поэтому при стереотаксической лучевой терапии операцию не проводят. Однако бóльшее количество исследований утверждают, что отдалённые результаты 5- и 10-летней выживаемости различаются в пользу пациентов, получивших радикальное хирургическое лечение.
При 3-й стадии многое зависит от поражения лимфоузлов. Если метастазы есть только на стороне опухоли, проводят комплексное лечение: предоперационную химиотерапию с последующей операцией или химиолучевой терапией (при неоперабельности опухоли или высоких рисках). Комбинаций лекарственной химиотерапии достаточно много. Это лечение бесплатно и доступно для каждого гражданина России с полисом ОМС.
Если поражены лимфоузлы с противоположной стороны грудной клетки, пациент считается неоперабельным, так как операция в этом случае неэффективна. Поэтому назначают химиотерапевтическое лечение в комплексе с лучевой терапией.
В случае 4-й стадии приоритетным и основным методом лечения является медикаментозная терапия, в том числе таргетная (т. е. направленная на сдерживание быстрого развития опухоли) и иммунотерапия. Такое лечение воздействует на опухоль и метастатические клетки сразу во всём организме. У него есть много схем и видов, их определяет врач-химиотерапевт (онколог).
Хирургическое лечение у таких пациентов не показано в абсолютном большинстве случаев, так как удаление опухоли не улучшает прогноз и выживаемость: основные симптомы и осложнения возникают в первую очередь из-за метастатических очагов и интоксикации организма. Т. е. операция не сможет существенно улучшить ситуацию, а любое хирургическое лечение сопряжено с высоким риском осложнений (в том числе фатальных).
В случаях большой распространённости опухолевого процесса и невозможности провести химиотерапию из-за высокого риска жизнеугрожающих осложнений у ослабленных пациентов отдают предпочтение паллиативному лечению. Оно не устраняет болезнь, но помогает облегчить состояние [15]. Обычно назначают один таргетный препарат. Его можно получить в ближайшем центре амбулаторной онкологической помощи (ЦАОП) и принимать дома по схеме, назначенной врачом.
Осложнения лечения
Осложнения хирургического лечения встречаются достаточно часто из-за анатомической сложности органов грудной клетки, тяжести вмешательства и наличия сопутствующей болезни, которая обостряется после операции. Наиболее опасные осложнения: длительный сброс воздуха (просачивание воздуха сквозь раны на поверхности лёгкого), кровотечение, несостоятельность культи бронха, эмпиема, нарушения ритма сердца и т. д.

Эмпиема
Наиболее частые осложнения при лучевой терапии: дерматит, пневмонит, эзофагит [16][17].
При химиотерапии чаще всего развивается: анемия, лейкопения, нейротоксичность, кардиомиопатии, токсическое поражение печени и почек и т. д. Вариативность осложнений индивидуальна, так как пациенты реагируют на препараты по-разному. Кроме того, различаются способы введения, варианты и схемы химиотерапии.
Однако почти все эти осложнения поддаются лечению, поэтому они не должны пугать пациента и становиться причиной отказа от терапии.
Прогноз. Профилактика
Точный прогноз, сколько проживёт пациент с аденокарциномой лёгкого, установить невозможно, так как каждый случай индивидуален и не всегда является стандартным. Естественно, что при 1-й стадии и вовремя проведённом лечении прогноз будет благоприятнее, чем при 3–4-й стадии. Однако встречаются случаи, когда пациенты с 1–2-й стадией погибают раньше. В этом случае причиной смерти обычно становятся выраженные сопутствующие заболевания (диабет, артериальная гипертензия, хроническая обструктивная болезнь лёгких и т. д.).
Прогноз зависит:
- от гистологического подтипа рака;
- стадии заболевания;
- возраста пациента;
- наличия определённых мутаций и транслокаций;
- доступности специализированного лечения;
- комплаентности пациента (соблюдения всех рекомендаций лечащего врача);
- наличия сопутствующей патологии, её выраженности и т. д.
В онкологии главным показателем результативности и эффективности лечения является общая и 5-летняя выживаемость.
Пятилетняя выживаемость в зависимости от стадии рака лёгкого
| Стадия | Процент выживших в течение 5 лет |
|---|---|
| 1 | 92–68 % |
| 2 | 53 % |
| 3 | 36–13 % |
| 4 | 10 % и ниже [18] |
Профилактика аденокарциномы лёгкого
Чтобы снизить риск развития болезни, следует:
- вести здоровый образ жизни;
- отказаться от вредных привычек;
- избегать места с низким качеством воздуха (жить вдали от различных производств и городов с большим количеством транспорта);
- свести к минимуму контакты с канцерогенами (стараться не работать на предприятии, где приходится часто контактировать с вредными веществами, например асбестом, а если это невозможно — соблюдать технику безопасности на производстве);
- ежегодно делать рентгенографию, а людям с повышенным риском (курильщикам, работникам вредных производств, пациентам с хроническими воспалительными заболеваниями органов дыхания) дополнительно проходить низкодозную компьютерную томографию;
- применять средства индивидуальной защиты (маски, респираторы) при работе с вредными материалами.
Список литературы
Рак // ВОЗ. — 2022.
Dias M., Linhas R., Campainha S. et al. Lung cancer in never-smokers — what are the differences? // Acta Oncol. — 2017. — № 7. — P. 931–935.ссылка
Dubin S., Griffin D. Lung Cancer in Non-Smokers // Mo Med. — 2020. — № 4. — P. 375. ссылка
Detterbeck F. C., Lewis S. Z., Diekemper R. et al. Executive Summary: Diagnosis and Management of Lung Cancer, 3rd ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines // Chest. — 2013. — № 5. — P. 7S–37S. ссылка
Белицкий Г. А. Химический канцерогенез // Российское общество клинической онкологии. — 2016. — С. 1–14.
Brambilla E., Gazdar A. Pathogenesis of lung cancer signaling pathways: roadmap for therapies // Eur Respir J. — 2009. — № 6. — P. 1485.ссылка
Имянитов И. Е., Хансон К. П. Фундаментальная онкология: наиболее примечательные события 2004 года // Практическая Онкология. — 2005. — № 1. — С. 1–5.
Pao W., Girard N. New driver mutations in non-small-cell lung cancer // Lancet Oncol. — 2011. — № 2. — P. 175–180. ссылка
Shimoji M., Shimizu S., Sato K. et al. Clinical and pathologic features of lung cancer expressing programmed cell death ligand 1 (PD-L1) // Lung Cancer. — 2016. — Vol. 98. — P. 69–75.ссылка
Proposals for the 9th edition of the TNM classification // memoinOncology. — 2023.
Kanchustambham V., Saladi S. Adenocarcinoma of the Lung With Inguinal Lymph Node Metastasis // Cureus. — 2021. — № 3. — Р. e13658.ссылка
Нефедов А. О., Костицын К. А., Гагуа К. Э. и др. Неинвазивные и инвазивные методы лечения первичной и уточняющей диагностики рака лёгкого // Вопросы онкологии. — 2020. — № 1. — С. 42–49.
Лактионов К. К., Артамонова Е. В., Бредер В. В., Горбунова В. А. и др. Практические рекомендации по лекарственному лечению немелкоклеточного рака лёгкого // Злокачественные опухоли. — 2022. — Т. 12. — С. 41–59.
NCCN Guidelines for Patients. Non-Small Cell Lung Cancer Early and Locally Advanced // NCCN. — 2022. — 70 р.
Araujo L. H. MS18.01 Treatment of Patients with Poor Performance Status (ECOG 3-4) // J Thorac Oncol. — 2018. — № 10. — P. S278–S279.
Kang K. H., Okoye C. C., Patel R. B. et al. Complications from Stereotactic Body Radiotherapy for Lung Cancer // Cancers (Basel). — 2015. — № 2. — P. 981–1004. ссылка
Zyrianov B. N., Zav’ialov A. A., Miller S. V et al. Complications of intraoperative radiotherapy and adjuvant chemotherapy in patients with lung cancer // Vopr Onkol. — 2003. — № 3. — P. 370–372.ссылка
Kay F. U., Kandathil A., Batra K. et al. Revisions to the Tumor, Node, Metastasis staging of lung cancer (8th edition): Rationale, radiologic findings and clinical implications // World J Radiol. — 2017. — № 6. — P. 269–279. ссылка
Types of Lung Cancer // LUNGevity Foundation. [Электронный ресурс]. Дата обращения: 19.07.2024.
Zhou F., Zhou C. Lung cancer in never smokers — the East Asian experience // Transl Lung Cancer Res. — 2018. — № 4. — P. 450–463. ссылка
Brenner D. R., Hung R. J., Tsao M. S. et al. Lung cancer risk in never-smokers: a population-based case-control study of epidemiologic risk factors // BMC Cancer. — 2010. — Vol. 10. — Р. 285.ссылка
Zhou W., Christiani D. C. East meets West: ethnic differences in epidemiology and clinical behaviors of lung cancer between East Asians and Caucasians // Chin J Cancer. — 2011. — № 5. — Р. 287–292.ссылка

