Определение болезни. Причины заболевания
Тромбоз глубоких вен (ТГВ) — патологическое состояние, характеризующееся образованием тромбов в глубоких венах. К последним относят крупные вены, анатомически расположенные под глубокой фасцией.
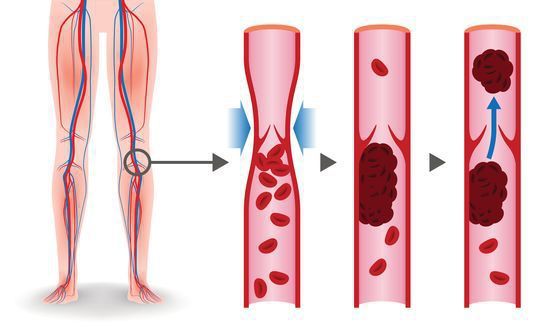
Образование тромбов в венах
Это распространённое заболевание, которое чаще всего поражает вены нижних конечностей и таза и может привести к тромбоэмболии лёгочной артерии (ТЭЛА) [1]. Учитывая, что ТГВ и ТЭЛА тесно связны друг с другом, они часто называются венозной тромбоэмболией (ВТЭ).
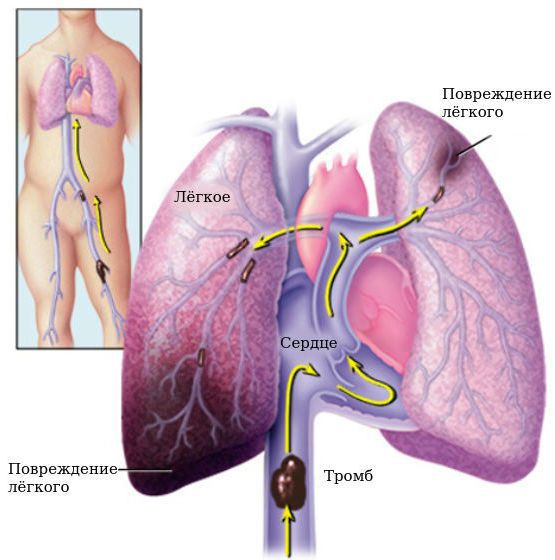
Тромбоэмболия лёгочной артерии
По данным исследований, проведённых в США, среди населения страны венозная тромбоэмболия ежегодно развивается у 375 000—425 000 больных, значительное количество случаев заболевания заканчивается смертью пациентов [1]. Тромбоз глубоких вен и тромбоэмболия лёгочной артерии в год встречаются у 1-2 человек из 1000. Существует возрастной градиент, который следует правилу 10. Согласно этому градиенту годовая заболеваемость составляет:
- 1:100 000 у детей;
- 1:10 000 в репродуктивном возрасте:
- 1:1000 в более позднем среднем возрасте;
- 1:100 в пожилом возрасте [6].
Риск развития ТГВ увеличивается с возрастом, также факторами риска являются: госпитализации, наличие активного онкологического процесса, серьёзные операции и декомпенсированные заболевания [2][3][4][5].
Наиболее заметными генетическими факторами риска развития венозного тромбоза являются дефицит природных антикоагулянтов, белка С, белка S и антитромбина. Приобретённые факторы риска могут быть связаны с заболеванием или хирургическим вмешательством. Из всех заболеваний онкология является самым сильным фактором риска: рак увеличивает риск тромбоза более чем в 50 раз [7]. Высокие риски наблюдаются во время оперативного вмешательства, в частности, в ортопедической хирургии и нейрохирургии. Важную роль в развитии тромбоза играет повышенный уровень факторов свёртывания крови. Это группа веществ в плазме крови и тромбоцитах, которые обеспечивают свёртывание крови. Самый выраженный эффект оказывает высокий уровень фактора VIII (антигемофильного глобулина).
Важно, что любой пациент, который поступает в больницу, имеет повышенный риск развития тромбоза, независимо от причины госпитализации. Многие препараты увеличивают риск тромбоза, например женские гормоны, оральные контрацептивы и заместительная постменопаузальная терапия. Комбинированные оральные контрацептивы, содержащие эстроген и прогестерон, увеличивают риск венозного тромбоза в 2-4 раза. Ещё одним фактором риска является ожирение, которое практически удваивает вероятность возникновения тромбов [8].
Частота первичного тромбоза выше у женщин, тогда как рецидивирующий тромбоз чаще встречается у мужчин [9]. Это относится к увеличению риска развития тромбоза глубоких вен, но не лёгочной эмболии [10].
Симптомы тромбоза глубоких вен
Основным диагностическим критерием тромбоза глубоких вен в большинстве случаев является отёк нижней конечности, выраженность которого зависит от уровня поражения. В случае илеофеморального тромбоза (образования тромбов в глубоких венах на уровне бедра и тазовой области) отмечается отёчность всей нижней конечности до уровня бедра, возможно с односторонним отёком половых органов и значимым болевым синдромом.
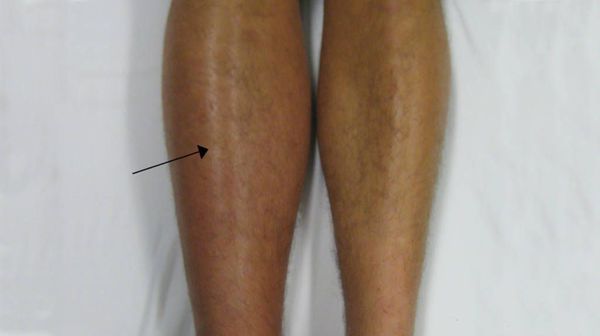
Отёк нижней конечности
Конечность меняет окраску от белого до синюшного цвета. Происходит снижение двигательной активности ввиду выраженного отёка и болевого синдрома.
ТГВ обычно начинается с уровня вен подколенной области и голени. Большинство тромбов формируется в глубоких венах ниже трифуркации (разделения артерии на три более мелкие ветви) подколенной артерии (дистальная ТГВ) [11]. Симптомы тромбоэмболии, такие как новая или усиливающаяся одышка, боль в груди или устойчивая гипотензия (низкое артериальное давление) без альтернативной причины [12], встречаются примерно у 30–40 % пациентов с ВТЭ [13].
Наиболее тяжёлая форма венозного тромбоза, когда блокированы не только основные, но и вспомогательные пути оттока, называется "синей флегмазией". Конечность при этом становится мертвенно-синего окраса, деревянной плотности, появляется отёчность, движения и чувствительность конечности снижены или отсутствуют. При этой форме, если не устранить венозную обструкцию (непроходимость), заболевание заканчивается ампутаций или смертью.
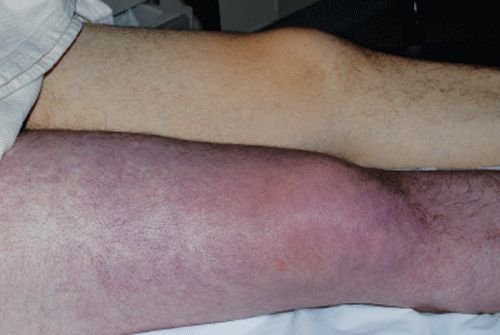
Синяя флегмазия
Симптомы тромбоза нижней полой вены: отёк и цианоз (синюшность) нижней половины туловища, обеих нижних конечностей, половых органов. Клиника выражена при полной закупорке соответствующего сегмента вены. В случаях флотирующих (плавающих) или пристеночных тромбов клинические симптомы могут соответствовать поражению бедренных или подвздошных вен.
Патогенез тромбоза глубоких вен
Немецкий врач Рудольф Вирхов описал три фактора, которые способствуют развитию ВТЭ: стаз (значимое замедление тока крови), повреждение сосудов и гиперкоагуляция (повышение свертываемости крови) [14].
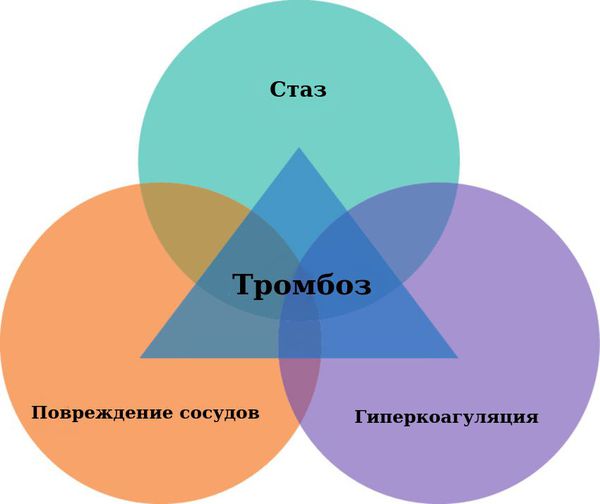
Триада Вирхова
Помимо послеоперационных и связанных с травмой случаев, стаз играет наибольшую роль в развитии венозного тромбоза [15]. Венозный тромбоз чаще начинается у венозных клапанов [16][17][18], вследствие низкого кровотока там появляются тромбы в виде небольших отложений фибрина (основной белок в формировании тромба). Точно так же послеоперационное или травматическое эндотелиальное повреждение (повреждение внутреннего слоя кровеносного сосуда) может спровоцировать этот фибриновый очаг [16][19].
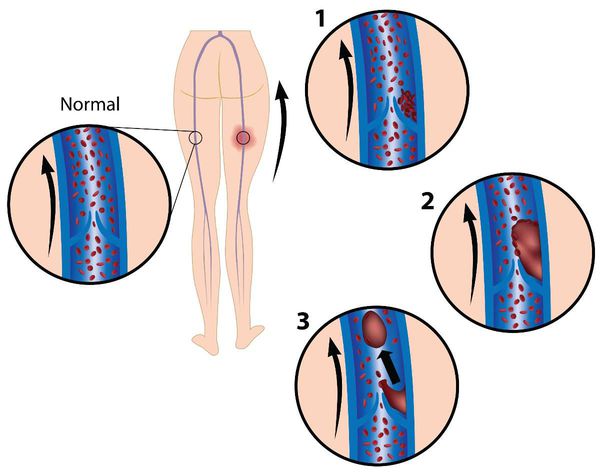
Венозный тромбоз начинается у венозных клапанов
Антитромботические белки, такие как тромбомодулин и рецептор эндотелиального белка С, синтезируются на клапанах местно, и они чувствительны к гипоксии (недостатку кислорода) и воспалению. Из-за недостатка кислорода может увеличиться концентрация прокоагулянтов, таких как тканевый фактор на эндотелии и P-селектин (молекула адгезии), которые повышают свёртывание крови, тем самым создавая условия развития тромбоза [20].
Как уже было сказано, повышенный риск образования тромбов связан с высоким уровнем факторов свёртывания крови, а именно фактора VIII, фактора фон Виллебранда, фактора VII и протромбина. Повышение их уровня наблюдается при сниженной эффективности природных антикоагулянтов (веществ, снижающих свёртывание крови), в то же время вероятность иммобилизации (обездвиживания) и инфекции становится выше[20].
Существует также "гипотеза множественного попадания". Согласно этой гипотезе, венозный стаз является основным фактором развития венозного тромбоза, однако он редко является единственной причиной образования сгустка [20].
Клинические наблюдения и эксперименты помогли понять, что для формирования значимого венозного тромбоза необходимы, по крайней мере, две из трёх составляющих триады Вирхова. Животные модели показали, что одних изменений венозного кровотока недостаточно для образования тромба [21]. Многочисленные ретроспективные обзоры пациентов с венозным тромбозом показывают, что у большинства пациентов есть несколько факторов риска [22].
Классификация и стадии развития тромбоза глубоких вен
Тромбозы глубоких вен возникают в двух основных крупных венозных системах человеческого организма.
- В системе верхней полой вены: тромбоз подключичной вены, известный как синдром Педжета – Шреттера, синдром верхней полой вены, синус-тромбозы.
- В системе нижней полой вены: суральные (икроножные) тромбозы, тромбозы берцовых вен, бедренно-подколенный, илеофеморальный тромбоз, синдром нижней полой вены.
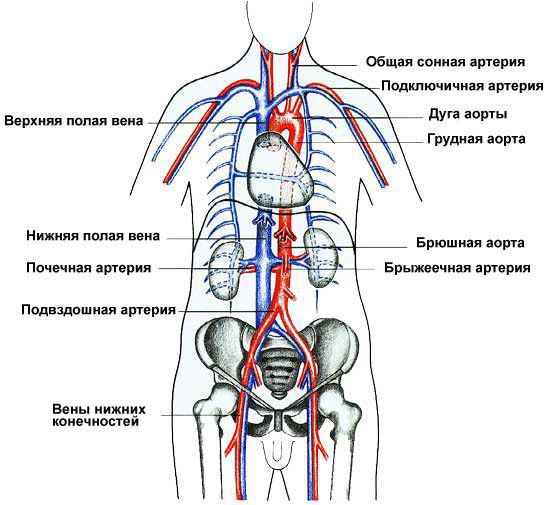
Расположение верхней и нижней полой вены
Классификация тромбоза глубоких вен по локализации:
- проксимальный (поражение бедренных, подвздошных и нижней полой вен);
- дистальный (вены голени, подколенная вена).
По степени фиксации проксимальной части тромба к венозной стенке:
- эмболоопасный (флотирующий тромб);
- неэмболоопасный (пристеночный и окклюзивный тромбы).
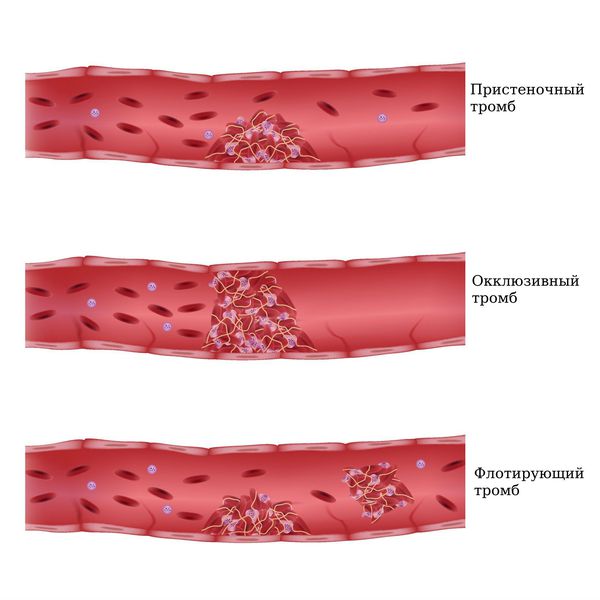
Классификация по степени фиксации проксимальной части тромба к венозной стенке
Выделяют острую, подострю и хроническую стадии ТГВ [36]. Острая стадия длится от нескольких дней до одного месяца [37] (обычно 7-14 дней), затем она переходит в подострую, а через 3 месяца начинается хроническая стадия [38].
Наибольшее признание получила классификация B.C. Савельева и соавторов (1972) [37], в которой учитываются клинические проявления в зависимости от локализации и протяжённости тромба.
По локализации:
- тромбоз магистральных вен нижних конечностей — нижний сегмент;
- тромбоз наружной и общей подвздошных вен — средний сегмент;
- тромбоз нижней полой вены — верхний сегмент.
По этиологическому фактору:
- первичный ТГВ;
- врождённый ТГВ.
По клиническому течению:
- стадия компенсации (когда организм самостоятельно возмещает ущерб, нанесённый патологией);
- стадия декомпенсации (когда организм уже не может справиться с ущербом, нанесённым болезнью).
Несмотря на большое количество предлагаемых классификаций ТГВ в настоящее время нет единой, которая являлась бы универсальной и была бы удобна для практического применения.
Осложнения тромбоза глубоких вен
Клинические исходы у пациентов с тромбозом в остром периоде и тромбоэмболией сильно различаются [24]. Чтобы облегчить принятие решений в этой непредсказуемой клинической обстановке, несколько специализированных групп и обществ разработали рекомендации относительно дифференциации риска и управления эмболией.
В заявлении 2011 года Американская кардиологическая ассоциация (AHA) определила, что массивную тромбоэмболию стоит диагностировать, если у пациента имеется устойчивая нестабильная гемодинамика [24]. Пациентам со стабильной гемодинамикой, у которых есть факторы риска надвигающейся нестабильности (дисфункция правого желудочка, повышенный натрийуретический пептид мозга или некроз миокарда), ставят диагноз субмассивные тромбоэмболии. Пациенты без гемодинамической нестабильности и вышеуказанных факторов риска классифицируются как группы низкого риска. Руководство рекомендует терапевтическую антикоагуляцию для всех пациентов с тромбоэмболией и без противопоказаний.
Использование тромболитиков (препаратов, растворяющих тромбы) непосредственно не одобрено ни для одной из категорий, так как многие препараты этой группы разрушают не только фибрин, но и другие вещества крови, придающие ей определённые свойства. Однако использование тромболитиков предлагается для пациентов с массивной формой тромбоэмболии и может быть рассмотрено для пациентов с субмассивной формой тромбоэмболии с целью купирования острого состояния.
По клиническим проявлениям выделяют три варианта ТЭЛА. Каждая форма представляет опасность для здоровья.
1. Инфаркт-пневмония (тромбоэмболия распространяется по мелким ветвям лёгочной артерии) — начинает свое проявление остро возникшей одышкой, которая усиливается, когда пациент переходит в вертикальное положение. Другие признаки: кровохарканье, тахикардия, периферические боли в грудной клетке (в месте поражения лёгкого) в результате поражения плевры.

Симптомы инфаркт-пневмонии
2. Острое легочное сердце (соответствует ТЭЛА крупных ветвей лёгочной артерии) — начинается с внезапной одышки, кардиогенного шока или пониженного артериального давления, может появиться загрудинная стенокардитическая боль.
3. Немотивированная одышка (соответствует рецидивирующей тромбоэмболии мелких ветвей) — возникают эпизоды внезапной одышки, которая быстро проходит, после некоторого времени может проявиться клиника хронического лёгочного сердца. Такое течение болезни обычно характерно для пациентов, имеющих в анамнезе хронические кардиопульмональные заболевания, а развитие хронического лёгочного сердца является следствием накопления предшествующих эпизодов ТЭЛА [23].
Посттромботический синдром (ПТС) является затяжным хроническим исходом проксимального тромбоза глубоких вен, который является хроническим клиническим процессом [25][26]. От 20 до 50 % пациентов с проксимальным ТГВ будут страдать от посттромботического синдрома в течение двух лет [27]. Было высказано предположение, что ПТС обусловлен неполным восстановлением проходимости сосуда или повреждением венозных клапанов, что приводит к клапанному рефлюксу (т. е. обратному току крови) [26]. Его патофизиология не совсем понятна, но клинически ПТС проявляется в виде тяжести в ногах, усталости, болей и отёков. Тяжёлый ПТС, обнаруженный у 3 % пациентов после перенесённого ТГВ, дополнительно сопровождается венозными язвами [27].
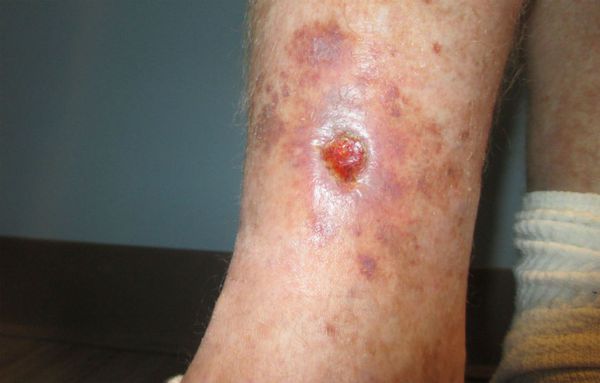
Венозная язва
Диагностика тромбоза глубоких вен
Существуют клинические симптомы ТГВ, выявляемые при обследовании больного.
- Симптом Хоманса — боли в икроножных мышцах при тыльном сгибании стопы.
- Симптом Мозеса — болезненность при сдавлении голени в передне-заднем направлении.
- Симптом Ловенберга — боли в икроножных мышцах при давлении до 80 мм рт. ст., создаваемом манжеткой сфигмоманометра (прибора для измерения артериального давления).
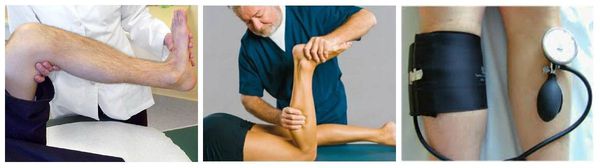
Симптом Хоманса. Симптом Мозеса. Симптом Ловенберга.
Распознавание симптомов имеет решающее значение для ранней диагностики ТГВ и ТЭЛА. Сначала необходимо оценить риск возникновения тромбоэмболии. Для этого разработано несколько систем, например шкала Уэллса или Женевы. Они представляют собой список признаков, каждому из которых соответствует определённое количество баллов. Например, по шкале Уэллса утверждению "Ранее перенесённые ТЭЛА или тромбозы глубоких вен" соответствует 1,5 балла и т. д. При значении показателя менее двух баллов вероятность ТЭЛА считается низкой, а при значении более шести баллов — высокой. При низкой, умеренной и высокой вероятности ТЭЛА по данным шкалы Уэллса частота указанного заболевания составляет около 6, 23 и 49 % соответственно.
Женевская шкала также оценивает тромбоэмболию по нескольким параметрам, среди которых возраст, пульс, кровохарканье и др.
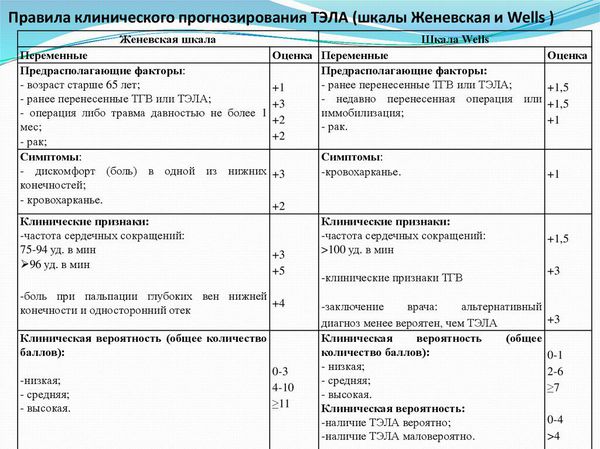
Женевская шкала и шкала Уэллса
Если по итогам клинической оценки видно, что риск лёгочной эмболии низкий, возможно применение дополнительной системы подсчета: системы критериев исключения тромбоэмболии лёгочной артерии (PERC). PERC можно быстро рассчитать без инвазивного тестирования. С помощью этой системы возможно определить, является ли вероятность лёгочной эмболии настолько низкой, что проводить дальнейшее тестирование нет необходимости. Если PERC исключает тромбоэмболию, вероятность её развития очень низкая.
Положительный результат по критериям PERC сопровождается анализом D-димера (маркера тромбообразования). Нормальный D-димер делает тромбоэмболию очень маловероятной, несмотря на высокую вероятность предварительного тестирования.
При умеренном риске развития тромбоэмболии следует применять высокочувствительный D-димер, а в случае отклонения от нормы врач должен провести КТ-ангиографию.
Высокий риск развития тромбоэмболии следует незамедлительно подтвердить с помощью КТ-ангиографии, минуя все остальные анализы. Лица с противопоказаниями к контрасту могут получить вентиляцию перфузируемых альвеол (VQ) вместо КТ-ангиографии [29].
Критерии Уэллса также широко используются для оценки вероятности тромбоза глубоких вен. Критерии Уэллса включают отёк конечностей, локальную болезненность и диагностику рака. Для пациентов с подозрением на низкий или умеренный уровень ТГВ часто проводится анализ D-димера. Нормальный D-димер у пациентов с низким или средним риском позволяет уверенно исключить ТГВ. Если D-димер является аномальным при любом уровне риска, показана дуплексная ультрасонография. Всем пациентам с высоким риском показано диагностическое ультразвуковое исследование (УЗИ) в дополнение к анализу D-димера. Положительное УЗИ для ТГВ предполагает активное лечение, тогда как отрицательное УЗИ у пациента с высоким риском требует повторного УЗИ в течение семи дней [29].
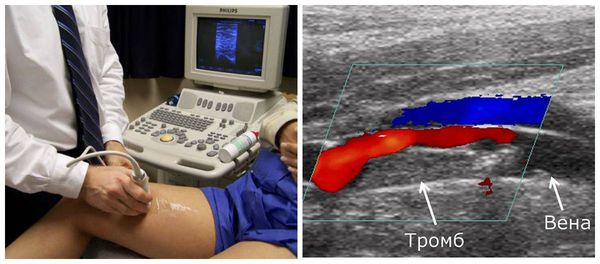
Дуплексная ультрасонография нижних конечностей
Лечение тромбоза глубоких вен
Роль кава-фильтров ("ловушек" для тромбов) нижней полой вены (НПВ) в управлении венозным тромбозом противоречива. Установка фильтра, согласно национальным рекомендациям, возможна в течение первых четырёх недель, только если существуют противопоказания к антикоагулянтной терапии, включая активное кровотечение или недавние крупные операции [29].
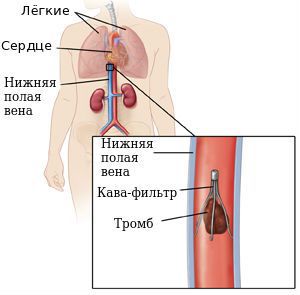
Кава-фильтр
Антикоагулянтная терапия продолжает оставаться основой терапии тромбоза НПВ. Она проводится с целью предотвращения дальнейшего формирования и роста сгустка и облегчения естественных механизмов лизиса (растворения) сгустка. Множественная дополнительная терапия в остром процессе может быть эффективной в правильных клинических условиях, включая системную фибринолитическую терапию, катетер-направленный тромболизис, фармакомеханическую тромбэктомию, аспирационную тромбэктомию, хирургическую тромбэктомию и стентирование.
Системная тромболитическая терапия показала значительные краткосрочные преимущества по сравнению с терапией антикоагулянтами, включая полный лизис сгустка крови на 45 % по сравнению с 5 % и частичный лизис на 65 % по сравнению с 20 %, а также значительное снижение частоты посттромботического синдрома. Эти преимущества, к сожалению, сопровождаются высоким риском сильного кровотечения, включая внутричерепное кровоизлияние (14 % при терапии тромболитиками против 4 % с гепарином) [30][31][32][33]. Альтернативные методы удаления тромба все чаще фиксируют эти результаты, одновременно снижая риск кровотечения. Альтернативой системному введению тромболитика является использование катетер-направленной тромболитической терапии (через прокол в вене к месту тромбоза проводится катетер, через него в сгусток вводят препарат, растворяющий тромбы). Механический тромболизис (MT) и фармакомеханический тромболизис (ФMT) также использовались для лечения илеофеморального (в глубоких венах на уровне бедра и тазовой области) тромбоза глубоких вен .
ТГВ требует динамического ультразвукового исследования для оценки проводимой антикоагулянтной терапии с оценкой обеих конечностей для исключения симультанного (сочетанного) тромбоза .
Прогноз. Профилактика
Прогноз при уже обнаруженных ТГВ и ТЭЛА зависят от выраженности процесса и общего состояния организма. Илеофеморальный тромбоз приводит к развитию посттромботической болезни, сопровождающейся развитием хронического отёка конечности и гиперпигментации. Однако при раннем выявлении тромбоза и проведении адекватной терапии клиническая симптоматика может быть минимальной.
Прогноз ТЭЛА напрямую зависит от степени её выраженности. Прогноз массивной ТЭЛА неблагоприятный и определяется врачом-реаниматологом, в остальных случаях относительно благоприятный.
Надлежащее использование профилактики ТГВ у стационарных больных важно для снижения риска посттромботических осложнений, а также фатальной и нефатальной эмболии лёгочной артерии.
Методы профилактики ТГВ включают общие меры:
- использование аспирина (место аспирина в профилактике ТГВ остается спорным);
- механическая профилактика с помощью градуированных (с неравномерным давлением) компрессионных и прерывистых пневматических компрессионных устройств.
Градуированные компрессионные чулки эффективны в снижении показателей ТГВ у пациентов общего и хирургического профиля, независимо от того, используются они отдельно или в дополнение к другой профилактике ТГВ. Механическая профилактика должна использоваться с осторожностью, если у пациента есть периферическая артериальная недостаточность (в связи с противопоказанием) [35].
Для пациентов с низким риском ТГВ важно больше двигаться, а механические методы профилактики могут обеспечить дополнительную защиту. Пациентам с более высоким риском ТГВ следует рекомендовать антикоагуляцию, основанную на рекомендациях, с антагонистами НМГ (низкомолекулярного гепарина), НФГ (нефракционированного гепарина) или витамина К, если нет чётких противопоказаний. Фондапаринукс является более новым средством, которое может обеспечить дополнительные профилактические возможности.
Список литературы
Benjamin E.J., Blaha M.J., Chiuve S.E. et al. Heart Disease and Stroke Statistics-2017 Update: A Report From the American Heart Association // Circulation. — 2017; 135(10): e146–603.ссылка
Silverstein M.D., Heit J.A., Mohr D.N., Petterson T.M., O'Fallon W.M., Melton L.J., 3rd Trends in the incidence of deep vein thrombosis and pulmonary embolism: a 25-year population-based study // Arch Intern Med. — 1998; 158(6): 585–93.ссылка
Königsbrügge O., Pabinger I., Ay C. Risk factors for venous thromboembolism in cancer: novel findings from the Vienna Cancer and Thrombosis Study (CATS) // Thromb Res. — 2014; 133(Suppl 2): S39–43.ссылка
Pannucci C.J., Shanks A., Moote M.J. et al. Identifying patients at high risk for venous thromboembolism requiring treatment after outpatient surgery // Ann Surg. — 2012; 255(6): 1093-9.ссылка
Pannucci C.J., Nackashi A. et al. Validation of the Caprini Venous Thromboembolism Risk Assessment Model in Critically Ill Surgical Patients // JAMA Surg. — 2015; 150(10): 941-8.ссылка
Naess I.A., Christiansen S.C., Romundstad P., Cannegieter S.C., Rosendaal F.R., Hammerstrøm J. Incidence and mortality of venous thrombosis: a population-based study // J Thromb Haemost. — 2007; 5: 692–9.ссылка
Blom J.W., Doggen C.J., Osanto S., Rosendaal F.R. Malignancies, prothrombotic mutations, and the risk of venous thrombosis // JAMA. — 2005; 293: 715–22ссылка
Pomp E.R., le Cessie S., Rosendaal F.R., Doggen C.J. Risk of venous thrombosis: obesity and its joint effect with oral contraceptive use and prothrombotic mutations // Br J Haematol. — 2007; 139: 289–96.ссылка
Kyrle P.A., Minar E., Bialonczyk C., Hirschl M., Weltermann A., Eichinger S. The risk of recurrent venous thromboembolism in men and women // N Engl J Med. — 2004; 350: 2558–63.ссылка
Bounameaux H., Factor V. Leiden paradox: risk of deep-vein thrombosis but not of pulmonary embolism // Lancet. — 2000; 356: 182-3.
Kearon C. Natural history of venous thromboembolism // Circulation. — 2003; 107(23, supplement 1): I22–I30.ссылка
Agnelli G., Becattini C. Acute pulmonary embolism // The New England Journal of Medicine. — 2010; 363(3): 210-274.
White R.H. The epidemiology of venous thromboembolism // Circulation. — 2003; 107 (23, supplement 1): I4-I8.ссылка
Kumar D.R., Hanlin E.R., Glurich I., Mazza J.J., Yale S.H. Virchow's contribution to the understanding of thrombosis and cellular biology // Clinical Medicine & Research. — 2010; 8(3-4): 168–172.ссылка
Mammen E.F. Pathogenesis of venous thrombosis // Chest. — 1992; 102(6): 640S-644S. ссылка
Nicolaides A.N., Kakkar V.V., Field E.S., Renney J.T. The origin of deep vein thrombosis: a venographic study // British Journal of Radiology. — 1971; 44(525): 653-663.
Aird W.C. Vascular bed-specific thrombosis // Journal of Thrombosis and Haemostasis. — 2007; 5(s1): 283–291.ссылка
Friedman S. Peripheral venous disease. In: Beers M.B., Berkow R., editors // The Merck Manual of Geriatrics. — 3rd. — New Jersey, NJ, USA: White House Station, 2000.
Stamatakis J.D., Kakkar V.V., Sagar S., Lawrence D., Nairn D., Bentley P.G. Femoral vein thrombosis and total hip replacement // British Medical Journal. — 1977; 2(6081): 223–225.ссылка
Esmon C.T. Basic mechanisms and pathogenesis of venous thrombosis. Blood Reviews. — 2009; 23(5): 225–229.ссылка
Wessler S., Reimer S.M., Sheps M.C. Biologic assay of a thrombosis-inducing activity in human serum // Journal of Applied Physiology. — 1959; 14(6): 943–946.
Cushman M., Tsai A.W., White R.H., et al. Deep vein thrombosis and pulmonary embolism in two cohorts: the longitudinal investigation of thromboembolism etiology // The American Journal of Medicine. — 2004; 117(1): 19–25.ссылка
McRae S. Pulmonary embolism // Australian Family Physician. — 2011; 39(6): 462–466.
Jaff M.R., McMurtry M.S., Archer S.L., et al. Management of massive and submassive pulmonary embolism, iliofemoral deep vein thrombosis, and chronic thromboembolic pulmonary hypertension: a scientific statement from the American Heart Association // Circulation. — 2011; 123(16): 1788–1830.ссылка
Vedantham S., Kahn S.R., Goldhaber S.Z., et al. Endovascular therapy for advanced post-thrombotic syndrome: proceedings from a multidisciplinary consensus panel // Vascular Medicine. — 2016; 21(4): 400–407.ссылка
Galanaud J.P., Kahn S.R. Postthrombotic syndrome: a 2014 update // Current Opinion in Cardiology. — 2014; 29(6): 514–519. ссылка
Kahn S.R., Shrier I., Julian J.A., et al. Determinants and time course of the postthrombotic syndrome after acute deep venous thrombosis // Annals of Internal Medicine. — 2008; 149(10): 698–707.ссылка
Ho W.K. Deep vein thrombosis risks and diagnosis // Australian Family Physician. — 2010; 39(7): 468–474.ссылка
Streiff M.B., Agnelli G., Connors J.M., et al. Guidance for the treatment of deep vein thrombosis and pulmonary embolism // Journal of Thrombosis and Thrombolysis. — 2016; 41(1): 32–67.ссылка
Arnesen H., Hoiseth A., Ly B. Streptokinase of heparin in the treatment of deep vein thrombosis. Follow-up results of a prospective study // Acta Medica Scandinavica. — 1982; 211(1-2): 65–68.ссылка
Elliot M.S., Immelman E.J., Jeffery P., et al. A comparative randomized trial of heparin versus streptokinase in the treatment of acute proximal venous thrombosis: an interim report of a prospective trial // British Journal of Surgery. — 1979; 66(12): 838–843.ссылка
Neglen P., Nazzal M.M.S., Al-Hassan H.K., Christenson J.T., Eklöf B. Surgical removal of an inferior vena cava thrombus // European Journal of Vascular Surgery. — 1992; 6(1): 78–82.ссылка
Plate G., Eklof B., Norgren L., Ohlin P., Dahlstrom J.A. Venous thrombectomy for iliofemoral vein thrombosis—10-year Results Of A Prospective Randomised Study // European Journal of Vascular and Endovascular Surgery. — 1997; 14(5):367–374.ссылка
Tooher R, Middleton P, Pham C, Fitridge R, Rowe S, Babidge W, et al. A systematic review of strategies to improve prophylaxis for venous thromboembolism in hospitals // Ann Surg — 2005; 241: 397-415.ссылка
Geerts W.H., Pineo G.F., Heit J.A., Bergqvist D., Lassen M.R., Colwell C.W., et al. Prevention of venous thromboembolism: the seventh ACCP conference on antithrombotic and thrombolytic therapy // Chest — 2004; 126(suppl 3): 338-400S.ссылка
Лидский А.Т. Важнейшие заболевания периферических сосудов. — М.: Медицинская литература,1958. — 300 с .
Савельев В.С., Думпе Э.П., Яблоков Е.Г. Болезни магистральных вен. — М., 1972. — 440 с.
Шалимов A.A., Сухарев И.И. Хирургия вен. — Киев: Здоровье,1984. 254 с.
Ho W.K. Deep vein thrombosis risks and diagnosis // Australian Family Physician. — 2010; 39(7): 468–474. ссылка

