Определение болезни. Причины заболевания
Свищ заднего прохода (прямой кишки) — это патологический ход, покрытый грануляционной тканью и соединяющий первичное отверстие внутри анального канала со вторичным отверстием на перианальной коже или промежности; вторичные ходы могут быть множественными и могут начинаться от одного и того же первичного отверстия.
Описание свищей прямой кишки уходят далеко в прошлое, еще Гиппократ, примерно в 430 г. до н. э., описывал хирургическое лечение свищей и был первым человеком, использовавшим сетон (от латинского seta — щетина).
В 1376 году английский хирург Джон Ардерн (1307-1390) написал "Трактат о свищах заднего прохода, геморрое и клизмах", где описывал фистулотомию и использование сетона.[1]
В конце 19-го и начале 20-го веков выдающиеся врачи хирурги, такие как Гудсал и Майлз, Миллиган и Морган, Томпсон и Локхарт-Маммери, внесли существенный вклад в лечение анальной фистулы. Эти врачи предложили теории патогенеза и системы классификации для анальных свищей.[2][3]
В 1976 году Паркс уточнил систему классификации, которая все еще широко используется. За последние несколько десятилетий многие авторы представили новые методы, чтобы свести к минимуму частоту рецидивов и осложнений, связанных с недержанием, но, несмотря на более чем два тысячелетия опыта, анальная фистула остается сложной хирургической проблемой.[4]
Анатомия
Понимание анатомии тазового дна и анатомии сфинктера является предпосылкой для четкого понимания системы классификации анальных свищей.
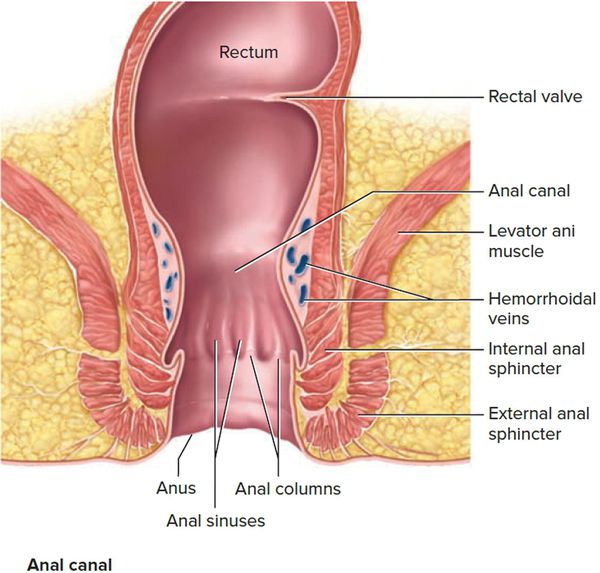
Анатомия тазового дна
Наружный сфинктер представляет собой поперечно-полосатую мышцу, подвластную произвольному контролю сознания, состоящую из трех частей: подкожной, поверхностной и глубокой.
Внутренний анальный сфинктер — гладкая мышца с автономным контролем, является продолжением циркулярного мышечного слоя стенки прямой кишки.
В большинстве случаев правило Goodsall помогает понять анатомию анального свища. Это правило гласит, что свищи с внешним отверстием перед плоскостью, проходящей поперек через центр ануса, будут соответствовать прямому переднему свищевому ходу. Свищи с их отверстиями, расположенными сзади этой линии, будут соответствовать извитому ходу к задней средней линии. Исключениями этого правила являются внешние отверстия, лежащие на расстоянии более 3 см от анального края. Они почти всегда происходят как первичный или вторичный тракт с задней средней линии, что соответствует предыдущему подковообразному абсцессу.[7][8]
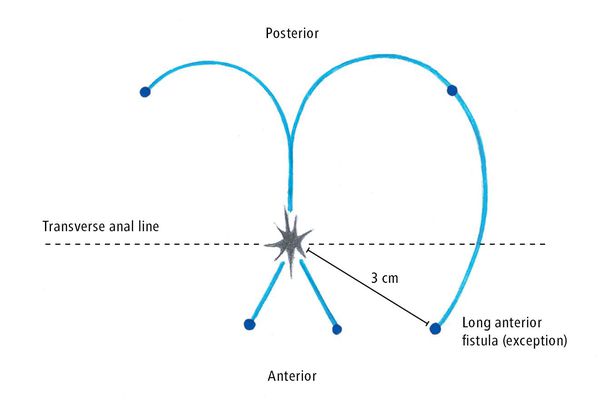
Правило Гудсэлла (Goodsall)
Истинная распространенность свищей неизвестна. Частота развития свищей после анального абсцесса колеблется от 26% до 38%.[5][12] Одно исследование показало, что распространенность свищей составляет 8,6 случая на 100 000 населения. У мужчин распространенность составляет 12,3 случая на 100 000 населения, а у женщин это 5,6 случая на 100 000 населения. Соотношение между мужчинами и женщинами составляет 1,8:1. Средний возраст пациентов составляет 38,3 года.[13]
Симптомы свища прямой кишки
При сборе анамнеза заболевания можно уточнить информацию о ранее возникавших болях, инфильтратах, уплотнениях и спонтанном или неотложном хирургическом дренировании аноректального абсцесса.
Признаки и симптомы аноректальных свищей:
- перианальные выделения;
- боль;
- припухлость;
- кровотечение;
- раздражение кожи;
- внешние свищевые отверстия.
Важные моменты в анамнезе пациента, которые помогают предположить сложный свищ:
- воспалительное заболевание кишечника;
- дивертикулит;
- предыдущая лучевая терапия при раке предстательной железы или прямой кишки;
- туберкулез;
- терапия гормонами;
- ВИЧ-инфекция.
Разнообразие симптомов и пациентов с аноректальными свищами может включать:
- боль в животе;
- потеря веса;
- изменение в работе кишечника.
Патогенез свища прямой кишки
В подавляющем большинстве случаев свищ прямой кишки является следствием аноректального абсцесса. Как правило, на уровне зубчатой линии по окружности в анальном канале расположено от 8 до 10 анальных желез. Эти железы проходят через внутренний сфинктер и заканчиваются в межсфинктерном пространстве, что в последующем обеспечивает путь распространения инфекции. Криптогландулярная гипотеза утверждает, что инфекция начинается в анальных железах и распространяется через сфинктер, вызывая аноректальный абсцесс.
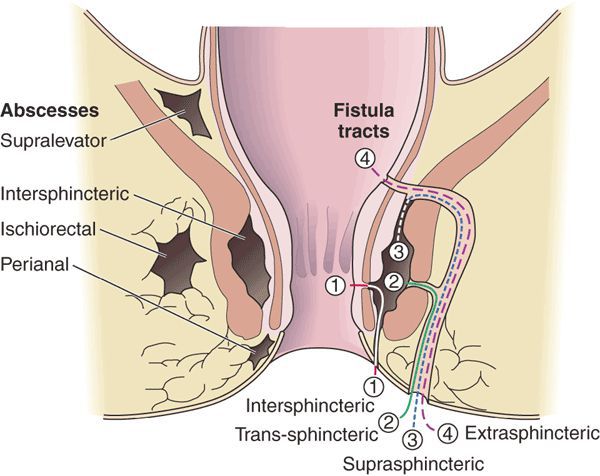
Аноректальный абсцесс
После хирургического или спонтанного дренирования на перианальной коже иногда остается свищевой ход. Образование свищевого тракта после аноректального абсцесса происходит в 7-40% случаев.[10][11]
Другие свищи развиваются вторично: после травмы (инородные тела), болезни Крона, анальных трещин, опухолей, лучевой терапии, актиномикозов, туберкулеза, венерических заболеваний.
Классификация и стадии развития свища прямой кишки
Классификация, наиболее полезная в клинической практике, по отношению свища к волокнам сфинктера (Классификация по Parks):[3]
1. интерсфинктерные (интрасфинктерные);
2. трансфинктерные;
3. супрасфинктерные;
4. экстрасфинктерные.
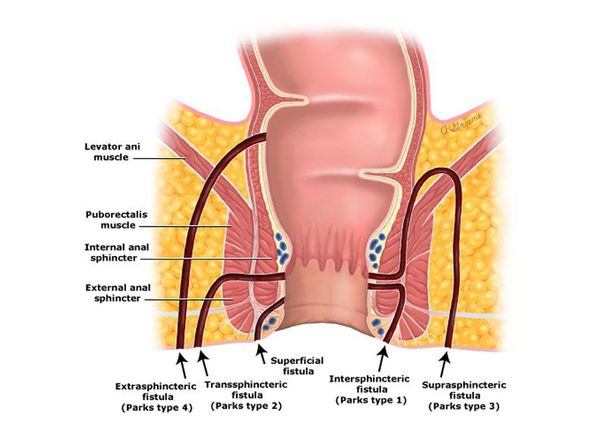
Классификация по Parks
Интерсфинктерный свищ:
- результат перианального абсцесса;
- начинается на уровне зубчатой линии, затем проходит через внутренний сфинктер в межсфинктерное пространство между внутренним и внешним анальным сфинктером и заканчивается на перианальной коже или промежности;
- заболеваемость составляет 70% всех анальных свищей;
- варианты: отсутствие наружного отверстия на промежности; высокий слепой ход; высокий ход до нижней трети прямой кишки или малого таза.
Трансфинктерный свищ:
- чаще всего возникает из-за ишиоректального абсцесса;
- начинается от внутреннего отверстия на зубчатой линии, проходит через внутренний и внешний анальные сфинктеры в ишиоректальной ямке и заканчивается на перианальной коже или промежности;
- заболеваемость составляет 25% всех анальных свищей;
- варианты: высокий свищевой ход с отверстием на промежности; высокий слепой свищевой ход.
Супрасфинктерный свищ:
- возникает из супралеваторного абсцесса;
- проходит от внутреннего отверстия на зубчатой линии до межсфинктерного пространства, отрог проходит выше пуборектальной мышцы, а затем спускается вниз к внешнему анальному сфинктеру в ишиоректальную зону и, наконец, к перианальной коже или промежности;
- заболеваемость — 5% всех анальных свищей;
- варианты: высокий слепой тракт (то есть ощущаемый через ректальную стенку выше зубчатой линии).
Экстрасфинктерный свищ:
- может быть связан: с проникновением инородного тела в прямую кишку, с дренажем через леваторы, с проникающим повреждением промежности, с болезнью Крона, опухолью или ее лечением, с тазовым воспалительным заболеванием;
- проходит от перианальной кожи через ишиоректальную ямку, продолжается вверх, через мышцы levator ani (поднимающие задний проход) к ректальной стенке, полностью вне сфинктера, с или без соединения с зубчатой линией;
- заболеваемость — 1% всех анальных свищей.
Классификация процедурных терминологических кодов (CPT, американская медицинская ассоциация)
- подкожные;
- субмышечные (интерсфинктерные, низкие трансфинктерные);
- сложные, рецидивные (высокие трансфинктерные, супрасфинктерные и экстрасфинктерные, множественные свищи, рецидивирующие);
- вторичные свищи.
Классификация, разработанная Parks et al., не включает подкожные свищи. Эти свищи не относятся к криптогландулярным, обычно возникают вследствие незаживающих анальных трещин или аноректальных процедур (например, геморроидэктомии или сфинктеротомии).
Осложнения свища прямой кишки
Ранние послеоперационные:
- задержка мочи;
- кровотечение;
- инфицирование;
- тромбоз геморроидальных узлов.
Отсроченные послеоперационные осложнения:
- рецидив;
- недержание (газов, кала);
- анальный стеноз — процесс заживления вызывает фиброз анального канала;
- медленное заживление ран.
Послеоперационные показатели рецидива и недержания (варьируют в зависимости от выполняемой процедуры):
- стандартная фистулотомия: частота рецидива составляет 0-18%, а частота недержания составляет 3-7%;
- использование сетона: частота рецидива составляет 0-17%, а частота недержания — 0-17%;
- перемещение слизистой оболочки: частота рецидива составляет 1-17%, недержание — 6-8%.
Диагностика свища прямой кишки
Осмотр
Врач должен осмотреть всю промежность, включая внешнее отверстие, которое представляет собой открытый синус или возвышение грануляционной ткани. Спонтанное выделение гноя или крови через наружное отверстие может быть видимым или появляться при пальцевом ректальном исследовании.
Пальцевое ректальное исследование может выявить свищевой ход в виде шнура под кожей, это также помогает определить острое воспаление, которое еще не купировалось. Боковое или заднее уплотнение предполагает глубокий позадианальный или ишиоректальный затек.
Врач должен определить взаимосвязь между аноректальным кольцом и расположением свищевого тракта до того, как пациент расслабится после анестезии. Тонус сфинктера и волевое усилие должны быть оценены до любого хирургического вмешательства, чтобы определить, показана ли предоперационная сфинктерометрия. Обычно для идентификации внутреннего отверстия требуется аноскопия. Большинство пациентов испытывают боль при зондировании свищевого тракта в кабинете, и этого следует избегать.
Лабораторные исследования
Никаких специальных лабораторных исследований не требуется при диагностике свищевого хода (проводятся стандартные предоперационные исследования в зависимости от возраста и сопутствующих заболеваний). Результаты локального осмотра остаются основой диагностики.
Инструментальные исследования
В рутинной практике рентгенологические методы исследования не проводятся, так как в большинстве случаев анатомию свищевого тракта можно определить в операционной. Однако такие исследования могут быть полезны, когда первичное отверстие трудно идентифицировать или когда заболевание рецидивирует. В случае рецидивных или множественных свищей такие исследования могут быть использованы для идентификации вторичных трактов или пропущенных первичных отверстий.[14]
Фистулография
Этот метод включает введение контраста через внутреннее или наружное отверстие, с последующими рентгеновскими снимками, чтобы определить ход свища.
Фистулография хорошо переносится, но может быть болезненной при введении контрастного вещества в свищевой тракт. Точность колеблется от 16% до 48%.[15]
Эндоанальная или эндоректальная ультрасонография
Эндоанальная или эндоректальная ультрасонография (УЗИ) включает в себя введение 7- или 10-МГц ультразвукового датчика в анальный канал для определения анатомии анального сфинктера и дифференцирования интерсфинктерных и трансфинктерных свищей. Добавление перекиси водорода через внешнее отверстие может помочь в определении свищевого хода, что может быть полезно при пропущенных внутренних отверстиях.
Эндоанальная/эндоректальная ультрасонография на 50% эффективнее, чем только осмотр, помогает обнаружить внутреннее отверстие, которое трудно локализовать.[16]
Магнитно-резонансная томография
Магнитно-резонансная томография (МРТ) показывает соответствие 80-90% с интраоперационными результатами. МРТ становится исследованием выбора для оценки сложных свищей и рецидивирующих свищей, что снижает частоту рецидивов, предоставляя информацию о неизвестных дополнительных ходах и полостях.[17][18]
Анальная манометрия
Проводится при планировании операции, в том числе:
- пациентам, у которых наблюдается снижение тонуса во время предоперационной оценки;
- пациентам с историей предыдущей фистулотомии;
- пациенткам с историей акушерской травмы;
- пациентам с высоким трансфинктерным или супрасфинктерным свищом;
- пожилым пациентам.
Лечение свища прямой кишки
Рассечение свища, фистулотомия
Рассечение свища (фистулотомия) используется для 85-95 % первичных свищей (подкожных, интерсфинктерных и низких трансфинктерных).
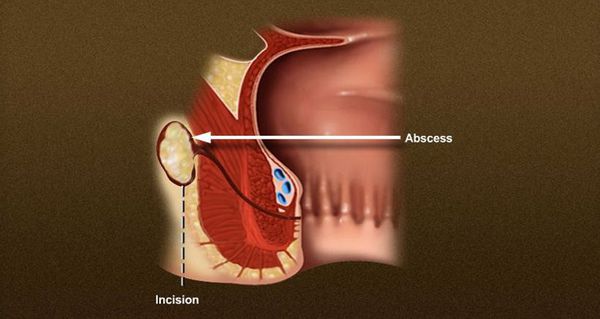
Выполняется надрез
Зонд проводится в свищевой тракт через внешнее и внутреннее отверстия. С помощью скальпеля или электрокоагулятора рассекаются кожа, подкожная клетчатка и внутренний сфинктер, таким образом открывается весь свищевой тракт.
При низком расположении свища внутренний сфинктер и подкожную часть наружного сфинктера можно разделить под прямым углом к основным волокнам. Кюретаж выполняется для удаления грануляционной ткани на дне раны. Рану оставляют открытой и не ушивают.
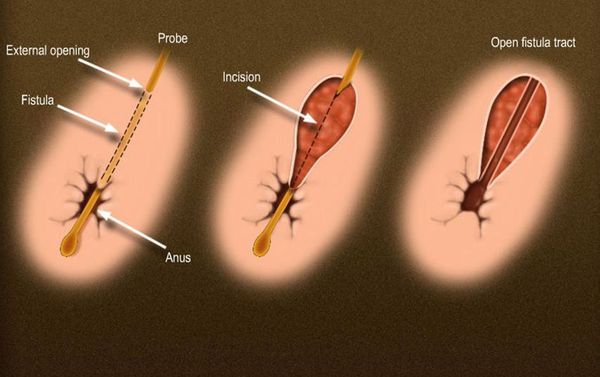
Рассечение свища
Иссечение свища (фистулэктомия) — полное удаление свищевого хода с окружающими его тканями, что оставляет раневые дефекты, требующие большего времени для заживления и не дает никаких преимуществ по сравнению с фистулотомией.
Проведение лигатуры (сетон, seton)
Сетон можно поставить отдельно, в сочетании с фистулотомией или поэтапно.
Показания:
- сложные свищи (высокие трансфинктерные, супрасфинктерные, экстрасфинктерные) или множественные свищи;
- повторные свищи после предыдущей фистулотомии;
- передние свищи у женщин;
- недостаточность анального сфинктера;
- пациенты с болезнью Крона или пациенты, страдающие иммуносупрессией.
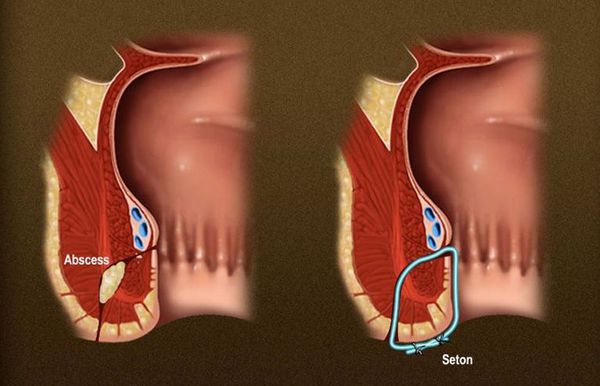
Проведение лигатуры
Помимо визуального определения количества вовлеченной мышцы сфинктера, лигатуры дренируют свищ, стимулируют фиброз и постепенно прорезают фистулу. Сетоны могут быть изготовлены из не рассасывающихся нитей или латекса.
Одномоментная техника (разрезание)
Лигатура проводится через свищевой ход и затягивается снаружи.Со временем свищевой ход постепенно прорезывается, выше лигатуры происходит фиброз. Время лечения составляет 6-8 недель.
Рецидивирование и недержание кала являются важными факторами, которые следует учитывать при использовании этого метода. Показатели успеха для режущих сетонов колеблются от 82-100%; однако долгосрочные показатели недержания могут превышать 30%.
Двухступенчатая техника (дренаж/фиброз)
Лигатура проводится вокруг глубокой части наружного сфинктера после разреза кожи, подкожной ткани, внутренней мышцы сфинктера и подкожной порции наружного сфинктера.
В отличие от режущего сетона, при данном варианте лигатура остается свободно завязанной, чтобы дренировать межсфинктерное пространство и стимулировать фиброз в глубокой части сфинктера. Как только поверхностная рана полностью заживает (через 2-3 месяца), мышца сфинктера, связанная лигатурой, разделяется.
Перемещение лоскута слизистой оболочки (FLAP-техника, Advancement Rectal Flap)
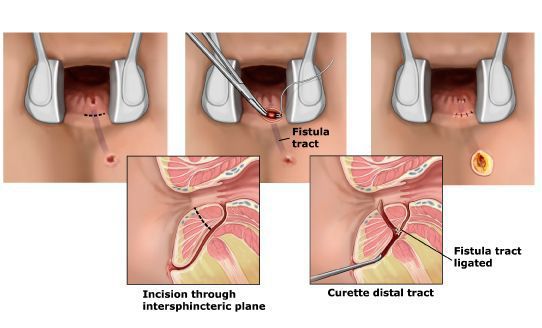
Перемещение лоскута слизистой оболочки
Перемещение слизистой оболочки показано у пациентов с хронической высокой фистулой, но показания могут быть те же, что и при проведении лигатуры.[19] Преимущества: одномоментная методика, без дополнительного повреждения сфинктера. Недостатки: малая эффективность у пациентов с болезнью Крона или острой инфекцией.
Эта процедура включает в себя полную фистулотомию с удалением первичного и вторичного трактов и полное удаление внутреннего отверстия.
Выделяется слизисто-подслизистый лоскут с широким проксимальным основанием (в два раза больше ширины вершины). Внутренний дефект мышц ушивается рассасывающимися швами, а лоскут подшивается над внутренним отверстием, так что его линия шва не перекрывает швы на сфинктере.
Штепсели и клеи ("фибриновый клей" (fibrin glue) и "коллагеновая пробка" (collagen plug)
Достижения в области биотехнологии привели к разработке новых тканевых адгезивов и биоматериалов, сформированных в виде фистулярных пробок. В связи с менее инвазивным характером эти методы лечения приводят к уменьшению послеоперационных осложнений и риска недержания, но долгосрочные результаты, особенно в сложных свищах, имеют высокую частоту рецидивов.
Зарегистрированные формы, содержащие фибриновый клей для лечения анальных свищей, имеют частоту рецидивов в течение года от 40 до 80%.
Есть данные об успешном применении более новых материалов, таких как бесклеточная дермальная матрица и биоабсорбируемая вилка Gore Bio-A, при низких свищах. Оценка долгосрочных показателей успеха с помощью технологий штепселей для комплексного заболевания будет основываться на дополнительных данных рандомизированных исследований.
В рандомизированном контролируемом исследовании, предназначенном для оценки эффективности и безопасности пробки у пациентов с перианальными свищами при болезни Крона, Senéjoux et al. не обнаружили, что штепсельная вилка превосходит сетон для закрытия свища, независимо от того, был свищ простым или сложным.
Также было предложено комбинированное сфинктерсохраняющее лечение, которое включает в себя как пробку в свищевой тракт, так и низведение лоскута прямой кишки для лечения трансфинктерных свищей.
Процедура LIFT (Ligation of Intersphincteric Fistula Tract)
Лигирование межсфинктерного свищевого тракта (LIFT) является процедурой, сохраняющей сфинктер при сложных трансфинктерных свищах, впервые описанной в 2007 году. Выполняется путем доступа к межсфинктерному пространству с целью обеспечения безопасного закрытия внутреннего отверстия и удаления пораженной криптогландулярной ткани.
Межсфинктерный ход идентифицируют и разделяют, выполняя тщательное рассечение через межсфинктерное пространство после того, как сделали небольшой разрез над зондом, соединяющим внешние и внутренние отверстия. После выделения межсфинктерный тракт лигируется вблизи внутреннего сфинктера, а затем выводится в дистальную сторону от точки лигирования. Перекись водорода вводится через внешнее отверстие, чтобы подтвердить правильное разделение свищевого хода. Проводится кюретаж оставшейся части свища. Межсфинктерный разрез ушивается рассасывающимся материалом. Рану в области наружного отверстия оставляют открытой для перевязок.
Из-за относительной новизны метод LIFT не был широко исследован. В рандомизированном исследовании участвовали 39 пациентов со сложной фистулой, у которых были неудачные предыдущие операции, и их лечили методом LIFT, показатели успеха были сопоставимы с показателями, наблюдаемыми с помощью FLAP-техники. Вероятность рецидива в течение 19 месяцев составляла 8% для метода LIFT против 7% для FLAP-техники. Время восстановления работоспособности было короче в группе LIFT (1 против 2 недель), но не было разницы в показателях недержания.
Лазерное лечение свищей (FiLaC – Fistula laser closure)
FiLaC — лечение свища прямой кишки при помощи изобретенного радиально излучающего лазерного зонда. Представляет собой новый, недостаточно изученный метод лечения хронического парапроктита с использованием специального лазерного зонда, который ликвидирует свищевой эпителий и одновременно уничтожает оставшиеся свищевые ходы. При этом аноректальный свищ удаляется мягко, без травмы сфинктера с сохранением функции анального сфинктера. Недавние исследования показали весьма обнадеживающие результаты этого нового вида лечения свищей.
Стома
В редких случаях может быть показано создание отводящей колостомы, чтобы облегчить лечение сложного рецидивирующего анального свища. Наиболее распространенные показания:
- некротизирующий фасциит промежности;
- тяжелая аноректальная болезнь Крона;
- рецидивирующие ректавагинальные свищи;
- индуцированные радиацией свищи.
Послеоперационный уход
После операции большинство пациентов могут лечиться в амбулаторных условиях, с соблюдением рекомендаций при выписке и тщательным наблюдением. Сидячие ванны, анальгетики и средства для размягчения стула (например, отруби и препараты подорожника) используются при последующем уходе.
Прогноз. Профилактика
Динамическое наблюдение колопроктолога в течение первых нескольких недель помогает обеспечить правильное лечение и заживление ран.
Важно обеспечить, чтобы внутренняя рана не закрывалась преждевременно, вызывая повторный свищ. Пальцевое обследование может помочь выявить ранний фиброз. Заживление ран обычно происходит в течение 6 недель.
Список литературы
Corman ML. Anal Fistula. Colon & Rectal Surgery. 5th ed. Philadelphia, Pa: Lippincott Williams & Wilkins; 2005. Chapter 11
Belliveau P. Anal fistula. Current Therapy in Colon and Rectal Surgery. Philadelphia: BC Decker; 1990. 22-7
Cosman BC. All's Well That Ends Well: Shakespeare's treatment of anal fistula. Dis Colon Rectum. 1998 Jul. 41(7):914-24
Phillips J, Lees N, Arnall F. Current management of fistula-in-ano. Br J Hosp Med (Lond). 2015 Mar. 76 (3):142, 144-7
Vasilevsky CA, Gordon PH. Benign Anorectal: Abscess and Fistula. Wolff BG, Fleshman JW, Beck DE, Pemberton JH, Wexner SD, eds. The ASCRS Textbook of Colon and Rectal Surgery. New York, NY: Springer; 2007. Chapter 13
Williams JG, Farrands PA, Williams AB, et al. The treatment of anal fistula: ACPGBI position statement. Colorectal Dis. 2007 Oct. 9 Suppl 4:18-50
Rosen L. Anorectal abscess-fistulae. Surg Clin North Am. 1994 Dec. 74(6):1293-308
Ross ST. Fistula in ano. Surg Clin North Am. 1988 Dec. 68(6):1417-26
Parks AG, Gordon PH, Hardcastle JD. A classification of fistula-in-ano. Br J Surg. 1976 Jan. 63(1):1-12
Hancock BD. ABC of colorectal diseases. Anal fissures and fistulas. BMJ. 1992 Apr 4. 304(6831):904-7
Hamalainen KP, Sainio AP. Incidence of fistulas after drainage of acute anorectal abscesses. Dis Colon Rectum. 1998 Nov. 41(11):1357-61; discussion 1361-2
Ramanujam PS, Prasad ML, Abcarian H. The role of seton in fistulotomy of the anus. Surg Gynecol Obstet. 1983 Nov. 157(5):419-22
Sainio P. Fistula-in-ano in a defined population. Incidence and epidemiological aspects. Ann Chir Gynaecol. 1984. 73(4):219-24
Sun MR, Smith MP, Kane RA. Current techniques in imaging of fistula in ano: three-dimensional endoanal ultrasound and magnetic resonance imaging. Semin Ultrasound CT MR. 2008 Dec. 29(6):454-71
Weisman RI, Orsay CP, Pearl RK, Abcarian H. The role of fistulography in fistula-in-ano. Report of five cases. Dis Colon Rectum. 1991 Feb. 34(2):181-4
Nevler A, Beer-Gabel M, Lebedyev A, Soffer A, Carter D, Zbar AP. Transperineal Ultrasonography (Tp-Us) In Perianal Crohn's Disease And Recurrent Cryptogenic Fistula-In-Ano. Colorectal Dis. 2013 Mar 12
Beckingham IJ, Spencer JA, Ward J, Dyke GW, Adams C, Ambrose NS. Prospective evaluation of dynamic contrast enhanced magnetic resonance imaging in the evaluation of fistula in ano. Br J Surg. 1996 Oct. 83(10):1396-8
Buchanan GN, Halligan S, Williams AB, Cohen CR, Tarroni D, Phillips RK, et al. Magnetic resonance imaging for primary fistula in ano. Br J Surg. 2003 Jul. 90(7):877-81
Seow-Choen F, Nicholls RJ. Anal fistula. Br J Surg. 1992 Mar. 79(3):197-205
Present DH, Rutgeerts P, Targan S, Hanauer SB, Mayer L, van Hogezand RA, et al. Infliximab for the treatment of fistulas in patients with Crohn's disease. N Engl J Med. 1999 May 6. 340(18):1398-405

