Определение болезни. Причины заболевания
Синдром Конигсмарка — это генетическое заболевание, которое характеризуется односторонним заращением наружного слухового прохода и маленькой, недоразвитой ушной раковиной в сочетании со снижением слуха.
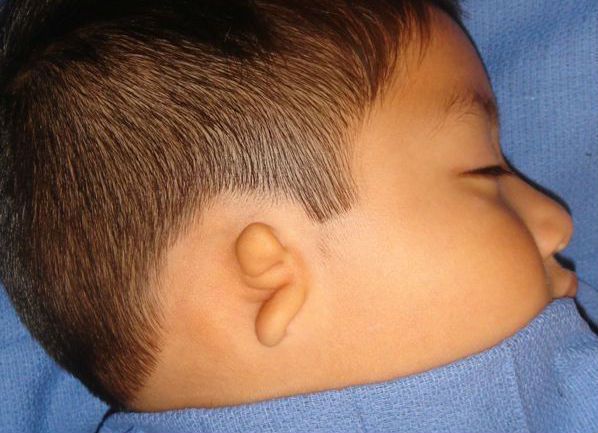
Недоразвитая ушная раковина при синдроме Конигсмарка
Согласно исследованиям российских авторов, частота встречаемости — 1 случай на 10-15 тысяч новорождённых [16]. По данным портала редких заболеваний Orphanet, основанного Французским национальным институтом здравоохранения и медицинских исследований, распространённость заболевания — около 1 случая на 1 млн новорождённых [20].
Нарушения генетического материала передаются детям от родителей. Каждый ребёнок получает гены отца и матери, иногда при этом получается сочетание, вызывающее болезни. Хромосомы условно делят на два типа: половые хромосомы, которые отвечают за формирование пола, и все остальные хромосомы (аутосомы). У человека только одна пара половых хромосом и 22 пары аутосом.
Большее количество аутосом по сравнению с половыми хромосомами обуславливает большую распространённость связанных с ними генетических нарушений. Минимальная "единица наследственности" — это ген. Существуют доминантные гены (более сильные) и рецессивные (слабые). Доминантный ген подавляет проявление рецессивного и таким образом определяет фенотипическое проявление наследуемого признака.
Синдром Конигсмарка относится к заболеваниям с аутосомно-рецессивным типом наследования. Из названия видно, что болезнь передаётся аутосомой, то есть болеть могут как девочки, так и мальчики с равной степенью вероятности. Проявляется заболевание только в том случае, если в организме ребёнка встречаются два "подавляемых" гена, которые получены и от отца, и от матери.
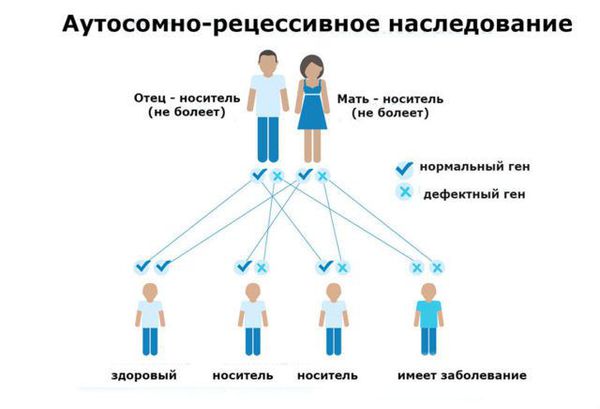
Аутосомно-рецессивный тип наследования
Если у человека только один патологический рецессивный ген, то он является носителем заболевания, следовательно, не имеет признаков патологии. Надо отметить, что именно из-за рецессивного типа наследования синдром Конигсмарка встречается достаточно редко [18].
Симптомы синдрома Конигсмарка
Главные признаки cиндрома Конигсмарка — это маленькая, недоразвитая ушная раковина (микротия), снижение слуха (кондуктивная тугоухость) и отсутствие (атрезия) наружного слухового прохода. Кондуктивная тугоухость — это снижение слуха, при котором звук не может достигнуть внутреннего уха обычным путём, то есть через наружное и среднее ухо.
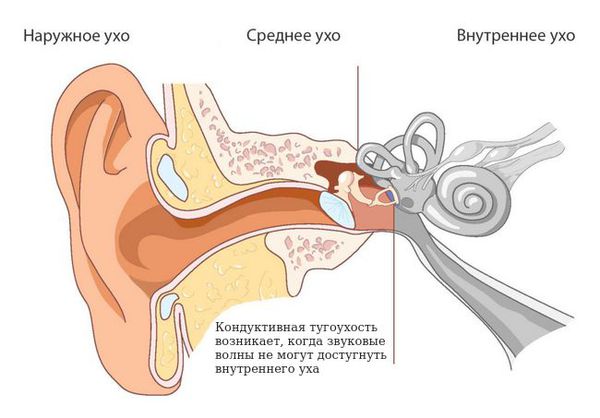
Кондуктивная тугоухость при синдроме Конигсмарка
Наружное ухо представлено небольшим кожно-хрящевым валиком, имеющим вертикальное направление, иногда — рудиментом с ярко выраженной мочкой, слуховой проход отсутствует [10]. При этом второе ухо не изменено, аномалий развития других органов нет, лицо симметрично.
Различают четыре степени микротии:
- I степень — уменьшенная ушная раковина.
- II степень — недоразвитие некоторых структур ушной раковины.
- III степень — ушная раковина представлена в виде бобовидного комочка.
- IV степень — полное отсутствие ушной раковины (анотия).
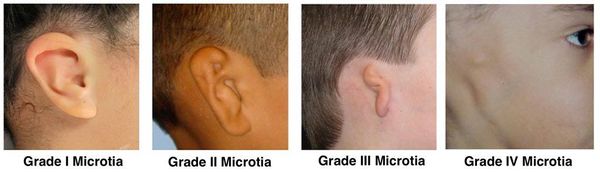
Степени микротии
Патогенез синдрома Конигсмарка
Патогенез синдрома Конигсмарка малоизучен. Поскольку заболевание является хромосомным, нарушение механизма развития наружного и среднего уха происходит в пренатальном (внутриутробном) периоде на этапе формирования структур среднего уха.
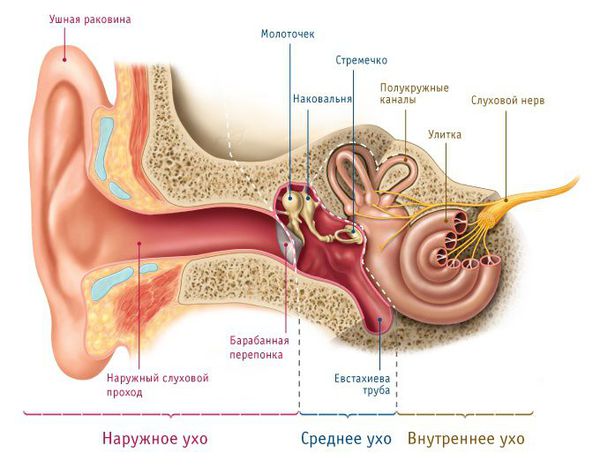
Нормальное строение уха
Ухо развивается из двух зародышевых листков:
- из эктодермального слоя формируются кожные покровы, подкожная клетчатка, хрящевая часть уха (ушная раковина), хрящевой отдел наружного слухового прохода, барабанная перепонка и все структуры улитки;
- из мезодермального — цепь слуховых косточек (молоточек, наковальня и стремечко) и височная кость.
Развитие структур наружного, среднего и внутреннего уха человека начинается с момента зачатия и заканчивается к концу беременности. На третьей неделе эмбрионального развития внутреннее ухо представлено слуховой ямкой, а среднее ухо — туботимпанальным карманом. К пятой неделе внутреннее ухо представляет собой слуховой пузырёк, а наружное ухо только начинает формироваться. С восьмой недели в среднем ухе начинают образовываться нижняя часть барабанной полости, барабанная перепонка и все её слои:
- наружный слой, который состоит из эпидермиса и является продолжением кожи наружного слухового прохода;
- средний слой, который состоит из двух слоёв фиброзных волокон (радиарных и циркулярных);
- внутренний слой, который состоит из слизистой оболочки, выстилающей барабанную полость.
В этот же период образуются слуховые косточки — пока ещё хрящевые молоточек и наковальня, которые со временем превращаются в костную ткань, а в наружном ухе формируется хрящевая часть наружного слухового прохода и ушная раковина. Таким образом, нарушение развития наружного слухового прохода и среднего уха возникает именно в период третьей-восьмой недели [14].
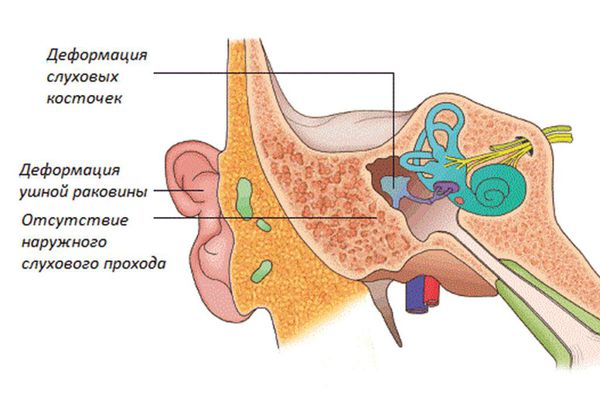
Строение уха при синдроме Конигсмарка
Классификация и стадии развития синдрома Конигсмарка
Согласно Международной классификации заболеваний 10-го пересмотра (МКБ-10), патология имеет код Q16.1 — врождённое отсутствие, атрезия и стриктура слухового прохода (наружного). Артезия или стриктура костной части канала [1].
Классификация атрезий наружного слухового прохода по Г. Ф. Шукнехту (Harold F. Schuknecht, американский оториноларинголог) [7]:
- Тип А: атрезия (заращение) хрящевой части наружного слухового прохода.
- Тип В: частичная атрезия с сужением костного и хрящевого отделов наружного слухового прохода.
- Тип С: полная атрезия наружного слухового прохода с нарушением развития всей костной системы среднего уха, отсутствие барабанной перепонки.
- Тип D: повторяет тип С, помимо этого отсутствует пневматизация (воздушность) височной кости.
Осложнения синдрома Конигсмарка
Осложнения синдрома Конигсмарка в основном связаны с психологическими аспектами. Ребёнок осознаёт, что он отличается от других в возрасте 3-3,5 лет, когда начинает активно общаться со сверстниками. Родители могут застать ребёнка у зеркала за рассматриванием своих ушей. В этом случае следует объяснить ребёнку, что он родился с одним большим ухом и одним маленьким, но когда он подрастёт, это можно будет исправить. Не нужно акцентировать внимание ребёнка на деформации. До 6-7 лет дети будут переживать по поводу микротии лишь в том случае, если родители вслух высказывают свои опасения по этому поводу.
Впервые ребёнок испытывает значительное потрясение, когда попадает в большую группу сверстников (например, в первый класс школы). В этот период у детей повышается уровень самосознания и они начинают сравнивать себя друг с другом, формируя представление о себе и своём теле. Пациент с микротией может быть подвержен издёвкам и насмешкам со стороны, тогда он начнёт осознавать, что отличается от остальных.
Вторая волна переживаний по поводу патологии начинается в подростковом возрасте. В этот период ребёнок подвергается давлению со стороны окружающих и стремится получить одобрение сверстников. Внешность становится очень значимой, каждый подросток хочет "вписаться" в окружение. Пациенты с микротией чаще замкнуты по причине своей непохожести на других и наиболее мотивированы к исправлению патологии уха. В то же время они предъявляют завышенные ожидания к исходу операции и могут быть не удовлетворены тем, что достигнуто хирургическим путём [16].
Если заболевание не лечить, при условии сохранности слуха на противоположной стороне никаких осложнений со здоровьем не будет. Но если слух на здоровой стороне снижается (например, из-за травмы, хронических отитов и др.) качество жизни пациента может значительно пострадать. Если эти процессы происходят в период формирования речи у ребёнка, возможно нарушение речевого развития.
Диагностика синдрома Конигсмарка
Диагностика синдрома Конигсмарка основывается на типичной клинической картине, исследовании слуха, данных медико-генетического консультирования с учётом уровня интеллекта и возраста ребёнка, а также данных компьютерной томографии.
Кондуктивную тугоухость III-IV степени определяют посредством аудиометрического исследования, которое направлено на оценку слуха. На аудиограмме отмечается костная и воздушная проводимость. Костная проводимость — это прохождение звуковой волны до внутреннего уха через кости черепа, минуя среднее ухо. Воздушная проводимость — прохождения звуковой волны до внутреннего уха обычным путём — через наружное и среднее ухо.
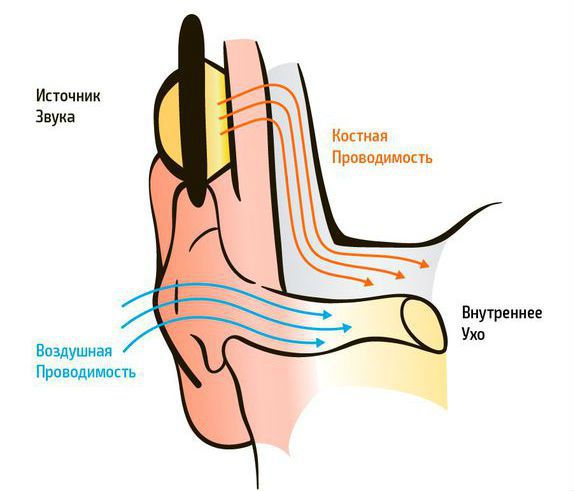
Костная и воздушная проводимость
При кондуктивной тугоухости снижение восприятия звука выявляется только при проверке воздушного звукопроведения. Костная проводимость находится в пределах нормы [9].

Аудиограмма при кондуктивной тугоухости
У детей раннего возраста в качестве методов диагностики нарушений слуха используют определение порогов слышимости (минимального уровня звука, который человек может воспринять) с помощью вызванной отоакустической эмиссии (ОАЭ) и коротколатентных слуховых вызванных потенциалов (КСВП)
Отоакустическая эмиссия исследуется путём регистрации сигнала, который посылают неповреждённые рецепторы слуховой системы (волосковые клетки улитки) в ответ на акустический импульс определённой амплитуды (громкости). Исследование безболезненно для ребёнка и занимает нескольких минут. В оба уха по очереди вводится зонд с микрофоном. Результаты исследования отображаются на мониторе компьютера.
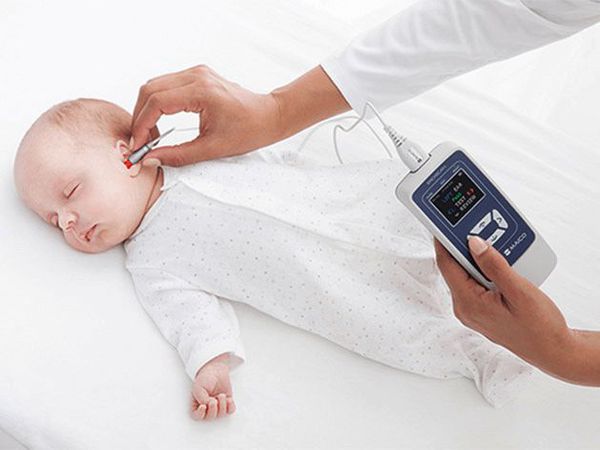
Отоакустическая эмиссия
Если результат положительный, значит ребёнок слышит. Если эмиссия не возникает, то, возможно, есть нарушения в среднем или внутреннем ухе. В этом случае рекомендуется провести исследование КСВП.
Этот метод основан на регистрации коротколатентных вызванных потенциалов. Слуховые вызванные потенциалы (СВП) — это колебания электрического напряжения (потенциала), которые возникают в слуховых восходящих путях в ответ на акустическое стимулирование. СВП регистрируют с поверхности кожи с помощью трёх электродов. Два из них закрепляются на лбу, а один на мочке уха. Чтобы подавать звуковые стимулирующие сигналы, в наружные слуховые проходы вводят мягкие поролоновые аудиометрические вкладыши. В ухо ребёнка посылаются щелчки и звуки определённой частоты. Аппарат регистрирует полученные короткие ответные сигналы и выдаёт результаты в виде графиков. Обследование длится около двух часов.
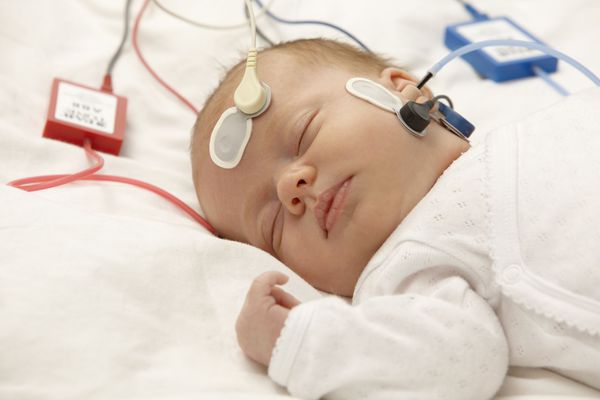
Исследование коротколатентных слуховых вызванных потенциалов
На рентгенологическом исследовании при синдроме Конигсмарка наблюдается: отсутствие наружного слухового прохода, сосцевидный отросток спонгиозного (губчатого) типа, щелевидная барабанная полость, как правило, отсутствие слуховых косточек или их недоразвитие с тугоподвижностью. Внутренний слуховой проход не изменён.
Рентгенологическое обследование детей с синдромом Конигсмарка важно не только для диагностики заболевания: на его основе врач принимает решение о хирургической реконструкции наружного слухового прохода и операции по улучшению слуха.
Для оценки данных мультиспиральной компьютерной томографии височной кости у пациентов с синдромом Конигсмарка и прогнозирования слуховосстанавливающей операции рентгенологами был предложен протокол-таблица результатов МСКТ. Рентгенолог описывает данные компьютерной томографии, а хирург заполняет протокол-таблицу. При отсутствии изменений признаку присваивается 2 балла, при умеренных изменениях — 1 балл. Значительное патологическое изменение оценивается в 0 баллов. То есть максимальное количество баллов — 26, минимальное количество баллов, при котором допускается меатотимпанопластика (операция, направленная на формирование слухового прохода) — 18 [12].
Таблица 1 — Протокол оценки КТ-данных при врождённых пороках развития височных костей.
Прогрессирование тугоухости при синдроме Конигсмарка не характерно.
Лечение синдрома Конигсмарка
Основным методом лечения синдрома Конигсмарка является оперативное. Оно заключается в проведении пластики ушной раковины и формировании наружного слухового прохода.
Возраст начала проведения первого этапа пластики ушной раковины определяется многими факторами, в основном психологическими и физиологическими. В идеале хирургическое вмешательство следует начать прежде, чем ребёнок попадёт в большой коллектив сверстников (детский сад, школу), чтобы избежать психологических травм.
Хирургическое вмешательство допустимо начинать в 6-7 лет в том случае, если восстановление ушной раковины проводят с использованием силиконового имплантата. Если используется рёберный хрящ пациента, операцию следует отложить до того момента, пока хрящевая часть рёбер не достигнет достаточных размеров для изготовления каркаса ушной раковины. Как правило, это происходит в 9-10 лет. Согласно исследованиям, ушные раковины продолжают активно расти примерно до 10 лет, что говорит о целесообразности проведения оперативного вмешательства в этот период. Тогда созданное искусственно наружное ухо дольше сохранит симметрию со здоровым.
Отмечается, что рёберный хрящ сохраняет рост и при пластике наружного уха. Таким образом восстановленные из рёберного хряща ушные раковины растут вместе с окружающими мягкими тканями в течение жизни пациента.
Отопластика — один из наиболее сложных разделов в пластической хирургии. Это объясняется следующим:
- Наружное ухо имеет тонкий упругий хрящ и сложный рельеф, что делает очень трудоёмким воссоздание его формы.
- Изгибы хряща ушной раковины покрыты тонкой, плотно прилегающей кожей.
- Снабжение кровью этой области может быть не таким хорошим, как кровоснабжение других областей лица.
- В самом хрящевом каркасе есть индивидуальные особенности в соотношении различных компонентов (количество хряща, промежуточная ткань, покрывающая кожа), составляющих здоровую ушную раковину [8].
Главная цель каждой реконструкции — воссоздание анатомических структур таким образом, чтобы они максимально соответствовали здоровым. То же самое касается пластики уха. При отсутствии большей части наружного уха достичь этой цели сложнее, чем при менее значительных дефектах.
Успех оперативного лечения больше зависит от соответствия здоровому уху (по размеру, положению, ориентации и анатомическим параметрам), чем от детального повторения естественных анатомических структур. Воссозданное наружное ухо получится естественным только тогда, когда будут воспроизведены вышеперечисленные характеристики. Однако, если какое-то из этих свойств (например, расположение или размер) не будет соответствовать свойствам здоровой ушной раковины, воссозданное ухо не будет выглядеть естественно [15].
Множество научных работ было посвящено проблемам отопластики, подробному описанию клинической анатомии, особенностям врождённых дефектов уха и способам их коррекции. Благодаря этим трудам была выведена техника отопластики, в которой чётко сформировались определённые этапы. Кроме того, учёные почти единогласно определили, что для воссоздания хрящевых структур ушной раковины лучшим источником опорного материала является рёберный хрящ [8].
Отопластика включает в себя три главных этапа:
- Первый этап: в околоушной области формируется подкожный карман. В этот карман помещается рёберный хрящ, он впоследствии станет основой ушной раковины.
- Второй этап: через 4-6 месяцев мочка уха будет перемещена в такое положение, в котором находится мочка уха на противоположной (здоровой) стороне.
- Третий этап: ещё через 4-6 месяцев создаётся кожно-хряще-фасциальный блок. На внутренней поверхности восстановленной ушной раковины и области сосцевидного отростка формируется дефект кожных покровов, который будет замещён свободным расщеплённым или свободным полнослойным кожным трансплантатом.

Отопластика при синдроме Конигсмарка
Для лечения микротии может использоваться ещё один вид импланта — "Медпор". В этом случае новое ухо формируют с помощью пористой полиэтиленовой рамки и аутокожи (кожи с другого участка тела). Такая операция выполняется детям старше трёх лет [2].
Операция с применением медпора менее травматична, так как нет необходимости выполнять надрезы на коже черепа. Это обеспечивает минимальное количество шрамов после восстановления слуха. Протез из медпора делается для каждого пациента индивидуально с учётом формы противоположного уха и небольшим "запасом", чтобы в процессе роста ухо соответствовало "взрослым" размерам. Затем рамка-имплант покрывается аутокожей.
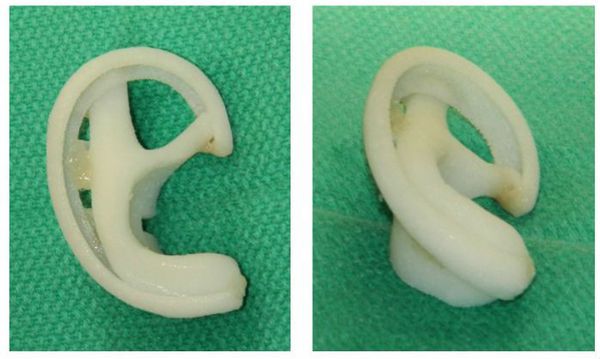
Имплант медпор
Позже появился ещё один способ лечения микротии в рамках операции — использование для восстановления слуха устройств костной проводимости. Эти устройства именуются BAHA (bone anchored hearing aid). Детям до 5 лет систему BAHA закрепляют на голове при помощи мягкой повязки. С 5-летнего возраста в кости черепа вживляется титановый абатмент или особая магнитная вставка-пластина. После завершения процесса заживления к системе подключается внешний звуковой процессор. Этот процессор при работе непосредственно стимулирует пациенту слуховой нерв во внутреннем ухе. Данная методика позволяет исключить оперативное восстановление анатомических структур наружного и среднего уха.
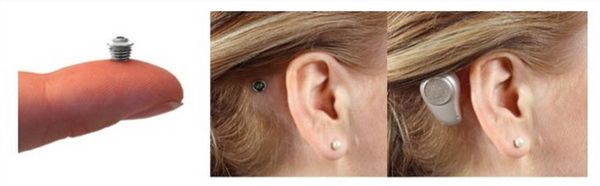
Устройство костной проводимости — BAHA
Новым веянием в лечении атрезии и микротии стало также одновременное оперативное лечение обоих пороков развития.
Реконструктивные операции, производимые отохирургами, являются сложной и не всегда успешно решаемой задачей. Положительный результат оперативного лечения составляет в среднем 12-17 %, около трети больным требуется повторная операция вследствие развития вторичного стеноза (сужения) в области наружного слухового прохода. В случае отсутствия слуховых косточек или при сращении всех слуховых косточек в единый блок требуется оссикулопластика (пластика цепи слуховых косточек). Операция считается успешной, если отмечается прирост слуха. Некоторые отохирурги считают операцию успешной при достижении прироста слуха на 20-25 децибел (дБ), другие видят успех операции в достижении социально-полезного слуха (пороги < 30 дБ) [16].

Уровень интенсивности разных звуков
Послеоперационные осложнения. Так как у пациентов с этой патологией слуховая труба развита нормально, как и у здоровых людей, операция может спровоцировать воспаление среднего уха (средний отит) [6]. В таком случае важна своевременно назначенная системная антибактериальная терапия, так как местное применение антибактериальных препаратов невозможно ввиду отсутствия наружного слухового прохода.
Препаратами выбора являются амоксициллин [3] в дозе 40 мг/кг/сут. или феноксиметилпенициллин в дозе 66 мг/кг/сут. (100000 МЕ/кг/сут). Оба препарата нужно принимать в два приёма. При аллергии на пенициллин в качестве альтернативы можно назначать цефаклор, цефуроксим [4] или сульфаметоксазол+триметоприм в дозе 25+8 мг/кг/сут. в два приёма [5].
Прогноз. Профилактика
Прогноз заболевания и результат операции зависят от степени аномалии барабанной плоскости и возможности создания нового слухового прохода [19].
Как и для большинства редких заболеваний, которые наследуются по аутосомно-рецессивному типу, никаких мер для профилактики синдрома Конигсмарка не разработано. Консультация генетика возможна, но не в качестве рутинного обследования, а скорее для выявления родителя-носителя дефектного гена при свершившемся факте рождения ребёнка с синдромом Конигсмарка. И в этом случае пара может иметь здорового второго ребёнка, так как вероятность повторного случая синдрома в семье составляет 25 %.
Список литературы
Классы МКБ-10 / Q00-Q99 / Q10-Q18 / Q16Врожденные аномалии [пороки развития] уха, вызывающие нарушение слуха (Q16) // МКБ 10 - Международная классификация болезней 10-го пересмотра.
Практические рекомендации отделения челюстно-лицевой хирургии, микрохирургии и эктопротезирования // Микротия. — М., 2020.
Douglas J. Biedenbach, Robert E. Badal, Ming-Yi Huang, Mary Motyl, Puneet K. Singhal, Roman S. Kozlov, Arthur Dessi Roman, and Stephen Marcella. In Vitro Activity of Oral Antimicrobial Agents against Pathogens Associated with Community-Acquired Upper Respiratory Tract and Urinary Tract Infections: A Five Country Surveillance Study // Infect Dis Ther. — 2016; 5(2): 139-153.ссылка
Козлов Р. С. Клиническая микробиология и антимикробная химиотерапия. — 2015. — Т. 17, № 2, Приложение 1, абстракт № 50. — С. 31.
Беликов А. С. Фармакоэпидемиология антибактериальной терапии острых отоларингологических инфекций: автореф. дис. ... канд. мед. наук. — Смоленск, 2001.
Pichichero M. E., Reiner S. A., Jenkins S. G. et al. Controversies in the medical management of persistent and recurrent acute otitis media // Ann Otol Laryngol. — 2000. — № 109. — С. 2-12.
Schuknecht H. Congenital aural atresia and Congenital Middle Ear Cholesteatoma // Surgery of the Ear and Temporal Bone, 1993. — Р. 263-274.
Nagata S. A new method of total reconstruction of auricle for microtia // Plast. Rec. Surg. — 1993;92(2): 187-201.ссылка
Альтман Я. А., Таварткиладзе Г. А. Руководство по аудиологии. — М.: ДМК Пресс, 2003.
Борисова, Е. В. Врождённая ушная атрезия: клиника и хирургическое лечение / Е.В.Борисова // Наука и практика в оториноларингологии: материалы III Российской научно-практической конференции. — М., 2004.
Transitory evoked otoacoustic emission (TEOAE) and distortion product otoacoustic emission (DPOAE) outcomes from a three-stage newborn hearing screening protocol / M. G Tzanakakis, T. S. Chimona, E. Apazidou, C. Giannakopoulou // Hippokratia. — 2016; 20(2): 104-109. ссылка
Куриленков Г. В. Компьютерная томография височной кости у детей (методика исследования и диагностика пороков развития): автореф. дис. ... канд. мед. наук. — М., 2002.
Ear Disease in Skulls From the Sully Burial Site / John B. Gregg et al., // Plains Anthropologist. — 2017. — P. 233-239.
Богомильский М. Р., Чистякова В. Р. Детская оториноларингология. — М.: ГЭОТАР-МЕД, 2002.
Чкадуа Т. З. Реабилитация пациентов с дефектами и деформациями ушных раковин: автореферат дис. ... доктора медицинских наук: 14.01.14, 14.01.17 / Т. З. Чкадуа. — М., 2011. — 36 с.
Тотрова З. А., Осипов Г. И., Караян A. C., Шургая Ц. М. Оптимальный метод восстановления ушной раковины при синдроме Конигсмарка // Стоматология на пороге третьего тысячелетия. —М., 2001. — С. 476-477.
Собчик Л .H. Введение в психологию индивидуальности. Теория и практика психодиагностики — М., 1998. — С. 13-43.
Основы генетики и наследственные нарушения развития у детей: учеб. пособие для студ. высш. пед. учеб, заведений /А. Ю. Асанов, Н. С. Демикова, С. А.Морозов; под ред. А. Ю. Асанова. — М.: Академия, 2003. — 224 с.
Хоров О. Г., Плавский Д. М. Опыт применения меатотимпанопластики в хирургическом лечении врожденной атрезии наружного слухового прохода // Журнал Гродненского государственного медицинского университета. — 2009. — № 4 (28). — С. 85-87.
Conductive deafness-malformed external ear syndrome [Электронный ресурс] // Orphanet (дата обращения 06.11.2020).

