Определение болезни. Причины заболевания
Острый парапроктит — острое воспаление околопрямокишечной клетчатки, обусловленное распространением воспалительного процесса из анальных крипт и анальных желез.
Острый парапроктит (в англоязычной литературе — аноректальный абсцесс) возникает из-за инфекции в криптогландулярном эпителии, выстилающем анальный канал.
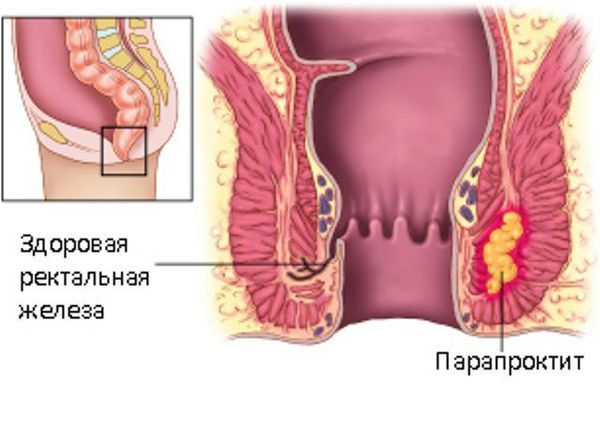
Здоровая ректальная железа и парапроктит
Около 30% пациентов с аноректальными абсцессами сообщают о возникновении подобных абсцессов ранее, которые либо разрешались спонтанно, либо требовали хирургического вмешательства.
Частота образования абсцессов выше весной и летом. В разных странах и регионах мира нет четкой статистики.
Ранее высказывалось предположение, что существует прямая связь между образованием аноректальных абсцессов и привычками кишечника, частой диареей и плохой личной гигиеной, однако эта связь остается недоказанной.
Пиковая частота аноректальных абсцессов приходится на 30-40 лет. Мужчины страдают в 2-3 раза чаще, чем женщины.
К образованию абсцессов могут приводить аэробные и анаэробные бактерии. Наиболее часто встречающиеся анаэробы: Bacteroides fragilis, Peptostreptococcus, Prevotella, Fusobacterium, Porphyromonas и Clostridium. Наиболее часто встречающиеся аэробы: Staphylococcus aureus, Streptococcus и Escherichia coli.
В более поздних исследованиях был выявлен метициллин-устойчивый S. aureus (MRSA) как микроорганизм, приводящий к образованию абсцессов.[8][9]
Приблизительно 10% аноректальных абсцессов могут быть вызваны причинами, не связанными с анальными железами, это:
- болезнь Крона;
- травмы;
- иммунодефицит, вызванный ВИЧ-инфекцией или злокачественными новообразованиями (гематологические, аноректальные);
- туберкулез;
- гнойный гидраденит;
- заболевания, передаваемые половым путем;
- лучевая терапия;
- инородные тела;
- перфорация дивертикула при дивертикулярной болезни;
- воспалительные заболевания кишечника или аппендицит (редкая причина тазово-прямокишечных абсцессов).[1]
Симптомы острого парапроктита
Классические положения аноректальных абсцессов следующие:
- перинальные (подкожные) (60%);
- ишиоректальные (20%);
- межсфинктерные (5%);
- супралеваторные (4%);
- подслизистые (1%).
Клиническая картина коррелирует с анатомическим расположением абсцесса (хотя следует иметь в виду, что подкожный абсцесс иногда не является изолированным поверхностным поражением, а представляет собой внешнее проявление более глубокого абсцесса).
Почти все параректальные абсцессы проявляются болью в области промежности и прямой кишки. Пациенты с подкожным абсцессом обычно жалуются на перианальный дискомфорт и зуд. Боль часто вызывается движением и повышением давления на промежность от сидения или дефекации. При ишиоректальных парапроктитах возникает лихорадка, озноб, выраженная боль в промежности, появление инфильтрата.
До 50% пациентов с парапроктитами могут иметь отек вокруг прямой кишки, а у 25% выделения: кровянистые, гнойные или слизистые.[2][4] Эти пациенты могут также жаловаться на запор, скорее всего, из-за боли при дефекации, но отсутствие запора или даже диарея не исключают диагноза. Большинство пациентов не сообщают об истории лихорадки или озноба.
Патогенез острого парапроктита
В нормальной анатомии анального канала присутствуют 4-10 анальных желез, лежащих на уровне зубчатой линии, которая разделяет плоскоклеточный эпителий дистально и цилиндрический эпителий проксимально. Считается, что внутренний анальный сфинктер обычно служит барьером для инфекции, проходящей из просвета кишки до глубоких параректальных тканей. Этот барьер может быть прорван через крипты Морганьи, которые проникают через внутренний сфинктер в межсфинктерное пространство. Как только инфекция получает доступ к межсфинктерному пространству, дальше у неё есть доступ к смежным параректальным пространствам. Распространение инфекции может происходить в межсфинктерном, ишиоректальном или супралеваторном пространстве. В некоторых случаях абсцесс остается в пределах внутрисфинктерного пространства. Тяжесть и глубина абсцесса довольно разнообразны, а полость абсцесса часто связана с образованием свищевого тракта.
Аноректальный абсцесс — заболевание, возникающее преимущественно (~ 90% случаев) из-за обструкции анальных крипт,[4] возможно при повышении тонуса сфинктера.[6] Инфицирование секрета желез приводит к нагноению и образованию абсцесса в анальной железе. Как правило, абсцесс формируется изначально в межсфинктерном пространстве, а затем распространяется вдоль соседних клетчаточных пространств.
Аноректальный абсцесс
Классификация и стадии развития острого парапроктита
Разнообразие анатомических локализаций первичной инфекции выражается в разных клинических проявлениях. Относительно простой перианальный абсцесс следует отличать от более сложных периректальных абсцессов.
Аноректальные абсцессы классифицируются в соответствии с их анатомическим расположением:
- перианальный (подкожный);
- седалищно-прямокишечный (ишиоректальный);
- интерсфинктерный;
- супралеваторный (тазово-прямокишечный).
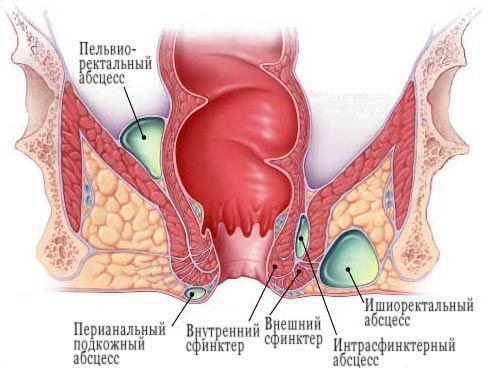
Классификация аноректальных абсцессов
Перианальные (подкожные) абсцессы представляют собой наиболее распространенный тип, на которые приходится примерно 60% зарегистрированных случаев.[1][2][3][4]
Это поверхностное скопление гноя расположено в подкожной клетчатке и не пересекает наружный сфинктер.
Ишиоректальные абсцессы образуются, когда гнойник через наружный сфинктер распространяется в ишиоректальное клетчаточное пространство. Ишиоректальный абсцесс может распространяться через позадианальное пространство в контралатеральную сторону, образуя так называемый подковообразный абсцесс.
Интерсфинктерные абсцессы, третий наиболее распространенный тип, являются результатом нагноения, возникающего между внутренним и внешним анальным сфинктером. Они могут локализоваться полностью в анальном канале, что приводит к сильной боли и может быть обнаружено только путем ректального обследования или аноскопии.
Супралеваторные (тазово-прямокишечные) абсцессы, наименее распространенные из четырех основных типов, могут образовываться из-за проксимального распространения межсфинктерного абсцесса над мышцей, поднимающей задний проход. Эти абсцессы могут быть диагностированы с помощью компьютерной томографии (КТ) и вызывают тазовые и ректальные боли.
Осложнения острого парапроктита
- формирование свища (фистулы), встречается у 30-60% пациентов с аноректальными абсцессами;
- бактериемия и сепсис, включая гематогенное распространение инфекции;
- недержание кала;
- злокачественные новообразования.
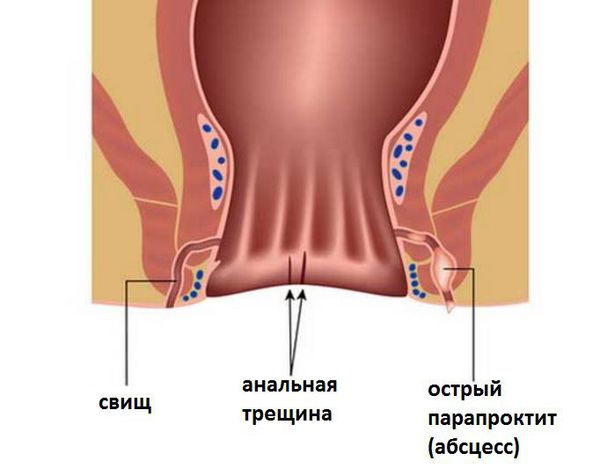
Формирование свища
Диагностика острого парапроктита
При оценке жизненно важных систем отклонений, как правило, не находят.
При осмотре промежности отмечается четко выраженный болезненный инфильтрат и гиперемированная кожа, пальпаторно можно определить зону флюктуации (размягчения).[2]
Пациенты с интерсфинктерным абсцессом при пальцевом ректальном осмотре жалуются на локальную болезненность, но иногда осмотр не позволяет идентифицировать межсфинктерный абсцесс.
Редкие супралеваторные (тазово-прямокишечные) абсцессы представляют собой сложную диагностическую проблему. В результате клинического подозрения на интерсфинктерный или супралеваторный абсцесс может потребоваться подтверждение с помощью компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ) или анальной ультрасонографии.
Пальцевой осмотр с анестезией может быть полезен в некоторых случаях, поскольку дискомфорт пациента может значительно ограничить оценку локального статуса.
Дифференциальный диагноз:
- боль в животе у пожилых людей (ишемический колит);
- анальные трещины;
- геморрой;
- воспалительные заболевания кишечника;
- ректальный пролапс.
Лабораторная диагностика
Лабораторная диагностика не является ведущей в постановке диагноза. В общем анализе крови может выявляться, иногда со сдвигом лейкоцитарной формулы влево. 23% пациентов с перианальными абсцессами имеют нормальную температуру и нормальное количество лейкоцитов.[2]
Несмотря на то, что назначение антибиотиков не требуется при вскрытии неосложненных перианальных абсцессов, [21][22] посев раневого отделяемого, с выделением культуры микроорганизмов, должен проводиться у всех пациентов, с целью выявление новых штаммов бактерий (например, резистентный к метициллину S. aureus ).[1][2][8][9]
Инструментальные методы (КТ, УЗИ и МРТ)
Вспомогательные инструментальные методы требуются при подозрении на абсцесс интерсфинктерный или супралеваторный.[23][24]
Как правило, использование анальной ультрасонографии ограничивается подтверждением наличия межсфинктерного абсцесса, также может использоваться внутриоперационно, чтобы помочь определить сложный абсцесс или свищ.
КТ обычно используется для диагностики абсцессов супралеваторных. Чувствительность метода 77%.[25]
Трансперинеальная ультрасонография показала хорошие результаты для обнаружения свищей и сбора жидкости в предоперационном планировании с чувствительностью от 85%[26][27][28] до 100%[29] или обнаружения хирургически значимого заболевания.
Чувствительность МРТ составляет 91%, что делает его полезным при предоперационном планировании,[30] однако использование МРТ ограничено.
Эндоскопия
Использование эндоскопической визуализации (трансректальной и трансанальной) является отличным способом оценки сложных случаев перианального абсцесса и свища (фистулы). С помощью эндоскопической техники можно четко визуализировать степень и конфигурацию абсцесса и свищей. Эндоскопическая визуализация столь же эффективна, как и фистулография.
Лечение острого парапроктита
Наличие абсцесса является показанием для вскрытия и дренирования. Введение антибиотиков является недостаточным. Задержка хирургического вмешательства приводит к хроническому разрушению тканей, фиброзу и образованию стриктур и может ухудшить анальное удержание.
Адекватный дренаж абсцесса является самым важным фактором в борьбе с прогрессирующей перианальной инфекцией.
Фармакологическая терапия
Рутинное назначение антибиотиков у пациентов с аноректальными абсцессами не требуется, так как нет доказательств ускорения времени заживления или уменьшения частоты рецидивов. Назначение антибиотиков оправдано пациентам с:[1]
- системным воспалительным ответом или сепсисом;
- обширным целлюлитом;
- диабетом;
- иммунодепрессией;
- пороками сердца и протезированием клапанов сердца.
Хирургическое вмешательство
Подготовка к оперативному вмешательству не требуется. Оно проводится под спинномозговой анестезией или наркозом.
Хирургическое дренирование гнойной полости:
Разрез должен быть сделан как можно ближе к анусу.[1] Гной эвакуируется, а рана заполняется салфеткой с йодопироном. Дренаж устанавливают только для лечения сложных или двусторонних абсцессов. Через 24 часа салфетку удаляют, и пациенту дается указание принимать сидячие ванны три раза в день и после дефекации. Послеоперационные анальгетики и размягчители стула назначают для облегчения боли и предотвращения запора.
Дренирование межсфинктерного абсцесса: в анальном канале делается поперечный разрез ниже зубчатой линии сзади. Выделяется интерсфинктерное пространство и открывается плоскость между внутренним и внешним сфинктерами. Абсцесс вскрывается, оставляется небольшой дренаж, для преждевременного закрытия раны.
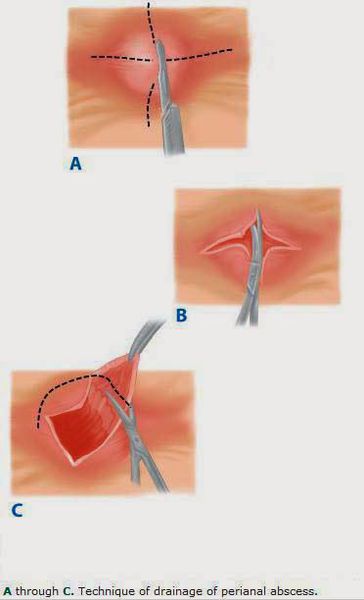
Дренирование межсфинктерного абсцесса
Техника дренирования супралеваторных абсцессов определяется положением и этиологией поражения. Оценка с помощью магнитно-резонансной томографии (МРТ) или компьютерной томографии (КТ) может исключать внутрибрюшную или тазовую патологию как возможные источники.
Если супралеваторный абсцесс развивается из ишиоректального абсцесса, то дренирование проводится через ишиоректальную ямку. Если абсцесс был вызван продолжением межсфинктерного парапроктита, то дренирование проводится через слизистую.
Если клиническое состояние пациента не улучшится в течение следующих 24-48 часов, необходима переоценка состояния с помощью КТ или повторной операции. Некоторым пациентам с рецидивирующими, тяжелыми абсцессами может потребоваться формирование колостомы.
Прогноз. Профилактика
Общая смертность от аноректальных абсцессов низкая.[2]
Ранние данные указывали на то, что образование абсцесса повторяется примерно у 10% пациентов, причем свищ формируется почти у 50% пациентов.[1][2][12]
Более позднее исследование показало, что у 37% пациентов сформировался свищ или возникал рецидив парапроктита (абсцесса).[6]
Список литературы
Whiteford MH. Perianal abscess/fistula disease. Clin Colon Rectal Surg. 2007 May. 20(2):102-9
Marcus RH, Stine RJ, Cohen MA. Perirectal abscess. Ann Emerg Med. 1995 May. 25(5):597-603
Pfenninger JL, Zainea GG. Common anorectal conditions: Part II. Lesions. Am Fam Physician. 2001 Jul 1. 64(1):77-88
Rizzo JA, Naig AL, Johnson EK. Anorectal abscess and fistula-in-ano: evidence-based management. Surg Clin North Am. 2010 Feb. 90(1):45-68, Table of Contents
Parks AG, Gordon PH, Hardcastle JD. A classification of fistula-in-ano. Br J Surg. 1976 Jan. 63(1):1-12
Hamadani A, Haigh PI, Liu IL, Abbas MA. Who is at risk for developing chronic anal fistula or recurrent anal sepsis after initial perianal abscess?. Dis Colon Rectum. 2009 Feb. 52(2):217-21
Brook I, Frazier EH. The aerobic and anaerobic bacteriology of perirectal abscesses. J Clin Microbiol. 1997 Nov. 35(11):2974-6
Albright JB, Pidala MJ, Cali JR, Snyder MJ, Voloyiannis T, Bailey HR. MRSA-related perianal abscesses: an underrecognized disease entity. Dis Colon Rectum. 2007 Jul. 50(7):996-1003
Brown SR, Horton JD, Davis KG. Perirectal abscess infections related to MRSA: a prevalent and underrecognized pathogen. J Surg Educ. 2009 Sep-Oct. 66(5):264-6
Beard JM, Osborn J. Anorectal Abscess. Rakel RE, Rakel DP, eds. Textbook of Family Medicine. 8th ed. Philadelphia, Pa: Saunders; 2011
Novotny NM, Mann MJ, Rescorla FJ. Fistula in ano in infants: who recurs?. Pediatr Surg Int. 2008 Nov. 24(11):1197-9
Hämäläinen KP, Sainio AP. Incidence of fistulas after drainage of acute anorectal abscesses. Dis Colon Rectum. 1998 Nov. 41(11):1357-61; discussion 1361-2
Athanasiadis S, Köhler A, Nafe M. Treatment of high anal fistulae by primary occlusion of the internal ostium, drainage of the intersphincteric space, and mucosal advancement flap. Int J Colorectal Dis. 1994 Aug. 9(3):153-7
Abbas MA, Lemus-Rangel R, Hamadani A. Long-term outcome of endorectal advancement flap for complex anorectal fistulae. Am Surg. 2008 Oct. 74(10):921-4
Hyman N, O'Brien S, Osler T. Outcomes after fistulotomy: results of a prospective, multicenter regional study. Dis Colon Rectum. 2009. 52:2022-7
Weizberg M, Gillett BP, Sinert RH. Penile discharge as a presentation of perirectal abscess. J Emerg Med. 2008 Jan. 34(1):45-7
Smereck J, Ybarra M. Acute hip pain and inability to ambulate: a rare presentation for perirectal abscess. Am J Emerg Med. 2011 Mar. 29(3):356.e1-3
Bennetsen DT. Perirectal abscess after accidental toothpick ingestion. J Emerg Med. 2008 Feb. 34(2):203-4
Erhan Y, Sakarya A, Aydede H, Demir A, Seyhan A, Atici E. A case of large mucinous adenocarcinoma arising in a long-standing fistula-in-ano. Dig Surg. 2003. 20(1):69-71
Fish D, Kugathasan S. Inflammatory bowel disease. Adolesc Med Clin. 2004 Feb. 15(1):67-90, ix
Whiteford MH, Kilkenny J 3rd, Hyman N, Buie WD, Cohen J, Orsay C, et al. Practice parameters for the treatment of perianal abscess and fistula-in-ano (revised). Dis Colon Rectum. 2005 Jul. 48(7):1337-42
Sözener U, Gedik E, Kessaf Aslar A, Ergun H, Halil Elhan A, Memikoglu O, et al. Does adjuvant antibiotic treatment after drainage of anorectal abscess prevent development of anal fistulas? A randomized, placebo-controlled, double-blind, multicenter study. Dis Colon Rectum. 2011 Aug. 54(8):923-9
Chandwani D, Shih R, Cochrane D. Bedside emergency ultrasonography in the evaluation of a perirectal abscess. Am J Emerg Med. 2004 Jul. 22(4):315
Tio TL, Mulder CJ, Wijers OB, et al. Endosonography of peri-anal and peri-colorectal fistula and/or abscess in Crohn's disease. Gastrointest Endosc. 1990 Jul-Aug. 36(4):331-6
Caliste X, Nazir S, Goode T, Street JH 3rd, Hockstein M, McArthur K, et al. Sensitivity of computed tomography in detection of perirectal abscess. Am Surg. 2011 Feb. 77(2):166-8
Berton F, Gola G, Wilson SR. Sonography of benign conditions of the anal canal: an update. AJR Am J Roentgenol. 2007 Oct. 189(4):765-73
Stewart LK, McGee J, Wilson SR. Transperineal and transvaginal sonography of perianal inflammatory disease. AJR Am J Roentgenol. 2001 Sep. 177(3):627-32
Buchanan GN, Halligan S, Bartram CI, Williams AB, Tarroni D, Cohen CR. Clinical examination, endosonography, and MR imaging in preoperative assessment of fistula in ano: comparison with outcome-based reference standard. Radiology. 2004 Dec. 233(3):674-81
Domkundwar SV, Shinagare AB. Role of transcutaneous perianal ultrasonography in evaluation of fistulas in ano. J Ultrasound Med. 2007 Jan. 26(1):29-36
Berman L, Israel GM, McCarthy SM, Weinreb JC, Longo WE. Utility of magnetic resonance imaging in anorectal disease. World J Gastroenterol. 2007 Jun 21. 13(23):3153-8

