Определение болезни. Причины заболевания
Гипофизарный нанизм, или гипопитуитаризм — это заболевание, при котором частично или полностью прекращается выработка гормона роста — соматотропина (соматотропного гормона) [1]. Оно сопровождается нарушением роста скелета, из-за чего мужчины не вырастают выше 130 см, а женщины — выше 120 см. В связи с этим характерным проявлением болезнь также называют карликовостью.
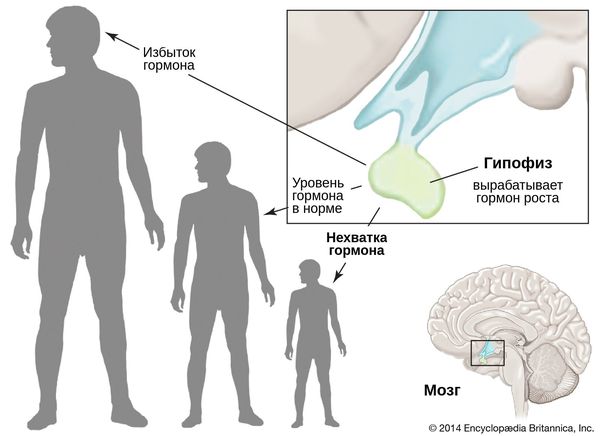
Рост человека в зависимости от уровня соматотропного гормона
Наиболее частые причины гипофизарного нанизма:
- Наследственность — мутации в гене соматотропного гормона (GH1) или его рецепторах. Частота встречаемости врождённого гипопитуитаризма колеблется от 1:4000 до 1:10000 [5].
- Дефекты развития гипоталамо-гипофизарной системы — области головного мозга, где вырабатывается соматотропный гормон:
- гипоплазия (недоразвитие) гипофиза;
- полное отсутствие гипофиза. При этом дефицит гормона роста сочетается с нехваткой других гормонов, которые вырабатываются в гипофизе. Такое состояние называется пангипопитуитаризмом. Оно проявляется надпочечниковой недостаточностью, ухудшением работы щитовидной железы (гипотиреозом), несахарным диабетом, гипогонадотропным гипогонадизмом (отсутствием полового развития и дефицитом гормона роста).
- Опухоли гипофиза:
- краниофарингиома — доброкачественная опухоль гипофизарной области, одна из самых распространённых в детском возрасте;
- гамартома — редкий вид доброкачественной опухоли;
- герминома — редкий вид опухоли, чаще всего бывает злокачественной — и др.
- Травмы головного мозга с повреждением гипофиза, возникшие до того, как человек достиг социально приемлемого роста — 155-170 см (например, родовая травма).
- Инфекционные заболевания — менингиты, энцефалиты и др.
- Облучение головы и шеи.
- Токсические последствия химиотерапии.
Теоретически, спровоцировать развитие гипофизарного нанизма может любое заболевание, которое будет затрагивать работу гипофиза.
Симптомы гипофизарного нанизма
Гипофизарный нанизм проявляется по-разному. Симптоматика зависит от причин дефицита гормона роста.
Основной симптом — отставание в темпах линейного роста [2]. Такие дети вырастают менее чем на 4 см в год. Нарушение динамики роста будет заметно уже в первые месяцы жизни ребёнка. Если повреждение гипоталамуса или гипофиза возникло в более позднем возрасте, то отставание в росте будет отмечаться позднее. Также для детей с гипофизарным нанизмом характерно отставание костного (биологического) возраста от паспортного (фактического) более чем на 2-3 года.
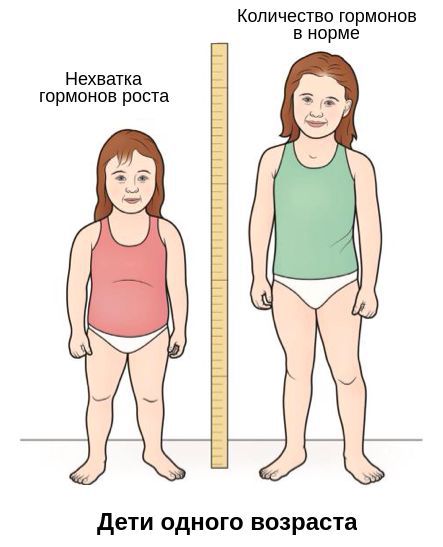
Отставание в росте
При нехватке гормонов роста телосложение остаётся пропорциональным. Это важный диагностический критерий: он позволяет исключить разные формы скелетных дисплазий [9].
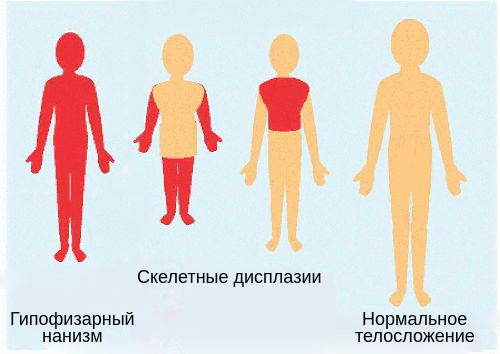
Пропорции тела
Задержка полового развития в период полового созревания объясняется отставанием костного возраста. В норме начало полового созревания у девочек наступает в период с 8-13 лет, у мальчиков — с 9-14 лет. При этом у девочек начинают расти грудные железы, а у мальчиков увеличивается объём яичек. У детей с дефицитом гормона роста эти признаки полового созревания появляются позже обычного.
Симптомами врождённого гипофизарного нанизма у новорождённых являются:
- гипогликемия — низкий уровень глюкозы в крови натощак. Это физиологическое состояние может встречаться и у здоровых детей из-за незрелости поджелудочной железы. Дети с нанизмом сталкиваются с ним гораздо чаще, особенно на первом году жизни, поскольку гормон роста участвует в регуляции углеводного обмена;
- позднее закрытие большого родничка;
- задержка костного созревания;
- истончение кожи — может быть связано со снижением функции щитовидной железы;
- медленный рост ногтей и волос;
- высокий голос.
Часто у детей с гипопитуитаризмом встречается множественный кариес зубов. Это объясняется задержкой окостенения скелета и снижением обменных процессов в костной ткани.
Психоинтеллектуальное развитие у детей с гипофизарным нанизмом, как правило, не страдает, но возможны некоторые психологические проблемы: повышенная потребность в родительской опеке, снижение самооценки, трудности в общении со сверстниками.
Патогенез гипофизарного нанизма
В зависимости от причин дефицита соматотропного гормона есть несколько вариантов механизмов развития заболевания. При этом в основе патогенеза всегда будет лежать нарушение выработки гормона роста. В дальнейшем его нехватка станет причиной нарушения работы органов и систем, на которые он оказывает влияние: костной, мышечной и соединительной ткани, жирового углеводного обмена. В некоторых случаях первоначально будут развиваться гипоталамические нарушения, а недостаточность соматотропного гормона станет вторичным проявлением.
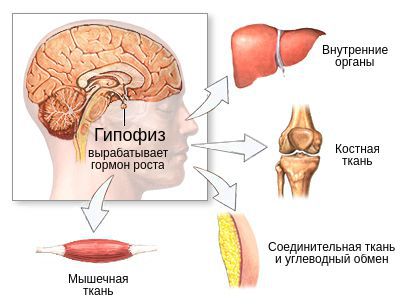
Влияние гормона роста на организм
Молекулярной основой изолированного дефицита гормона роста является мутация определённого гена, которая не даёт организму синтезировать гормон. От видов генетических мутаций зависит, будет ли дефицит соматотропного гормона изолированным, или же он будет сочетаться с нехваткой других гормонов гипофиза, которые лежат в основе других патологий:
- дефицит тиреотропного гормона — вторичный гипотиреоз;
- дефицит пролактина — гипопролактинемия;
- дефицит гонадотропинов — аменорея и недоразвитие половых органов у женщин, снижение потенции и либидо у мужчин;
- дефицит АКТГ — вторичная недостаточность надпочечников;
- дефицит вазопрессина — несахарный диабет;
- дефицит кортизола — гипокортицизм.
У некоторых пациентов с мутацией конкретных генов выявляется гиперплазия передней доли гипофиза (аденогипофиза). В процессе жизни может произойти её атрофия вплоть до формирования синдрома "пустого турецкого седла" — недостаточности области головного мозга, где расположен гипофиз. Данный синдром приводит к внедрению мягкой мозговой оболочки в полость турецкого седла, сдавлению и уменьшению гипофиза, что нарушает или полностью прекращает его работу.
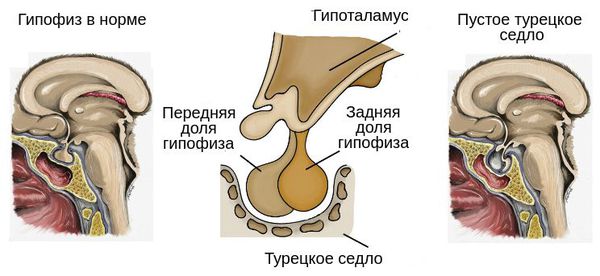
Синдром "пустого турецкого седла"
В подобных случаях дефицит гормона роста и других гормонов гипофиза будет возникать постепенно [3].
Классификация и стадии развития гипофизарного нанизма
Единой, общепринятой классификации гипофизарного нанизма не существует. Наиболее удобной для практикующих врачей является классификация, основанная на причинах заболевания. Она выделяет две большие группы: врождённый и приобретённый гипопитуитаризм [4].
Врождённый гипофизарный нанизм делится на три подгруппы:
- Наследственный:
- изолированный дефицит гормона роста: мутации гена самого гормона (GH1) или мутации гена рецептора к соматотропину (GHRHR);
- множественный дефицит гормонов передней доли гипофиза: мутации гена PIT-1 или гена PROP1.
- Идиопатический (незафисимый) дефицит СТГ-релизинг гормонов, которые стимулируют выработку гормонов передней доли гипофиза.
- Дефекты развития гипоталамо-гипофизарной системы:
- патология срединной трубки;
- нарушение развития гипофиза: врождённая аплазия (отсутствие гипофиза), гипоплазия (недоразвитие), эктопия (неправильное расположение).
Приобретённый гипофизарный нанизм включает в себя девять причин развития болезни:
- Опухоли гипоталамуса и гипофиза: краниофарингиома, гамартома, нейрофиброма, герминома, аденома гипофиза.
- Опухоли других отделов мозга: глиома зрительного перекреста.
- Травмы: черепно-мозговая, хирургическое повреждение ножки гипофиза.
- Инфекционные заболевания: вирусный, бактериальный энцефалит и менингит, неспецифический гипофизит (воспаление гипофиза).
- Супраселлярные арахноидальные кисты — полые опухоли, заполненные жидкостью (ликвором), которые распространяются в полость черепа.
- Сосудистые нарушения: аневризмы сосудов гипофиза, инфаркт гипофиза.
- Облучение головы и шеи по поводу лейкемии, медуллобластомы, ретинобластомы; общее облучение всего тела (при пересадке костного мозга).
- Токсические последствия химиотерапии.
- Инфильтративные болезни: саркоидоз, гистиоцитоз.
Осложнения гипофизарного нанизма
Осложнения заболевания связаны с утратой воздействия гормона роста на органы и системы. Они развиваются вследствие несвоевременной диагностики.
У новорождённого с дефицитом соматотропина относительную опасность может представлять гипогликемическое состояние, поскольку этот гормон играет важную роль в регуляции углеводного обмена. Клинически гипогликемия проявляется бледностью, потливостью, повышенным аппетитом, беспокойством ребёнка, иногда наблюдается судорожный синдром [5].
Гипогликемия новорождённого
Так как сомтатотропин усиливает синтез белка и тормозит его распад, у детей с дефицитом этого гормона может снизиться уровень общего белка в организме и его фракций. Это сказывается на общем физическом развитии: снижается иммунитет, повышается риск присоединения других гормональных сопутствующих нарушений.
Значительная часть эффектов гормона роста передаётся через ИПФР-I (инсулиноподобный фактор роста-I). Он вырабатывается в печени под действием соматотропина и стимулирует рост внутренних органов. Вследствие дефицита соматотропного гормона рост и своевременное развитие органов может частично нарушиться. Это приводит к нарушению работы печени, почек, сердечно-сосудистой системы. Такое осложнение встречается нечасто.
При дефиците гормона роста совместно с другими гормонами гипофиза (пангипопитуитаризме) будет развиваться недостаточность других эндокринных желёз — щитовидной железы, надпочечников, репродуктивной системы. Несвоевременная диагностика этих нарушений после рождения опасна для жизни, а также может стать причиной необратимым нарушений психического или интеллектуального развития.
Диагностика гипофизарного нанизма
Диагностика заболевания начинается с оценки линейного роста ребёнка и скорости прибавки в росте. Для этого врачи сравнивают фактические параметры ребёнка с предполагаемым ростом и среднестатистической скоростью роста. Подставив все данные в специальную формулу, они вычисляют коэффициент стандартного отклонения. Если у ребёнка отставание в росте больше двух сигмальных отклонений, плохая скорость прибавки роста, то проводится дальнейшее обследование.
Затем врачи определяют костный возраст. Сделать это можно с помощью рентгена или УЗИ запястья. В норме костный возраст может отставать или опережать паспортный на два года.
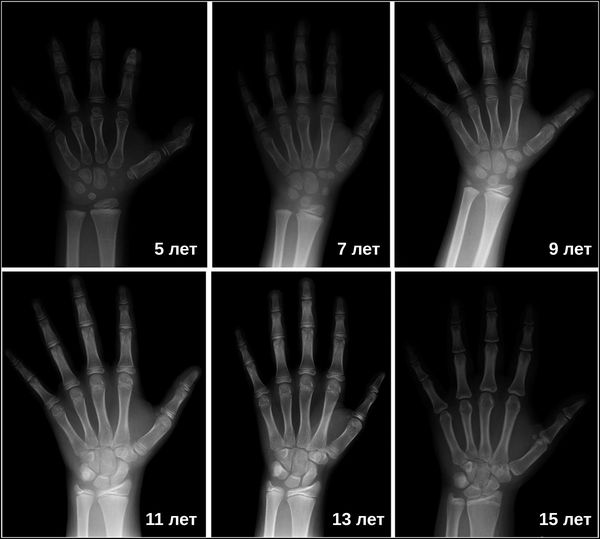
Пример созревания детского скелета
Также важно провести оценку гормонального профиля:
- уровень тиреотропного гормона (ТТГ) и свободного тироксина (Т4) — проверка работы щитовидной железы;
- уровень кортизола и АКТГ (кортикотропина) — исключение нарушений работы надпочечников [10];
- уровень лютеинизирующего гормона (ЛГ) и фоллитропина (ФСГ) — исключение гипогонадотропного гипогонадизма в возрасте, когда должно начаться половое созревание;
- инсулиноподобный фактор роста-I (ИПФР-I) — оценка уровня гормона роста.
Прямая оценка уровня соматотропина, как правило, не проводится. Гормон роста в течение суток выделяется в разном количестве, поэтому узнать его истинный уровень невозможно.
При необходимости проводится МРТ головного мозга и гипофиза с контрастированием[6]. Она позволяет исключить или подтвердить наличие объёмных образований области гипофиза и головного мозга.
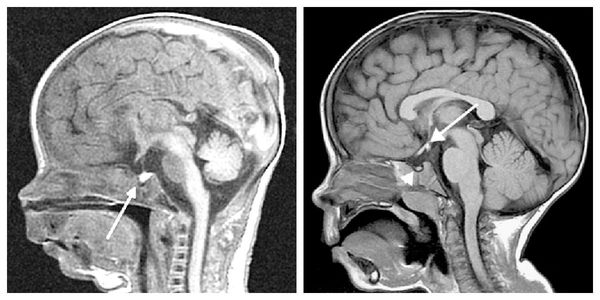
МРТ-снимки новорождённых: слева гипофиз здорового ребёнка, справа — ребёнка с дефицитом гормона роста
Для дифференциальной диагностики задержки роста, не связанной с гормоном роста, исключают дефицит железа, дефицит витамина D, общего белка и другие дефицитные состояния, т. к. их наличие может отрицательно влиять на скорость линейного роста. Рентгенография черепа в данном случае не информативна.
Для исключения определённых генетических синдромов может потребоваться консультация генетика.
При подозрении на истинный дефицит гормона роста проводятся пробы на стимуляцию соматотропина. Эти провокационные тесты стимулируют выброс гормона роста при введении определённых препаратов. Они проводятся только после исключения других возможных причин низкорослости. На основании этих проб, при отсутствии должного выброса гормона роста, будет установлен диагноз "гипопитуитаризм".
Лечение гипофизарного нанизма
Лечение проводится рекомбинантным гормоном роста, который получают методом генной инженерии. Он назначается после исключения активных злокачественных новообразований и тяжёлых сопутствующих заболеваний (как физических, так и психических). Эти состояния являются противопоказанием к использованию данного препарата.
Если имеются другие дефициты гормонов гипофиза, то перед лечением их также нужно компенсировать. Иначе должного эффекта от применения гормона роста не будет.
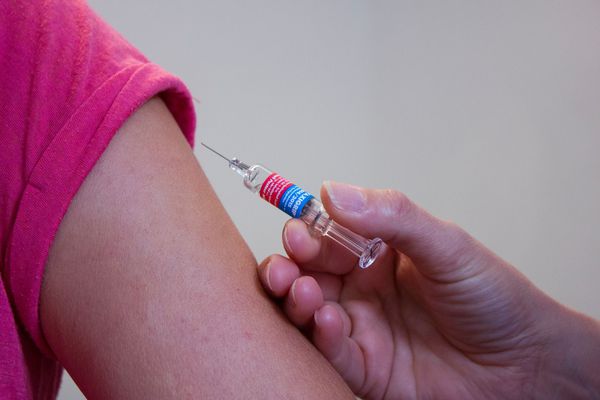
Лечение гипофизарного нанизма рекомбинантным гормоном роста
Цели лечения:
- ускорить темп роста и нормализовать рост;
- стимулировать начало периода полового созревания с нормальным ростом;
- достичь генетически прогнозируемого роста ребёнка или опередить его;
- улучшить качество жизни;
- повысить минеральную плотность костей;
- снизить факторы риска сердечно-сосудистых заболеваний.
Противопоказания к назначению рекомбинантным гормоном роста:
- закрытые зоны роста, за счёт которых происходит линейный рост (при их закрытии человек перестаёт расти);
- активные злокачественные новообразования;
- прогрессирующий рост внутричерепных опухолей;
- аллергия на препарат.
Прекращают терапию гормоном роста при:
- закрытии зон роста;
- плохой скорости прибавки роста — менее 2 см в год;
- достижении социально приемлемого роста.
Крайне редко возможны побочные эффекты и осложнения при терапии гормоном роста:
- доброкачественная внутричерепная гипертензия — повышение внутричерепного давления;
- боли в суставах — обычно наблюдаются при значительном ускорении линейного роста;
- возможно усугубление заболеваний, связанных с недифференцированными дисплазиями соединительной ткани (сколиозов);
- отёки — связано с функцией гормона роста задерживать жидкости в организме;
- пубертатная гинекомастия — увеличение грудных желёз за счёт разрастания железистой ткани у мальчиков [7].
Прогноз. Профилактика
Прогноз заболевания при своевременной диагностике и проведении должного лечения, как правило, благоприятный. Дети достигают своего генетически прогнозируемого роста и иногда даже опережают его.
Если дефицит гормона роста сочетается с дефицитом других гормонов гипофиза, то для достижения желаемого эффекта, профилактики ухудшения состояний и более лёгкой социальной адаптации ребёнка необходимо лечение других дефицитов.
Также очень важен чёткий и своевременный контроль во время лечения гормоном роста: оценка динамики линейного роста, гормонального статуса и костного возраста. Особое внимание необходимо уделять режиму лечения и своевременной коррекции дозы препарата с учётом прибавки в росте и весе. При применении соматотропного гормона доза препарата будет увеличиваться. При несвоевременной прибавке дозы динамика роста может ухудшится [8].
Мониторинг детей, находящихся на лечении, проводится раз в полгода, при других сопутствующих дефицитах гормонов гипофиза — по показаниям.
Вопрос профилактики данного заболевания сложен, т. к. речь идёт о генетических нарушениях. В первую очередь важен ответственный подход будущих родителей к рождению ребёнка:
- своевременное обследование и лечение заболеваний;
- восполнение дефицитов при планировании беременности;
- отказ от вредных привычек.
Для профилактики дефицита гормона роста, который возникает вследствие другого заболевания (инфекции, опухоли, травмы), следует проводить профилактики первоисточника.
Список литературы
World Health Organization (WHO). ICD-10 classification of mental and behavioural disorders: diagnostic criteria for research 1993. — Geneva (Switzerland), 1993.
Calabria A. Growth hormone deficiency in children // MSD Manual. — 2018.
Гарднер Д., Шобек Д. Базисная и клиническая эндокринология / под ред. Г. А. Мельниченко. — М., 2015. — С. 169.
Российская ассоциация эндокринологов. Федеральные клинические рекомендации по ведению детей с эндокринными заболеваниями. — М., 2014 — С. 338.
Kurtoglu S., Ozdemir A., Hatipoglu N. Neonatal hipopituitarism: approaches to diagnosis and treatment // J Clin Res Pediatr Endocrinol. — 2019; 11 (1): 4-12.ссылка
Дедов И. И., Мельниченко Г. А., Фадеев В. В. Эндокринология. — М., 2015. — С. 59.
Дедов И. И., Петеркова В. А., Малиевский О. А. Детская эндокринология. — М., 2016. — С. 9.
Дедов И. И., Мельниченко Г. А. Эндокринология. Национальное руководство. Краткое издание. — 2-е изд., перераб. и доп. — М.: ГЭОТАР-Медиа, 2018. — 832 с.
Young W. F. The netter collection of medical illustrations: the endocrine system / 2 edition. — 2011. — С. 12.
Камачо П., Гариба Х. Доказательная эндокринология. — М., 2009. — С. 58.

