Определение болезни. Причины заболевания
Гастроинтестинальные стромальные опухоли, или ГИСО (Gastrointestinal stromal tumors), — это группа доброкачественных и злокачественных новообразований, которые обычно развиваются в различных отделах пищеварительной системы. Чаще всего страдает желудок и тонкая кишка.
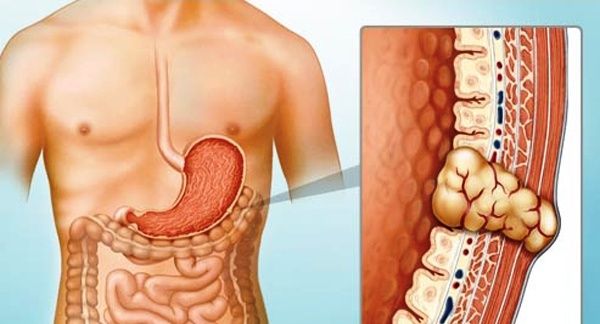
Гастроинтестинальная стромальная опухоль желудка
Причины ГИСО
Известно, что ГИСО развиваются в организме человека из той же клеточной линии, из которой происходят клетки Кахаля, управляющие моторикой (сокращениями) стенок желудка и кишечника. Можно предположить, что именно эти клетки — источник злокачественного процесса, но однозначных доказательств этому нет [4].
Любое злокачественное новообразование — результат мутаций в определённых генах. Из-за них клетки начинают быстро размножаться, становятся «бессмертными», приобретают способность распространяться по организму.
Известно, что 85–90 % спорадических (случайных) ГИСО развиваются из-за мутаций в генах рецептора тирозинкиназы под названием KIT (CD 117) или рецептора фактора роста тромбоцитов α под названием PDGFRA [5]. Эти же мутации способны передаваться от родителей детям, и они ответственны за редкие семейные случаи ГИСО [7].
ГИСО, не связанные с мутациями в KIT и PDGFRA, относятся к дикому типу, так как встречаются реже остальных. В этих опухолях обнаруживаются мутации в генах NF1, BRAF, HRAS и др. Некоторые из них возникают как проявления других заболеваний (опухолевых синдромов): нейрофиброматоза 1-го типа, синдрома Карнея — Стратакиса или триады Карнея.
О факторах риска развития ГИСО известно мало. К ним можно отнести возраст старше 50 лет и уже упомянутые опухолевые синдромы.
Распространённость
ГИСО составляют менее 1 % от всех злокачественных новообразований пищеварительной системы, но это самые распространённые мезенхимальные опухоли желудочно-кишечного тракта (ЖКТ), т. е. происходящие из соединительной ткани [1].
Более половины всех ГИСО (больше 60 %) обнаруживаются в желудке, около 30 % — в тонкой кишке [2]. Реже ГИСО встречаются в других отделах пищеварительного тракта и за его пределами [3].
В западных странах распространённость ГИСО составляет менее 1 случая на 10 тыс. [4], а по другим источникам — 1–1,5 случая на 100 тыс. населения в год [5][6]. Средний возраст диагностики заболевания — 60 лет. Мужчины и женщины болеют одинаково часто [4].
Около 70 % ГИСО — доброкачественные, и только 30 % — злокачественные [4].
Симптомы гастроинтестинальной стромальной опухоли
До 75 % всех ГИСО выявляются случайно, когда опухоль ещё небольшая (до 4 см) и не вызывает симптомов либо проявляется неспецифическими признаками, которые могут возникать и при других заболеваниях [1].
Зачастую врачи устанавливают диагноз во время манипуляций по другим поводам:
- рентгенографии с контрастированием (вводом специальной жидкости для улучшения изображения);
- эндоскопических исследований (осмотра внутренних органов с помощью гибкой трубки с камерой);
- операций.
К неспецифическим симптомам ГИСО относятся:
- боль или дискомфорт в животе (самое распространённое проявление);
- быстрое чувство насыщения после приёма небольшого количества пищи;
- снижение аппетита и беспричинная потеря веса;
- повышенная утомляемость, постоянное чувство усталости и недомогание;
- плохая переносимость физических нагрузок и одышка [1];
В редких случаях, если опухоль уже достигла больших размеров, её можно прощупать.
Особенность ГИСО в том, что они легко повреждаются и начинают кровоточить. Зачастую это и помогает их обнаружить.
Такие симптомы в подавляющем числе случаев встречаются при многих других заболеваниях и функциональных расстройствах, а иногда просто из-за погрешностей в рационе. Если эти проявления сохраняются в течение нескольких дней и состояние ухудшается, нужно обязательно обратиться к врачу.
Патогенез гастроинтестинальной стромальной опухоли
Чаще всего ГИСО появляются из-за мутаций, возникших в отдельных клетках тела спонтанно в течение жизни, а наследственные формы встречаются крайне редко. Изменения в генах приводят к тому, что клетки начинают быстрее размножаться. Сначала развивается гиперплазия (чрезмерное разрастание ткани), а затем неоплазия (образование опухоли). Большая часть ГИСО — доброкачественные, но некоторые становятся злокачественными. Они начинают врастать в окружающие ткани и распространяться по организму [4].
Чаще всего ГИСО — одиночные новообразования. В более редких случаях, например у детей, встречаются множественные очаги. Опухоли могут быть размером от менее 1 см до 40 см [1]. Характер их роста бывает разным:
- Интралюминальным — внутрь просвета поражённого органа. Ярко выраженные симптомы появляются, когда такая опухоль начинает кровоточить или достигает больших размеров и перекрывает просвет органа.
- Экстралюминальным — наружу. Симптомы могут очень долго отсутствовать и появляются, когда новообразование достигает больших размеров.
При поздних стадиях злокачественных ГИСО возникают отдалённые метастазы (вторичные опухоли). Чаще всего они распространяются гематогенным путём (с током крови) в печень и брюшину — тонкую оболочку, выстилающую брюшную полость. Метастазирование лимфогенным путём (через лимфатические сосуды) с поражением лимфоузлов для ГИСО нехарактерно [1].
Классификация и стадии развития гастроинтестинальной стромальной опухоли
Гистологически (по типу тканей) выделяют 3 типа ГИСО:
- Веретеноклеточный. Наиболее распространён, встречается в 70 % случаев. При изучении опухолевой ткани под микроскопом клетки в ней располагаются в виде пучков или завитков. Подтипы:
- палисадно-вакуолизированный (клетки расположены в виде забора, а внутри содержат органеллы с жидкостью);
- склерозирующий (с большим количеством соединительной ткани);
- саркоматозный (с агрессивным ростом клеток);
- гиперклеточный (клетки расположены близко друг к другу).
![Веретеноклеточный тип ГИСО [12] Веретеноклеточный тип ГИСО [12]](/media/bolezny/gastrointestinalnaya-stromalnaya-opuhol/veretenokletochnyy-tip-giso-12_s.jpeg?dummy=1755257074689)
Веретеноклеточный тип ГИСО [12]
- Эпителиоидноклеточный. Составляет 20 % от всех ГИСО. В таких опухолях клетки располагаются рассеянно или в виде гнёзд (скоплений). Подтипы:
- склерозирующий с синцитиальной структурой (преобладает соединительная ткань, состоящая из крупных клеток с несколькими ядрами);
- склерозирующий с гнёздчатой структурой;
- гиперклеточный стромальный (клетки соединительной ткани расположены близко друг к другу);
- саркоматозный.
![Эпителиоидноклеточный тип ГИСО [12] Эпителиоидноклеточный тип ГИСО [12]](/media/bolezny/gastrointestinalnaya-stromalnaya-opuhol/epitelioidnokletochnyy-tip-giso-12_s.jpeg?dummy=1755257095256)
Эпителиоидноклеточный тип ГИСО [12]
- Смешанный. Встречается в 10 % случаев. Выглядит под микроскопом как смесь веретеноклеточной и эпителиоидноклеточной опухоли [4][5][9].
Система стадий ГИСО довольно сложна. Она учитывает не только общепринятые параметры: T (первичная опухоль), N (поражение лимфоузлов) и M (отдалённые метастазы), но и митотический индекс (МИ) — показатель, характеризующий то, насколько активно в опухоли происходят клеточные деления. Чем выше митотический индекс, тем быстрее делятся клетки и тем агрессивнее опухоль. Критерии определения стадии различаются в зависимости от расположения новообразования [6].
Выделяют следующие стадии:
Осложнения гастроинтестинальной стромальной опухоли
Многие из осложнений ГИСО — экстренные состояния, которые сильно ухудшают самочувствие, создают угрозу для жизни и требуют немедленной операции. К осложнениям относятся:
- Кровотечение. Его симптомы зависят от того, насколько оно сильное и где находится источник:
- сильное кровотечение в пищеводе или желудке — рвота с примесью алой крови, а если кровь подвергается воздействию соляной кислоты и ферментов в желудке — рвота «кофейной гущей»;
- выраженное кровотечение в желудке или тонкой кишке — мелена (чёрный кал, который внешне напоминает дёготь);
- сильное кровотечение в толстой кишке — примесь свежей крови в кале;
- слабое кровотечение без симптомов (хроническое) — развитие анемии (снижение гемоглобина и эритроцитов в крови), которая проявляется бледностью, головной болью, слабостью, головокружениями и обмороками [3].
- Обструкция (непроходимость). Если опухоль достигает больших размеров и перекрывает определённый участок пищеварительного тракта, то возникают специфичные (характерные) симптомы, и по ним можно судить о том, в каком месте находится новообразование:
- при обструкции пищевода — нарушение прохождения пищи и ощущение, что еда застревает в горле;
- при обструкции двенадцатиперстной кишки (ДПК) — рвота, механическая желтуха (из-за нарушения оттока желчи), которая проявляется пожелтением и зудом кожи, а также болью в правом подреберье;
- при обструкции толстой или прямой кишки — кишечная непроходимость, которая может выражаться запорами, вздутием живота и болями [1].
- Перфорация. Из-за разрушения опухоли в стенке органа образуется сквозное отверстие.
- Перитонит. Из-за перфорации кишечника возникает воспаление в брюшной полости [8].

Перитонит
Диагностика гастроинтестинальной стромальной опухоли
Диагностика начинается со сбора жалоб, анамнеза (истории жизни и болезни) и осмотра. Доктор может заподозрить ГИСО, если пациент жалуется, например, на боль в животе, рвоту с примесью крови или свежую кровь в кале. Если опухоль большая, врач может её прощупать при осмотре. Но основное значение имеет инструментальная диагностика.
Инструментальная диагностика
1. Компьютерная томография (КТ). С неё начинают обследование во многих случаях при подозрении на опухоль в брюшной полости. В ходе исследования используют внутривенное или пероральное (с применением растворов для проглатывания) контрастирование. Благодаря ему ГИСО на снимках хорошо видны. КТ позволяет оценить размеры, расположение опухоли и степень её распространения в соседние органы [5].
2. Магнитно-резонансная томография (МРТ). Она бывает нужна, чтобы определить степень распространения рака и выявить отдалённые метастазы и рецидивы. Иногда с неё начинают обследование вместо КТ, если пациенту противопоказано рентгеновское облучение или нельзя вводить контрастные растворы с йодом.
3. Позитронно-эмиссионная томография (ПЭТ/КТ)с контрастированием радиофармпрепаратом (радиоактивным изотопом). Помогает уточнить диагноз, если он не ясен после КТ и МРТ, а также выявить опухолевые очаги в разных частях организма.
4. Эндоскопические методы диагностики. Гастроскопия и колоноскопия (обследования с помощью гибкой трубки с камерой) особенно предпочтительны, когда есть симптомы желудочно-кишечного кровотечения [5]. Во время эндоскопии можно провести биопсию — получить образец опухолевой ткани для исследования. Также можно выполнить эндоУЗИ (эндосонографию) — ультразвуковое исследование с помощью миниатюрного датчика на конце эндоскопа. Это помогает отличить ГИСО от других опухолей (любых, которые бывают в пищеварительном тракте). Под контролем эндоУЗИ в опухоль можно ввести иглу и выполнить биопсию.
С помощью классических эндоскопических методик легко исследовать пищевод, желудок, двенадцатиперстную, толстую и прямую кишку. С основной частью тонкой кишки возникают проблемы, потому что она длинная и в ней много изгибов. В этом случае можно применить другие виды диагностики:
- Видеокапсульную эндоскопию. Её проводят с помощью маленькой капсулы со встроенными камерами. Пациента просят её проглотить, она проходит через пищеварительный тракт и делает снимки.
- Двухбаллонную энтероскопию. Для её проведения используют специальный эндоскоп [11]. Он состоит из двух трубок, вставленных одна в другую. Врач вводит в кишку тонкую внутреннюю трубку, выдвигая её из внешней более толстую, и раздувает на её конце маленький баллончик, чтобы зафиксировать. Затем продвигает вперед внешнюю трубку и раздувает баллончик на ней. Баллончик на тонкой трубке сдувают, продвигают её ещё вперёд, а далее повторяют действия. Так эндоскоп постепенно «ползёт» по кишке. Рутинно этот метод не применяют.

Гастроскопия
Лабораторная диагностика
- Исследование опухолевых биоптатов. Играет ключевую роль в диагностике ГИСО, так как позволяет не только изучить ткани новообразования под микроскопом, но и провести иммуногистохимическое исследование. Оно помогает выявить аномальные белки, которые производятся в злокачественных клетках в результате генетических мутаций [5]. Благодаря этим исследованиям можно выяснить, доброкачественное образование или нет.
- Общий анализ крови. Помогает обнаружить анемию при хроническом кровотечении.
- Биохимический анализ крови. С помощью него исследуют «печёночные» показатели, если есть подозрение, что опухолевый процесс мог распространиться в печень [3].
Лечение гастроинтестинальной стромальной опухоли
Иногда при небольшой ГИСО врач может не проводить лечение, а просто наблюдать за новообразованием. В большинстве же случаев прибегают к операции.
Цель радикальной операции:
- полностью удалить новообразование;
- обеспечить негативный край резекции — при изучении под микроскопом ткани возле линии разреза не должно быть опухолевых клеток;
- не повредить псевдокапсулу опухоли — структуру из сдавленных окружающих тканей.
Так как ГИСО практически никогда не распространяются в близлежащие лимфоузлы, удалять их, как это делают при других злокачественных опухолях, не нужно [5][6].
Операция может быть выполнена открытым (через разрез) или лапароскопическим (через проколы) способом. Обычно лапароскопическая хирургия рекомендуется, если диаметр опухоли менее 5 см. В противном случае можно повредить псевдокапсулу, и это приведёт к обсеменению операционной раны злокачественными клетками, что повысит риск рецидива.
Даже если ГИСО достигла больших размеров и вторглась в соседние органы, зачастую её всё ещё можно полностью удалить. Если опухоль очень большая, то проводят неоадъювантную (предоперационную) таргетную терапию: на фоне применения противоопухолевых препаратов новообразование уменьшается и его становится проще удалить [5].
В случае с отдалёнными метастазами решение принимают индивидуально. Единичные очаги часто получается удалить хирургически [10]. Если операция невозможна, то основное лечение — таргетная терапия.
Противоопухолевые препараты
Классические химиопрепараты при ГИСО применяются крайне редко, так как они малоэффективны и практически не влияют на размеры таких опухолей [9].
Революция в лечении ГИСО произошла после открытия роли мутаций в генах KIT и PDGFRA. Оказалось, что эти генетические изменения делают опухоли чувствительными к таргетным препаратам, блокирующим фермент тирозинкиназу. Из-за мутаций он способствует быстрому и бесконтрольному размножению клеток, а препарат подавляет активность этого фермента [2][9].
Ингибиторы тирозинкиназы применяются на разных этапах лечения:
- перед операцией — чтобы уменьшить очень большую опухоль и сократить объём хирургического вмешательства;
- после операции — чтобы предотвратить рецидив заболевания;
- при опухоли на поздней стадии — как основной метод лечения, чтобы замедлить прогрессирование болезни и продлить жизнь пациента [3].
Другие методы лечения
Лучевая терапия, как и классическая химиотерапия, низкоэффективна при ГИСО, и её практически не применяют. В некоторых случаях она помогает уменьшить мучительные симптомы, например боли в костях.
При IV стадии ГИСО часто метастазируют в печень. В таких случаях, если невозможно хирургическое лечение, хорошим решением становится применение абляционных или эмболизационных методик.
- Абляционные методы. Предполагают уничтожение опухолевой ткани с помощью высоких и низких температур или агрессивных химических веществ. Чаще всего прибегают к радиочастотной абляции (РЧА). В очаг внутри печени под контролем ультразвука или компьютерной томографии вводят иглу-электрод и подают в неё электрический ток высокой частоты. За счёт этого опухолевая ткань сильно нагревается и её клетки погибают. Также применяют микроволновую, крио- и этаноловую абляцию.
- Эмболизация. Это метод интервенционной (эндоваскулярной) хирургии. Во время процедуры делают небольшой надрез в верхней части бедра, заводят в бедренную артерию катетер, продвигают его до кровеносного сосуда, питающего опухоль, и заполняют его микроскопическими эмболизирующими частицами, чтобы закупорить сосуды. В итоге нарушается поступление кислорода и питательных веществ к опухолевой ткани. У этого метода есть разновидности:
- химиоэмболизация — вместе с эмболизирующими частицами вводят химиопрепарат;
- радиоэмболизация — в качестве эмболизирующих частиц используют микроскопические радиоактивные сферы.
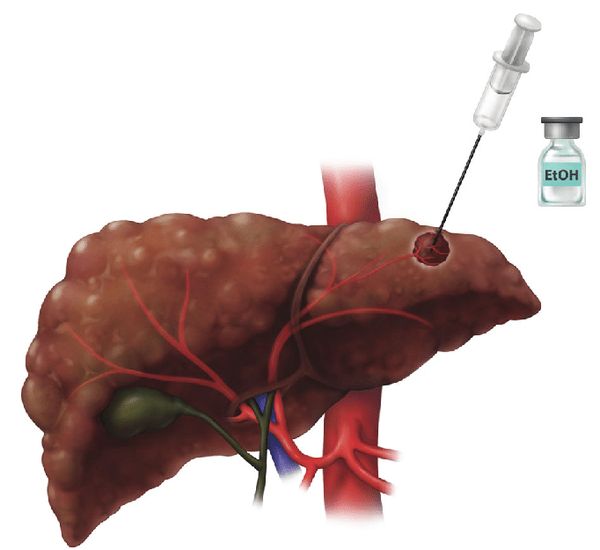
Этаноловая абляция. В опухоль печени вводят чистый этанол
Прогноз. Профилактика
Прогноз при ГИСО зависит от размера опухоли, её МИ и расположения: например, ГИСО в желудке обычно менее агрессивны, чем в тонкой кишке [1]. Риск рецидива наиболее низкий, если получилось удалить новообразование полностью, не вскрыть псевдокапсулу и добиться негативного края резекции.
Показатели пятилетней выживаемости при всех типах ГИСО, по данным Американского онкологического общества, составляют:
- 95 % — если опухоль не распространилась;
- 84 % — если опухоль распространилась в регионарные лимфоузлы и соседние органы;
- 52 % — если есть отдалённые метастазы [3].
После завершения лечения ГИСО могут рецидивировать, поэтому пациент должен наблюдаться у онколога и проходить контрольные обследования (обычно они включают КТ, но могут быть назначены и другие методы диагностики). В первые несколько лет посещать врача нужно каждые 3–6 месяцев, затем промежутки увеличиваются.
О факторах риска развития ГИСО, связанных с образом и условиями жизни, неизвестно, поэтому и эффективных мер профилактики не существует.
Список литературы
Choti M. A. Gastrointestinal Stromal Tumors (GISTs) // Medscape. — 2022.
Никулин М. П., Архири П. П., Владимирова Л. Ю., Мещеряков А. А. и др. Практические рекомендации по лекарственному лечению гастроинтестинальных стромальных опухолей. Злокачественные опухоли // Практические рекомендации RUSSCO. — 2021. — Т. 11, № 3s2. — С. 490–498.
Gastrointestinal Stromal Tumor (GIST) // American Cancer Society. [Электронный ресурс]. Дата обращения: 14.08.2025.
Burch J., Ahmad I. Gastrointestinal Stromal Cancer // Treasure Island (FL): StatPearls Publishing. — 2024. ссылка
Ассоциация онкологов России. Гастроинтестинальные стромальные опухоли: клинические рекомендации. — М., 2020. — 45 с.
Casali P. G., Blay J.-Y. Клинические рекомендации ESMO по диагностике, лечению и наблюдению при гастроинтестинальных стромальных опухолях (GIST) // Минимальные клинические рекомендации европейского общества медицинской онкологии (esmo). — М., 2010. — С. 147–154.
Ахметзянов Ф. Ш., Петров С. В., Халиков Д. Д. Молекулярно-генетические особенности гастроинтестинальных стромальных опухолей // Вопросы онкологии. — 2019. — Т. 65, № 1. — С. 65–76.
Sorour M. A., Kassem M. I., Ghazal A. E.-H. A., El-Riwini M. T. et al. Gastrointestinal stromal tumors (GIST) related emergencies // Int J Surg. — 2014. — Vol. 12, № 4. — P. 269–280.ссылка
Корнилова А. Г., Когония Л. М., Мазурин В. С., Морданов С. В. и др. Гастроинтестинальные стромальные опухоли: что нового в терапии? // Сибирский онкологический журнал. — 2015. — № 2. — С. 81–87.
Коржева И. Ю., Чернеховская Н. Е., Волова А. В., Бурдюков М. С. и др. Гастроинтестинальные стромальные опухоли — лечебно-диагностический алгоритм // ЭиКГ. — 2023. — Т. 213, № 5. — С. 108–113.
Nakatani M., Fujiwara Y., Nagami Y., Sugimori S. et al. The usefulness of double-balloon enteroscopy in gastrointestinal stromal tumors of the small bowel with obscure gastrointestinal bleeding // Intern Med. — 2012. — Vol. 51, № 19. — P. 2675–2682.ссылка
Hu S., Alpert L., Cates J. M. M., Gonzalez R. S. Gastrointestinal stromal tumors (GISTs) arising in uncommon locations: clinicopathologic features and risk assessment of esophageal, colonic, and appendiceal GISTs // Modern Pathology. — 2022. — № 35. — P. 554–563.

